09/04/2019
Site Natura 2000 Petite Montagne du Jura. Ça grouille dans la mare
Site Natura 2000 Petite Montagne du Jura.
Ça grouille dans la mare !

Sortie / pique-nique autour de l'eau
Non, il ne s’agit pas de déguster des cuisses de grenouilles ou des brochettes de libellules ! Mais plutôt de discuter ensemble de la vie d’une mare, des espèces incroyables qui la peuplent, des bons gestes pour l’entretenir… Tout en partageant pique-nique et boissons (on essaiera quand même de ne pas trop parler la bouche pleine).
Sortie organisée samedi 27 avril
Rendez-vous à 11h devant la mairie de Maisod (prévoir un pique-nique)
Inscription au 03 84 48 85 15
Animé par Jura nature Environnement
L’équipe Natura 2000
Site Natura 2000 Petite Montagne du Jura
http://petitemontagnedujura-n2000.fr
natura2000@petitemontagne.fr
03 84 25 39 78
11:18 Publié dans Herpétologie, Insectes, Mollusques, Ornithologie, Poissons, Sorties terrain | Tags : site natura 2000 petite montagne du jura, faune et flore de la mare | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
21/03/2019
Sorties nature












18:27 Publié dans Art et Nature, Environnement-Écologie, Géologie-hydrogéologie-Climatologie, Herpétologie, Insectes, Invertébrés, Limnologie-hydrobiologie, Mammifères, Mollusques, Mycologie, Ornithologie, Patrimoine franc-comtois et jurassien, Poissons, Sorties terrain | Tags : sorties nature du doubs | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
30/06/2018
Embrassades entre limaces léopards
Embrassades entre limaces léopards
par André Guyard
En Franche-Comté, le mois de juin 2018 fut ensoleillé et très sec. Mais la température ressentie fut modérée par une violente bise. Ce samedi 30 juin vers six heures du matin, j'ai pu observer une étreinte de deux limaces léopards qui avaient escaladé la façade sud-est de ma maison et qui étaient étroitement enlacées.

Étreinte entre deux limaces léopards
L'étreinte dura une demi-heure environ et je restai à l'affût pour guetter l'enlacement des pénis des deux congénères de cette espèce hermaphrodite. Malheureusement, il ne s'agissait que d'une simple embrassade et l'un des individus quitta son congénère dans un parcours vertical descendant abandonnant une piste de mucus.
Au bout d'une vingtaine de cm, il se ravisa, fit volte-face et se mit à brouter son chemin de mucus.

Dans cette nouvelle ascension, on peut voir
le pneumostome grand ouvert

Bon appétit !
Le partenaire supérieur entreprit alors une descente le long du ruban de mucus pour prendre part à la dégustation.

À la rencontre l'un de l'autre
Au contact de l'autre, le partenaire inférieur fit alors demi-tour pour s'enfuir et regagner l'horizontalité de la terrasse, puis l'ombre du feuillage.

Traversée de la terrasse
En conclusion : un simple flirt, sans fécondation réciproque !
08:40 Publié dans Mollusques | Tags : limax maximus, limace léopard, andré guyard | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
28/09/2017
Offres de stages


15:43 Publié dans Actualité des Sciences, Insectes, Mollusques, Sorties terrain | Tags : nacré de la canneberge, boloria aquilonaris, vertigo septentrional, vertigo geyerijura | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
24/01/2016
Quels poissons et quels fruits de mer peut-on encore manger l'esprit tranquille ?
Quels poissons et quels fruits de mer peut-on encore manger l'esprit tranquille ?


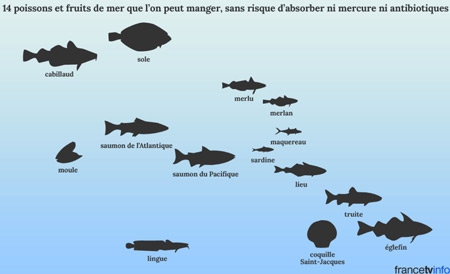

Pour en savoir plus : Article de Francetvinfo
08:43 Publié dans Mollusques, Poissons | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
10/05/2011
OGM : de la toxine Bt retrouvée dans le sang de femmes enceintes et de leurs fœtus au Québec
OGM : de la toxine Bt retrouvée dans le sang de femmes enceintes et de leurs fœtus au Québec

D'après Greenpeace, une étude indépendante réalisée à Sherbrooke auprès de femmes enceintes, de leurs fœtus et de femmes non enceintes révèle la présence de résidus de pesticides issus d’aliments transgéniques dans le sang de chacun de ces groupes. Des résidus de glyphosate et de glufosinate (herbicides couramment utilisés lors de la culture de certaines plantes génétiquement modifiées) ont également été retrouvés.
Une étude scientifique publiée en avril par des chercheurs de l’Université de Sherbrooke au Canada, fait état de résultats inédits jusqu’ici.
Les auteurs concluent à la nécessité de poursuivre les analyses d’impact des organismes génétiquement modifiés (OGM) sur les humains. Professeur-chercheur au département de gynécologie-obstétrique de la faculté de médecine de l’Université de Sherbrooke, Aziz Aris s’intéresse particulièrement à la toxicité d’origine environnementale sur les fœtus et les mères. Or, dit-il, l’impact des OGM a été abondamment testé sur les animaux, mais jamais sur les humains. C’est la première fois que la présence de résidus de pesticides d’OGM dans le sang des femmes est démontrée. Ces femmes et leur conjoint, étant citadins et n’ayant jamais travaillé au contact de pesticides, ces résultats résulteraient donc principalement de leur alimentation.
Les résultats de l’étude, financée par un fonds québécois de recherche en santé, seront publiés dans la revue scientifique américaine Reproductive Toxicology.
Environ 70% du maïs au Québec est génétiquement modifié (OGM) et inclut la toxine Bt.
Cette étude scientifique indépendante confirme les pires craintes de Greenpeace sur le manque de rigueur, d’indépendance et de transparence des études menées par les entreprises de biotechnologies.
Comme les autorités gouvernementales canadiennes refusent toujours d’appliquer le principe de précaution, les citoyens sont traités comme des cobayes par le gouvernement fédéral. Au Canada comme en Europe, les OGM sont toujours approuvés sans études sérieuses et indépendantes. Il est temps de sortir de l’obscurantisme !
Combien d’études scientifiques indépendantes seront nécessaires pour que les autorités gouvernementales exigent des entreprises de biotechnologies des preuves de l’innocuité des OGM ?
15:01 Publié dans Biologie, Environnement-Écologie, Mollusques, Nature et santé, Pollution | Tags : ogm, pesticides, femmes enceintes, foetus, glyphosate, glufosinate | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
17/04/2010
La Moule perlière d'eau douce

La Moule perlière d'eau douce
Margaritifera margaritifera (L. 1758)
Famille des Margaritiféridés
par André Guyard
Pour s'assurer de la qualité des eaux douces, l'Onema inspecte 1500 sites de rivières tous les deux ans et 200 lacs tous les six ans.
La directive-cadre européenne (DCE) exige de définir les équilibres naturels entre espèces ainsi que la productivité optimale d'une rivière. Cette dernière se calcule en kilos de poissons par hectare de rivière. Pour l'instant, on estime qu'une rivière à cyprinidés "produit" de 200 à 600 kilos de poissons par hectare... une fourchette trop vaste pour avoir une idée précise du "bon état écologique" exigé par la DCE. Mais on manque de références historiques comme l'explique Philippe Barran : «La morphologie de presque tous nos cours d'eau a été modifiée depuis la révolution industrielle.»
Pour essayer de définir un bon état écologique de base, la meilleure approche est d'étudier la petite centaine de ruisseaux qui ont traversé les siècles sans dommages : le Chabot, la Lamproie de Planer, l'Écrevisse à pattes blanches et la Moule perlière y vivent encore. Ces quatre espèces sont évaluées dans le Morvan par un programme européen Life. Ces espèces sentinelles de la qualité des sites aquatiques sont appelées espèces indicatrices.
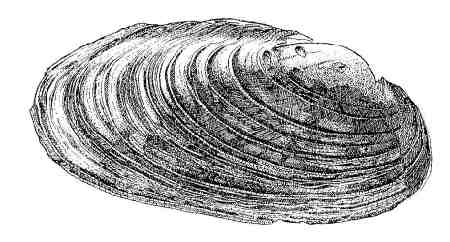
Parmi les espèces indicatrices de la qualité des sites aquatiques d'eau douce est la Mulette perlière ou Moule perlière (Margaritifera margaritifera). En France, son aire de répartition couvre l'essentiel des massifs cristallophylliens du territoire métropolitain français : Massif Armoricain, Massif Central, Morvan, Alpes et Pyrénées, à l'exclusion du bassin du Rhône. Elle était jadis si abondante que ses perles ont orné colliers et parures jusqu'au milieu du XXe siècle. C'est un mollusque lamellibranche des rivières claires d'Europe, de Russie, du Canada et de la façade Est des États-Unis, une espèce désormais protégée et connue pour sa durée de vie exceptionnelle (plus d'un siècle). Dans la nature, on rencontre une perle pour mille individus. À l'occasion du baptême de son fils, le futur Louis XIII, Marie de Médicis exigea une robe entièrement recouverte de milliers de perles venues des rivières françaises. On imagine l'hécatombe engendrée par ce caprice royal !
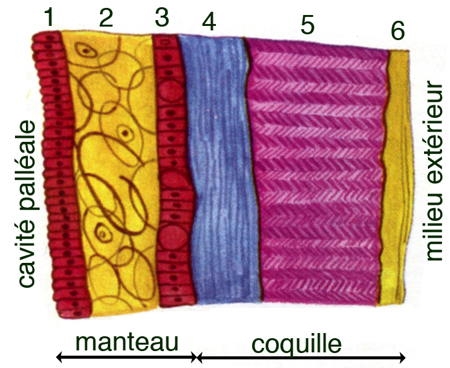
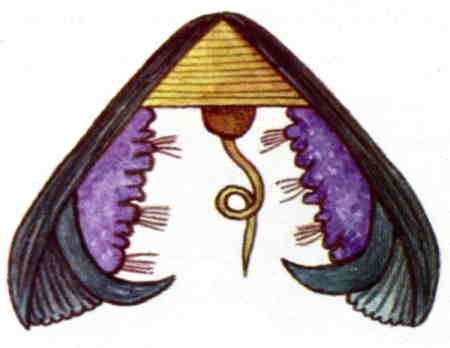
Le schéma ci-dessus montre une coupe de la coquille et du manteau d'une moule.
Le manteau est un repli tégumentaire qui enveloppe le corps de la moule. L'épiderme (en rouge) est replié sur le derme (2 en jaune). Sa face externe (3) secrète la coquille et la face interne (1) limite la cavité palléale.
La coquille présente trois couches : une couche externe : la cuticule ou périostracum (6 en jaune), pellicule cornée formée d'une substance organique la conchyoline ; une couche moyenne ou ostracum (5 en violet), formée de prismes constitués par des lames calcaires noyés dans de la conchyoline ; une couche interne, la nacre ou hypostracum (4 en bleu) formée de minces lamelles de conchyoline imprégnées de calcaire. Les interférences entre les rayons lumineux réfléchis par ces différentes lamelles donnent une irisation particulière à la nacre. Cette couche lamelleuse est sécrétée par toute la surface de la face externe du manteau. De sorte que l'accroissement en épaisseur de la coquille est due uniquement à la nacre qui participe à la réparation des brèches de la coquille et éventuellement à la formation de perles englobant des particules introduites accidentellement entre manteau et coquille. Ainsi, le germe d'une perle peut être un fragment de manteau voire un débri de coquille ou même un microinvertébré.

La Mulette est un mollusque lamellibranche qui se reconnaît à sa forme allongée. Les adultes mesurent de 8 à 14 cm et vivent aux deux tiers enfoncés dans le sédiment (sable ou gravier), en position quasi verticale. La Mulette filtre ainsi environ 50 litres d'eau par jour, se nourrissant des particules véhiculées par les courants. Pour résister au froid, elle exige un substrat gravillonnaire, voire sableux, lui permettant de s'enfouir, parfois plusieurs années. Elle est donc très sensible à la sédimentation des rivières constituant son habitat : la baisse des débits, colmatant les fonds, entraîne systématiquement sa disparition, bien qu'on observe parfois des déplacements volontaires de sujets adultes (baisse des niveaux d'eau ou augmentation de la turbidité).
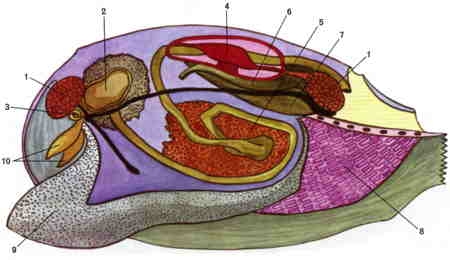
Dissection de la Mulette
Le schéma ci-dessus représente une dissection de la Mulette. 1. : muscles adducteurs ; 2. : estomac ; 3. : bouche ; 4. : ventricule cardiaque ; 5. : gonade ; 6. : canal excréteur ; 7 : rein ; 8. : branchie ; 9 : pied ; 10. : palpes labiaux.
Biologie
L'espèce a besoin d'une eau bien oxygénée pour assurer un cycle de reproduction complexe. "Cela impose qu'on ne perturbe pas la morphologie d'une rivière et que les eaux restent pures. Deux conditions qui n'ont cessé de reculer", explique Pierre Durlet, gérant du programme du Morvan. La France aura donc atteint le bon état écologique de ses eaux quand on reverra en bijouterie des colliers de perles de moule. C'est en tout cas le but recherché par les écologues. Les gestionnaires de l'eau se contenteraient de beaucoup moins.
Le cycle de vie de la Moule perlière est associé à celui de la Truite fario et à celui du Saumon atlantique, car les larves du mollusque se développent à l'abri des branchies de ces poissons, et uniquement de ceux-ci.
Les sexes sont séparés. Pour la reproduction, le mâle libère ses spermatozoïdes dans l'eau, ils rejoignent alors les ovules, très abondants de la femelle. Après fécondation, l'œuf commence son développement dans la cavité palléale de la femelle. Il évolue en une larve, nommée glochidium, qui est incubée par la femelle pendant un mois. La taille de 0,05 mm atteinte, la larve est libérée dans le cours d'eau. Le glochidium est doté d'une coquille bivalve pourvue d'un crochet recourbé à l'intérieur et d'une sorte de filament adhésif. Cette larve va se fixer sur l'appareil branchial d'une Truite fario ou d'un Saumon atlantique, provoquant chez son hôte la formation d'une tumeur où se développe le glochidium, qui se nourrit par la surface de son manteau. Cette phase parasitaire dure en général quelques semaines (jusqu'à 10 mois), temps au bout duquel le glochidium devient un véritable bivalve en miniature de 0,5 mm. La larve s'enkyste alors dans les sédiments durant plusieurs années et poursuit sa croissance, pour atteindre sa maturité sexuelle à 20 ans.
La larve glochidium
La longévité de cette espèce est remarquable, puisqu'elle varie entre 20 et 30 ans pour les individus vivant dans les eaux plus chaudes du sud de l'Europe, à plus de 150 ans pour ceux de Scandinavie.
État des populations
Cette moule constitue un excellent indicateur écologique. L'habitat de la Moule perlière correspond à des eaux fraîches, courantes, pauvres en calcaire, à fond de gravier ou de sable mais dépourvu de vase. Elle tolère très mal la présence de phosphates, ne supporte pas des eaux avec plus de 5 mg/l de nitrate et ne peut se reproduire avec plus de 1 mg/l ! (rappelons que la norme autorisée est 50 mg/l).

En tant que filtreur, elle accumule de nombreux toxiques (métaux lourds, pesticides...) qui peuvent la tuer ou nuire à ses capacités de développement et de reproduction. Il est possible que les perturbateurs endocriniens soient également un facteur de régression de l'espèce, comme c'est démontré pour d'autres mollusques.
La création de lacs de retenue (absence de courant), de microcentrales électriques (changement des débits), les pratiques agricoles (eutrophisation des cours d'eau, pollution par les pesticides, augmentation de l'érosion des sols et par suite de la turbidité), ainsi que l'introduction de truites arc-en-ciel (impropres au développement du glochidium) ont entraîné la quasi-disparition de cette espèce sur pratiquement toute son aire de répartition.
D'où le statut particulier de cette espèce, qui relève de l'annexe III de la Convention de Berne et sa cotation UICN : menacée d'extinction.
Protection
Suite au Grenelle de l'Environnement, la France a prévu un plan de restauration national, à décliner régionalement. La Directive cadre sur l'eau devrait contribuer à la restauration de la bonne qualité écologique des cours d'eau et des bassins versants, mais un certain nombre de paramètres critiques dont la turbidité restent préoccupants, voire montrent une dégradation. Le réchauffement climatique en mettant en été à sec les parties amont de cours d'eau est également un facteur de risque supplémentaire puisque Margaritifera margaritifera dépend de la présence de jeunes salmonidés, Saumon ou Truite fario.
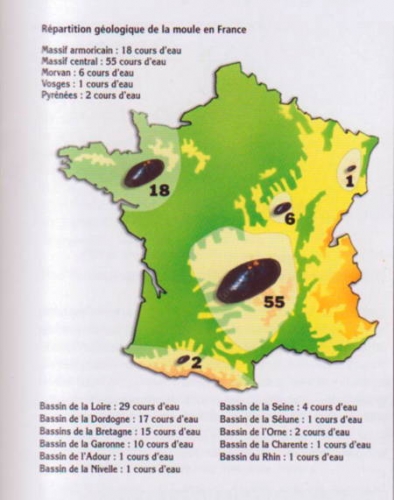
C'est une espèce menacée de disparition en Europe de l'Ouest en 2008. En France, la moule perlière est encore présente dans une centaine de rivières en France suite au recensement réalisé par Gilbert Cochet dans les années 1990.
La production de perles de culture en Chine
En Chine, l'élevage de moules d'eau douce en vue de la production de perles de culture peut se pratiquer en lac naturel, en réservoir ou en étang.

Aquaculture de moules perlières au centre piscicole du District de Qingpu (Shanghai)
(Cliché F.A.O.)
Trois espèces de moules perlières y sont élevées en étang: Hyriopsis cumingi (la meilleure), Cristaria plicata et Anodonta woodiana. Pour provoquer la formation de perles, on implante manuellement, entre le manteau et la coquille de chaque moule perlière, plusieurs dizaines de petits morceaux du manteau de moules sacrifiées. L'on utilise ainsi en moyenne quatre manteaux par moule perlière et un ouvrier spécialisé peut préparer environ 30 moules perlières par jour.


Ces moules sont ensuite placées en étang, suspendues individuellement à un fil vertical. La densité de stockage est de 150-225 individus par 100 m2 de plan d'eau. Après deux étés (température de l'eau 20-25°C), l'on récolte jusqu'à 40-50 perles de culture par moule, en fonction du nombre de noyaux implantés.

La qualité des perles ainsi produites est très variable. Même si, étant principalement destinées en Chine à l'usage médicinal, leur forme et leur qualité n'ont pas la même importance qu'au Japon, leur prix peut varier du simple au triple selon qu'elles se classent en quatrième (700 yuans/kg) ou en première (2 000 yuans/kg) catégorie.


En moyenne, 100 moules perlières produisent 0,5 kg de perles de culture, soit un rendement de 0,75-1,125 kg par 100 m2 d'étang. Le revenu de cette activité aquacole peut donc être intéressant si la qualité des perles produites est bonne, particulièrement lorsque cet élevage se fait en lac naturel et en réservoir où il permet d'intensifier l'exploitation du milieu aquatique sans grand investissement. C'est, par exemple, le cas à la Commune populaire "Libération" (District de Qingpu, Shanghai), qui exploite ainsi le Dianshan Hu et produit annuellement 500 kg de perles.


Un grand merci à Gilbert Cochet, éminent spécialiste de la Moule perlière pour ses envois de clichés photographiques et les corrections apportées à cet article.
Sources :
Cochet G. (2004) La moule perlière et les nayades de France Catiche Productions Ed. 32 p.
Chauveau L. : Les moules perlières jouent les sentinelles (Sciences et Avenir, juin 2009).
Perles de culture en Chine : http://www.fao.org/docrep/005/AD016F/AD016F15.htm
18:56 Publié dans Invertébrés, Limnologie-hydrobiologie, Mollusques | Tags : moule perlière, mollusques, bivalves, eau douce, pollution, bioindicateurs | Lien permanent | Commentaires (19) | ![]() Facebook | | |
Facebook | | |
18/11/2009
L'Escargot (1) : Morphologie externe
L'Escargot, cet animal hermaphrodite, est un excellent modèle pour l'étude de la sexualité et le déterminisme du sexe. En effet, les cellules souches de sa gonade évoluent soit en ovules, soit en spermatozoïdes. Voici toute une série d'articles sur cet animal fabuleux. Ce premier chapitre traite l'étude de la morphologie de l'animal.
10:22 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : sexualité, hermaphrodisme, escargot, mollusques, morphologie | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
17/11/2009
L'Escargot (2) : La coquille
Dans ce deuxième chapitre consacré à l'Escargot, intéressons-nous à la structure de la coquille, à sa régénération en cas de fracture et ses applications en cosmétologie
10:42 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : escargot, coquille, mollusques, gastéropodes | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
16/11/2009
L'Escargot (3) : Locomotion
Entre autres particularités, l'Escargot a un mode de locomotion tout particulier : il se déplace grâce à un unique pied, escaladant n'importe quelle surface et déclivité, et en avançant sans déraper ni rester collé au substrat : tout ça grâce à la thixotropie de son mucus.
18:26 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : sexualité, hermaphrodisme, escargot, mollusques, locomotion | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
15/11/2009
L'escargot (4) : Anatomie
Les Gastéropodes sont vraiment des animaux "tordus". Au cours de leur embryogenèse, ils subissent flexion et torsion, voire enroulement dans une coquille spiralée… Et en plus, un appareil génital à tout faire : spermatozoïdes et ovules.
08:55 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : sexualité, hermaphrodisme, escargot, mollusques, anatomie | Lien permanent | Commentaires (17) | ![]() Facebook | | |
Facebook | | |
14/11/2009
L'escargot (5) : Biologie et développement
Bien qu'ils soient hermaphrodites et et que leur gonade produise les deux sexes gamétiques, il n'y a pas autofécondation chez les escargots. L'accouplement est réciproque avec échanges de spermatophores mis en réserve chez le partenaire, en attente de la maturation des ovocytes.
09:01 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : sexualité, hermaphrodisme, escargot, mollusques, biologie, développement | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
13/11/2009
L'Escargot (6) : L'hermaphrodisme
Étude en microscopie photonique et électronique de la glande hermaphrodite de l'Escargot : les gamètes mâles et femelles sont produits dans chaque tubule de la gonade où l'on trouve simultanément les ovocytes sur la paroi et les gonocytes mâles en évolution dans la lumière des tubules.
14:56 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : sexualité, hermaphrodisme, escargot, mollusques, gamétogenèse | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
12/11/2009
L'Escargot (7) : L'ovotestis adulte
Quelle que soit la lignée gamétique mâle ou femelle, le cycle de la glande hermaphrodite montre que les gamètes naissent des mêmes cellules souches situées sur la paroi des tubules.
09:43 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : sexualité, hermaphrodisme, escargot, mollusques, gamétogenèse | Lien permanent | Commentaires (1) | ![]() Facebook | | |
Facebook | | |
11/11/2009
L'Escargot (8) : la spermatogenèse
Nés de cellules souches pariétales, les gonocytes mâles se multiplient dans la lumière des tubules pour donner finalement des spermatozoïdes. Pendant ce temps, les ovocytes ne se multiplient plus sur la paroi mais prennent de l'embonpoint.
12:04 Publié dans Invertébrés, Mollusques, Sexualité-embryologie | Tags : sexualité, hermaphrodisme, escargot, spermatogenèse | Lien permanent | Commentaires (2) | ![]() Facebook | | |
Facebook | | |
10/11/2009
L'Escargot (9) : l'ovogenèse
Nés de cellules souches pariétales, les ovocytes vont subir un accroissement considérable de leur volume par la constitution de réserves mettant en jeu toute une machinerie cellulaire.
17:19 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : sexualité, hermaphrodisme, escargot, ovogenèse | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
09/11/2009
L'Escargot (10) : genèse de la gonade
La genèse de la gonade permet de confirmer que les gamètes des deux sexes proviennent des mêmes cellules souches présentant une morphologie semblable à celle des cellules somatiques.
14:41 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : sexualité, hermaphrodisme, escargot | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
08/11/2009
L'Escargot (11) : Organes présumés endocrines
La différenciation des gamètes dans le sens mâle ou dans le sens femelle est sans doute due à des interactions hormonales. Il faut donc rechercher des organes endocrines susceptibles d'agir sur la gamétogenèse.
09:46 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : sexualité, hermaphrodisme, escargot, organes endocrines | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
07/11/2009
L'Escargot (12) : culture organotypique de la gonade isolée sur milieu anhormonal
Pour s'affranchir de l'influence de l'organisme sur la gonade, il faut l'isoler sur des milieux de culture dépourvus de toute hormone et de tester ainsi les potentialités intrinsèques des cellules souches à l'origine de la gamétogenèse. On montre ainsi que le sexe fondamental est le sexe femelle qui se manifeste spontanément en l'absence d'hormones : c'est l'autodifférenciation ovocytaire.
09:26 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : sexualité, hermaphrodisme, escargot, culture organotypique | Lien permanent | Commentaires (1) | ![]() Facebook | | |
Facebook | | |
06/11/2009
L'Escargot (13) : culture de la gonade sur milieux enrichis
En culture d'organes sur milieu anhormonal, les gonocytes évoluent spontanément en ovocytes. Pour obtenir des spermatozoïdes, il faut ajouter au milieu de culture du sang d'escargot en phase mâle. Le schéma de la sexualisation des gonocytes est le suivant : pas d'hormones : sexe femelle ; hormones : sexe mâle.
08:39 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : sexualité, hermaphrodisme, escargot, culture organotypique | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
05/11/2009
L'Escargot (14) : association de la gonade avec d'autres organes
L'ajout de sang d'escargot a montré que la spermatogenèse était induite par des facteurs humoraux. Il faut rechercher les organes effecteurs de ces facteurs masculinisants. On les trouvera dans le cerveau et le tentacule oculaire.
10:09 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : escargot, hermaphrodisme, sexualité, culture organotypique | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
04/11/2009
L'Escargot (15) Conclusion générale
 L'Escargot (15) : Interprétation de l'hermaphrodisme chez Helix aspersa
L'Escargot (15) : Interprétation de l'hermaphrodisme chez Helix aspersa
par André Guyard
(suite de l'Escargot 14)
Le présent article constitue une conclusion aux 14 articles précédents consacrés à l'Escargot et au déterminisme du sexe chez cet animal hermaphrodite.
Le comportement de la gonade d'Escargot en culture organotypique autorise à penser que la différenciation sexuelle des gonocytes est sous la dépendance d'une séquence hormonale. La confrontation des résultats de l'analyse du cycle in vivo et de l'étude expérimentale in vitro permet de mieux comprendre certaines modalités de l'expression de l'hermaphrodisme.
1) La culture de l'ébauche gonadique isolée démontre que non seulement chaque cellule-souche morphologiquement identique à une cellule somatique est sexuellement bivalente mais qu'elle est potentiellement une cellule femelle. Chez cette espèce hermaphrodite, le sexe femelle se réalise dans des conditions anhormonales. Il s'agit d'une autodifférenciation femelle.
2) Comment interpréter la protandrie ? Il faut supposer que la phase germinative qui débouche in vivo sur la spermatogenèse est déclenchée par un facteur masculinisant. L'expérimentation nous apprend que ce facteur présumé est humoral. Il est présent dans l'hémolymphe d'animaux en phase mâle et il permet l'accomplissement de la spermatogenèse in vitro. La sécrétion de cet agent est discontinue puisque sa présence dans l'hémolymphe est épisodique.
Le primum movens de l'action androgène siège au niveau du ganglion cérébroïde d'animaux d'âge postembryonnaire puisque cet organe favorise la multiplication spermatogoniale et, conjointement avec le tentacule oculaire, empêche la manifestation de l'autodifférenciation ovocytaire. Un fonctionnement endocrine discontinu du cerveau expliquerait les démarrages de spermatogenèses abortives au cours du premier mois de la vie postembryonnaire.
3) L'apparition des ovocytes un mois après l'éclosion correspondrait à un épuisement corrélatif des hormones masculinisantes cérébrales. La différenciation des protogonies dans le sens femelle coïncide dans un tubule donné avec l'arrêt de la multiplication spermatogoniale. In vitro, c'est l'époque où la seule présence des ganglions cérébroïdes ne permet plus d'assumer le contrôle de la spermatogenèse et de refréner l'autodifférenciation ovocytaire. Le taux de facteur masculinisant serait insuffisant pour imposer le sexe mâle à toute la gonade puisqu'il s'établit une espèce de gradient de sexualité dans la culture. La partie la plus proche du tissu nerveux est occupée par des spermatogonies en multiplication alors que dans la partie la plus éloignée, des gonocytes échappant probablement à l'action du facteur masculinisant s'autodifférencient en ovocytes.
4) Plus tard, au cours du cycle annuel de la gonade mature, le démarrage de la spermatogenèse puis l'apparition des ovocytes sur les parois peuvent s'expliquer de la même façon par l'intervention puis l'épuisement du facteur androgène. Or, chez les Crustacés, le cerveau qui contrôle le fonctionnement de la glande androgène a lui-même le même effet directement sur les gonocytes (J. Berreur-Bonnenfant, 1968). L'association in vitro des ganglions cérébroïdes d'animaux en spermatogenèse avec la gonade ne permet jamais la réalisation d'une spermatogenèse comparable à celle réalisée par l'adjonction d'hémolymphe d'hiver. Peut-être que cette expérience ne met en évidence que la stimuline contrôlant le fonctionnement d'un hypothétique tissu androgène.
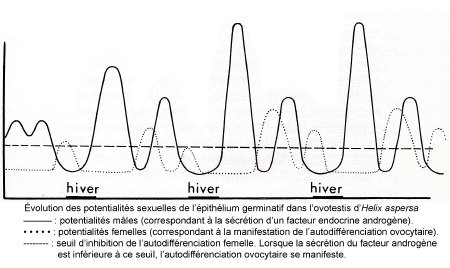
5) En outre, après accomplissement de la spermatogenèse, la lignée femelle poursuit son évolution. Or in vitro, le cerveau extirpé d'animaux en ovogenèse ne permet que la seule manifestation de la lignée femelle. C'est une nouvelle preuve de la labilité du facteur cérébral masculinisant. En sa présence en un taux suffisant, la lignée mâle entre en multiplications spermatogoniale ; en son absence ou en sa présence en quantité insuffisante, la lignée femelle se manifeste et amorce son auxocytose.
6) On peut se demander quel est le mécanisme responsable du déclenchement et de la modulation de la sécrétion de ce facteur masculinisant. D'une façon générale, il est certain que le système nerveux intervenant aussi bien dans le contrôle de la vie de nutrition et de reproduction que dans la vie de relation de l'organisme, la sécrétion des neurohormones est sousmise à l'influence des facteurs exogènes trophiques, climatiques ou psychiques, les récepteurs sensoriels (notamment le tentacule oculaire des Gastéropodes) pouvant jouer le rôle de relais. Ces considérations expliqueraient l'intervention des facteurs externes dans l'expression du phénotype cytosexuel chez les espèces hermaphrodites.
On peut également envisager que le signal du virage sexuel au niveau du cerveau provienne de l'ovotestis lui-même qui, par une sorte de feed-back déclenché par exemple par l'état de réplétion des tubules gonadiques dû à l'abondance des spermatogonies, avertisse le système nerveux central par voie humorale.
7) La participation d'autres facteurs humoraux contrôlant la physiologie de l'une ou l'autre des gamétogenèses doit être supposée pour expliquer la coexistence des deux lignées gamétiques.
Ainsi, pendant que se déroule la spermiogenèse in vivo ou en culture en présence d'hémolymphe d'hiver, l'accroissement ovocytaire est réprimé. C'est alors qu'on peut supposer l'intervention d'une inhibition de l'ovogenèse parallèlement à l'action d'un facteur spermiogénétique d'origine inconnue. Le fait que le tentacule montre un rôle constamment répressif sur l'ovogenèse est un indice en faveur de l'intervention de cet organe dans l'inhibition de l'accroissement ovocytaire.
D'autre part, un facteur cérébral semble, contrôler l'auxocytose. En culture, le ganglion cérébroïde prélevé sur des animaux en ovogenèse a une influence bénéfique sur l'accroissement ovocytaire sans qu'on puisse préjuger d'un rôle sur la vitellogenèse.
On peut soupçonner l'intervention de multiples facteurs dont les interactions constituent un jeu subtil permettant l'évolution en parallèle des deux lignées sexuelles ; ainsi la préméiose au sein des ovocytes débute fréquemment en même temps que s'amorcent les divisions réductionnelles des spermatocytes. Peut-être y a-t-il là une indication de l'intervention d'un facteur méiotique non sexualisé ?
Le schéma de la sexualisation des cellules germinales au sein de la gonade paraît plus simple. Les protogonies ou gonies indifférenciées sont sexuellement bivalentes. Elles reçoivent de la part du soma l'impulsion qui les orientera vers un sexe ou vers l'autre. C'est la nature et le cheminement de cette impulsion qui sont en cause.
Chez Helix aspersa, la culture organotypique a permis de mettre en évidence le phénomène d'autodifférenciation femelle.
Le schéma de la séquence hormonale qui contrôle la différenciation dans le sens mâle, évoqué par les résultats de l'association de la gonade avec le ganglion cérébroïde demande à être confirmé. S'agit-il de facteurs qualitativement distincts ou simplement de la modulation d'un unique facteur stimulateur de la gamétogenèse ?
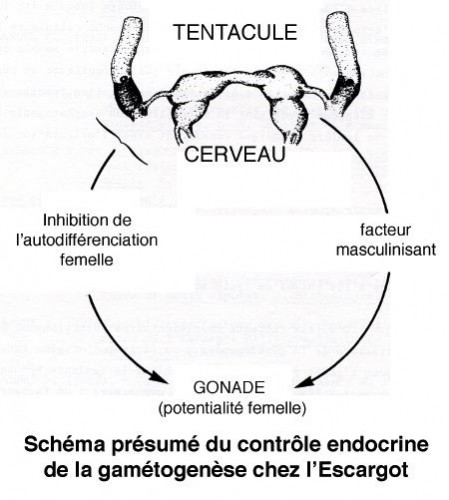
Il ne faut pas perdre de vue que ces résultats ont été obtenus avec la seule technique des cultures organotypiques. La mise en évidence d'actions endocrines ne pourra être résolue qu'avec le concours d'expériences complémentaires. Injections d'extrait cérébral et/ou tentaculaire, ablation sélective de cellules nerveuses, greffes ou implantations de ganglions, observation de la différenciation fine au niveau des organites des cellules germinales, identification chimique des substances actives constituent autant de techniques à exploiter pour poursuivre la discussion sur le contrôle de l'hermaphrodisme chez l'Escargot.
RÉSUMÉ
Helix aspersa Müll. est une espèce d'Hélicidés hermaphrodite protandre. L'étude histologique et ultrastructurale complétée par la mise en culture organotypique de la gonade a permis d'apporter quelques précisions quant aux mécanismes qui régissent la sexualisation des gonocytes.
La mise en place de la gonade est caractérisée par une période d'indifférenciation qui se prolonge jusqu'à dix jours après l'éclosion. Il n'existe qu'une seule souche cellulaire à l'origine des deux lignées germinales.
La protandrie semble due à une induction mâle d'origine cérébrale qui se manifeste en réprimant une tendance spontanée à l'autodifférenciation femelle et par un effet mitogène favorisant la multiplication spermatogoniale qui envahit la lumière gonadique consacrant ainsi l'orientation définitive du gonocyte dans le sens mâle.
Un mois après l'éclosion, l'hermaphrodisme se manifeste par la différenciation d'ovocytes en position pariétale. Ce phénomène réalité de l'autodifférenciation ovocytaire non refrénée par le cerveau dont l'action modulée selon l'âge ou la saison déterminera les phases du cycle sexuel.
D'autres facteurs complémentaires interviennent dans la réalisation de la gamétogenèse : un facteur d'origine tentaculaire dont l'effet principal est d'inhiber la tendance spontanée des gonocytes à l'autodifférenciation ovocytaire ; un facteur dont le siège est le ganglion cérébroïde qui favorise l'accroissement de la cellule femelle avec le concours de facteurs trophiques.
09:59 Publié dans Biologie, Invertébrés, Mollusques, Sexualité-embryologie | Tags : escargot, sexualité, hermaphrodisme | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |


