Césaire et Marie PHISALIX :
deux savants comtois
spécialistes des venins et des serpents
par Claude-Roland Marchand
Professeur des Universités
Membre correspondant de l'Académie des Sciences,
Belles Lettres et Arts de Besançon.
En 2006, la commune de Mouthier-Hautepierre et la Société Herpétologique de France ont honoré la mémoire de Césaire PHISALIX, pour le centenaire de sa mort. Cet enfant du pays s’est illustré, au cours d’une riche et brillante carrière, dans plusieurs domaines de la biologie et de la physiologie ; mais son nom reste surtout attaché à la mise au point d’un sérum antivenimeux. Malgré l’importance de cette découverte, Césaire PHISALIX nous semble injustement tombé dans l’oubli.
Mouthier-Hautepierre a associé à cet hommage, son épouse et collaboratrice, Marie PICOT-PHISALIX, disciple talentueuse qui a prolongé l’œuvre de son époux, pendant trente neuf ans au Muséum d’Histoire Naturelle de Paris.
La ville de Besançon a baptisé une rue de la capitale comtoise du nom de PHISALIX.

Cliché C.R. Marchand
Je voudrais retracer, ici, les principales étapes de leurs vies et les importantes retombées de leurs recherches en m’aidant des nombreux témoignages rassemblés dans différentes revues dont on trouvera les références dans la bilbiographie ci-dessous.
Auguste-Césaire PHISALIX (1852-1906)
Est né le 8 octobre 1852 à Mouthier-Hautepierre (Doubs) dans une modeste famille de vignerons ; c’est un élève brillant qui entame sa scolarité, auprès de son instituteur à Lods, puis au petit Séminaire d’Ornans ; il la poursuit au Collège catholique de Besançon où il obtient ses baccalauréats (en 1872, 1873). Pour alléger les sacrifices consentis par sa famille, il s’engage comme élève au Service de Santé Militaire. En 1877, au Val de Grâce, il termine ses études médicales par la soutenance d’une thèse sur « La néphrite interstitielle ». Parmi ses maîtres se trouve Alphonse LAVERAN, qui découvrira l’Hématozoaire du paludisme (Prix Nobel 1907), et parmi ses camarades il y a Émile ROUX qui fera, comme on sait, une brillante carrière à l’Institut Pasteur (mise au point du sérum anti-diphtérique).
Césaire PHISALIX va occuper différents postes au Val de Grâce, puis revient à Besançon avec le grade de médecin aide-major au 4ème Régiment d’Infanterie.
En 1881, il participe à la campagne de Tunisie, où il tombe gravement malade ; rapatrié il entame sa convalescence à Roscoff où il va assouvir sa passion de naturaliste. C’est là qu’il réunit du matériel qui lui servira à soutenir sa thèse de sciences après l’obtention de sa licence de sciences naturelles en 1882. Sa thèse de doctorat ès sciences est soutenue en 1884 ; elle s’intitule : « L’anatomie et la physiologie de la rate chez les Ichthyopsidés* ». Sa santé ne s’améliorant pas il sera mis à la retraite de l’Armée active à 35 ans, en 1887.
(* Ce sont des Poissons).
En 1884, il est nommé préparateur à la Faculté des sciences de Besançon, puis professeur suppléant de zoologie médicale à l’École de Médecine et de Pharmacie en 1886. Deux ans plus tard il est nommé Chef de travaux de zoologie à la Faculté des sciences de Besançon. Cette même année, à l’âge de 35 ans, sur proposition du Professeur CHAUVEAU (Directeur de l’École vétérinaire de Lyon), il entre au Muséum d’Histoire Naturelle de Paris, en tant qu’Aide-naturaliste ; puis il est promu Assistant en 1892. C’est pendant ce séjour de 18 ans au Muséum, jusqu’à sa mort en 1906, que Césaire PHISALIX fera ses découvertes majeures sur les venins et la sérothérapie.
Plus de 200 articles, publiés dans des revues scientifiques renommées, présentent les résultats de ses essais, de ses protocoles et des applications possibles de ses découvertes.
Malheureusement, sur le même sujet et avec des conclusions similaires, à son corps défendant, il entrera en compétition avec le Dr Albert CALMETTE dont le nom est le seul à être associé à la mise au point des sérums antivenimeux.
Marie-Émilie PICOT-PHISALIX (1861-1946)

Elle est née le 20 novembre 1861 à Besançon (150e anniversaire). Elle est la fille de Camille-Joseph PICOT originaire de Gap (Hautes Alpes) et de Marie-Joséphine DALLOZ née à Saint-Claude (Jura). En 1863 sa maman décède. Son papa élèvera alors seul sa petite famille. Grâce à un milieu aisé elle bénéficie d’une bonne éducation, entre à l’École Normale Supérieure des Jeunes filles de Sèvres en 1882, dans la deuxième promotion de cette école ; elle obtient, et c’est nouveau pour une fille à l’époque, l’agrégation de sciences en 1888.
Marie PICOT a enseigné dans plusieurs établissements : à Besançon, Bourg-en-Bresse, Cambrai. Et c’est à Besançon, qu’elle reprend des études de médecine. En 1895 Marie PICOT épouse Césaire PHISALIX qu’elle avait connu lors d’un stage à la station de Roscoff.
Cette même année, Marie PICOT-PHISALIX quitte l’enseignement et rejoint, au Muséum d’Histoire Naturelle, son mari avec qui elle va travailler, d’abord à une thèse de médecine et ensuite à des recherches approfondies sur les venins, les appareils venimeux dans le règne animal.
En 1900 elle soutient à Paris une thèse de Médecine intitulée : « Recherches histologiques, embryologiques et physiologiques sur les glandes à venin de la salamandre terrestre ». Pour les grandes qualités de ce travail, certes un peu éloigné du domaine médical, elle reçoit la médaille d’argent de la Faculté de Paris ; elle rejoint alors le groupe des premières femmes françaises titrées du grade de docteur en médecine.
De 1900 à 1906, elle travaille auprès de son mari, et l’entoure de ses soins attentifs dans les dernières années de sa vie.
En 1910, elle entre au Laboratoire d’Herpétologie du Muséum d’Histoire Naturelle de Paris où elle travaillera jusqu’à sa mort en 1946, en qualité d’Attachée bénévole. En 2011 son bureau existe toujours dans le pavillon d’Herpétologie.
Nous voulons, ici, en 2011, rendre hommage à « ces deux savants du pays de Courbet », l’année même où est inauguré le Musée du peintre d’Ornans, qui n’a pas pu, évidemment, connaître ses illustres voisins de la vallée de la Loue.
La CARRIÈRE SCIENTIFIQUE de Césaire PHISALIX
Docteur en médecine et docteur ès Sciences naturelles, Césaire PHISALIX s’est intéressé à de nombreux sujets, avec curiosité, rigueur et efficacité.
Son collègue de la Faculté de Médecine de Paris, le Dr DESGREZ, a décrit, quatre ans après sa mort, la puissance de travail et l’opiniâtreté de ce chercheur enthousiasmé aussi bien par l’embryologie et l’anatomie humaines, que par la physiologie, la pathologie générale et la bactériologie.
En effet, ce qui force l’admiration chez Césaire PHISALIX, c’est son total engagement dans chaque sujet abordé, que les circonstances ou ses maîtres lui proposent. Nous nous attarderons sur les venins et la sérothérapie, sans passer sous silence la pertinence de ses observations sur le cerveau de l’embryon humain (que Sigmund FREUD citera dans un de ses articles), la cyclopie, les chromatophores des Mollusques Céphalopodes, la rate des Vertébrés inférieurs (son sujet de thèse), et les glandes venimeuses des Amphibiens. Il a isolé la bufoténine du Crapaud, mais aussi une quinone des Myriapodes Diplopodes. On reste surpris par la dispersion de ses centres d’intérêt, mais ce qui va l’occuper la majeure partie de sa carrière c’est le problème des venins et le traitement de l’envenimation.
Pour comprendre l’origine de son intuition géniale concernant l’obtention d’un sérum neutralisant les venins, il nous paraît important de rappeler les premiers travaux de microbiologie qu’il a effectués sous la conduite du Professeur Auguste CHAUVEAU (1827-1917 ; titulaire de la Chaire de Pathologie comparée qui a mis au point le vaccin contre le charbon) et qui ont trait à la maladie charbonneuse. En effet, à l’instar de nombreux chercheurs, il atténue la virulence du Bacille par la chaleur. Mentionnons par exemple, dans cette période féconde en découvertes, les nombreux travaux convergents des années 1880-1890 : ceux de TOUSSAINT sur le charbon en 1880, de FERRAN* en 1884 et de GAMALEÏA sur le choléra en 1888, ceux de PASTEUR sur la rage en 1885, ceux de ROUX et YERSIN sur la diphtérie en 1888, BEHRING et KITASATO en 1890 sur la diphtérie et le tétanos, et de BABES et LEPP en 1889 sur la rage. C’est une période de recherches animées et parfois conflictuelles procédant d’un même principe : affaiblir un microbe, pour vacciner un animal, et utiliser le sérum de son sang qui a acquis la capacité de neutraliser les toxines microbiennes.
* Jaime FERRAN, prix Bréant 1907, aurait même la priorité sur PASTEUR, puisqu’il a vacciné, en Espagne, 4700 personnes contre le choléra en 1885.
Dès 1889, PHISALIX concentre ses recherches sur les venins, qu’il avait déjà abordés avec la Salamandre et le Crapaud, et qu’il élargit aux Serpents. Il reconnaîtra plus tard comment lui est venue l’idée, auprès de son maître A. CHAUVEAU, d’une analogie entre « les sécrétions cellulaires toxiques et les sécrétions microbiennes… et que les procédés d’atténuation et de vaccination applicables aux unes le sont aussi aux autres. »
Ce paradigme, pourrait-on dire, se confirmera au fil des essais et des ajustements expérimentaux qu’il conduira avec la collaboration d’un jeune pharmacien, Gabriel BERTRAND, dont le nom restera attaché à ses découvertes majeures.
GENÈSE d’une DÉCOUVERTE HISTORIQUE
De tous temps la médecine traditionnelle a proposé différents remèdes contre l’envenimation ; citons parmi les plus anciennes la Thériaque d’Andromachus (cf le texte de Moyse CHARAS 1668), utilisées pendant 17 siècles, ou d’improbables préparations « magiques » à base de plantes, d’insectes, d’extraits divers et variés… souvent inefficaces et à tout le moins dangereux sur des patients en état de choc.
L’accoutumance des montreurs et des chasseurs de serpents, était attribuée à des petites morsures répétées, où de faibles quantités de venin agissaient un peu comme un vaccin (Marie PHISALIX, mordue à plusieurs reprises pourrait en être le plus bel exemple !).
Dans ses travaux de 1886-1888, KAUFMANN signalait déjà l’accoutumance qu’il obtenait chez le chien par des injections répétées de petites quantités de venin entier ou de venin vieilli (travail couronné par l’Académie de Médecine). Mais nous trouvons également dans la littérature du XVIIIe siècle, sous la plume de FONTANA (1780) des essais d’accoutumance par injections de petites quantités de venin. C’est à partir de 1892 que, de son côté déjà, Albert CALMETTE parvient à détruire la « virulence » du venin de Cobra par la chaleur ; mais il reconnaît avoir cherché, en vain, à obtenir l’immunité totale chez les animaux expérimentés . L’ensemble de toutes ces observations sur les venins, l’envenimation et l’accoutumance, sont prises en compte par Césaire PHISALIX qui, à partir de 1892, s’emploie à les utiliser dans des protocoles méthodiques savamment répétés et contrôlés.
Matériels et méthodes utilisés par PHISALIX et BERTRAND
PHISALIX et BERTRAND ont utilisé le venin de Vipera aspis, récoltée dans le Centre de la France et en Franche-Comté (CALMETTE, on l’a dit plus haut, travaillait sur le Cobra mais il a réalisé quelques essais avec des Vipères récoltées autour d’Arbois ). Dans un premier temps ils ont établi que la dose mortelle minima pour un Cobaye de 500 g était de 0,3 mg de venin sec.
Puis ils testent l’effet de températures de plus en plus élevées sur l’atténuation du venin ; ils établissent finalement que c’est un chauffage de 15 mn à 80° qui est le plus efficace. Leurs différents essais les amènent à conclure que la chaleur met en évidence trois substances dans le venin : un composé toxique à effet local : l’ échidnase, un composé qui détermine les effets généraux mortels : l’échidno-toxine et ce qui est obtenu après un chauffage de 15 mn à 80° : l’échidno-vaccin. Cette observation est fondamentale pour l’établissement du protocole rigoureux et reproductible que nos deux chercheurs vont proposer dans leurs publications historiques de 1894.
Le protocole de 1893-1894
In : Comptes Rendus de l’Académie des Sciences vol. 118, 5 février 1894, pp 288-291. C’est le treizième article de PHISALIX sur les venins ; il s’intitule : « Atténuation du venin de vipère par la chaleur et vaccination du cobaye contre ce venin. » note présentée par M. A. Chauveau.
PHISALIX et BERTRAND réalisent une vaccination le 11 janvier sur un cobaye mâle de 510 g, avec 0,3 mg de venin de vipère chauffé à 75° pendant 5 min : l’animal est un peu nauséeux, sans symptôme local. Le 13 janvier inoculation de 0,3 mg de venin entier : quelques nausées, pas de gonflement local, vivacité normale. Le 14 janvier pas d’œdème. Encore vivant le 5 février.
Un résultat identique est obtenu avec 0,6 mg de venin.
Conclusion des auteurs : « Le venin chauffé acquiert des propriétés vaccinantes, soit parce que la chaleur respecte des substances douées de ces propriétés, soit parce qu’elle en fait naître aux dépens de matières toxiques… »
« … Disons toutefois, dès maintenant, qu’il se produit dans le sang des animaux vaccinés des modifications importantes, analogues à celles que l’on a découvertes pour le tétanos ».
Cette communication est suivie le 10 février 1894 par un article complémentaire et fondamental, qui démontre que le sang des animaux vaccinés a des propriétés antitoxiques.
In : Comptes Rendus de la Société de Biologie vol. 46, pp. 111-113. Il s’intitule : « Sur la propriété antitoxique du sang des animaux vaccinés contre le venin de vipère. »
PHISALIX et BERTRAND vaccinent deux cobayes le 21 janvier et les sacrifient le 24 en prélevant leur sang (Notons que ce délai est très court quand on sait que le maximum d’IgG (imunoglobulines G est produit plusieurs semaines après la première injection. Il semblerait que les IgM rapidement produites auraient leur importance ). Ce sang est défibriné, mélangé à la dose de 15 cc avec 0,3 mg de venin sec. Ce mélange est ensuite injecté à un Cobaye qui fait un oedème 2 heures après. Le 10 février l’animal est bien portant. Même résultat avec 0,5 mg dans 12 cc du sang de l’animal vacciné. Confirmation des résultats avec 3 cc de sang mélangé à 0,3 mg de venin.
Conclusion des auteurs :
« Nous espérons obtenir des modifications du sang suffisamment intenses pour qu’il puisse être utilisé comme agent curatif. »
Il nous semble qu’un grand pas est alors franchi dans le traitement des envenimations : le sérum antivenimeux est inventé. Mais une publication contemporaine d’Albert CALMETTE va perturber les retombées de la découverte de PHISALIX et BERTRAND.
Les travaux d’Albert CALMETTE (1863-1933)
Élève de l’École de Médecine navale de Brest, il entre au Service de Santé de la Marine, obtient sa thèse en 1885 et effectue de nombreuses missions en Afrique, St Pierre et Miquelon et en Asie. Dès 1891 Louis PASTEUR le désigne pour fonder une filiale de l’Institut Pasteur à Saïgon ; c’est là qu’il supervise la production de vaccins contre la variole et contre la rage et conduit des recherches sur le choléra, la dysenterie, les fermentations et les venins de serpents.
Placé hors cadre du Corps de Santé des colonies, en 1894, il consacre tout son temps à la préparation d’un sérum antipesteux (avec BORREL et YERSIN) et surtout d’un sérum antivenimeux contre le venin de Cobra. Tout comme CHAUVEAU et PHISALIX il croyait à une analogie entre les composants toxiques du venin et les toxines bactériennes. La chaleur, selon lui, ne modifiant pas le venin de Cobra, il y parvient à l’aide d’hyposulfites alcalins.
En 1892, il publie ses premiers essais d’immunisation sur les Poules ; mais c’est en 1894, le même jour que PHISALIX et BERTRAND, à la Société de Biologie, mais plus tard dans la journée (!), qu’il présente un travail intitulé : « L’immunisation artificielle des animaux contre le venin des serpents et la thérapeutique expérimentale des morsures venimeuses. » Il conclut en affirmant que son protocole effectué sur l’animal pourrait être appliqué à l’Homme.
Notons que dans le traitement de la morsure, il accordait autant d’importance à l’injection locale d’hypochlorite (eau de Javel) qu’au sérum lui-même. Il finira par ne plus préconiser l’injection d’hypochlorite dont PHISALIX et BERTRAND démontrent l’inefficacité en 1895, sans jamais reconnaître explicitement son erreur. De même il mit beaucoup de temps à reconnaître la spécificité des sérums antivenimeux et pensait que son antisérum préparé avec le venin de cobra était efficace contre toutes les envenimations ophidiennes. Pourtant PHISALIX et BERTRAND (1895) notaient que : « le venin des serpents diffère non seulement d’une espèce à l’autre, mais aussi chez la même espèce », en fonction, en particulier, de la saison et du lieu de récolte.
C’est le professeur Max GOYFFON, du Muséum d’Histoire Naturelle, qui résume le mieux en 2009, les tenants et les aboutissants de la querelle de priorité qui oppose pour longtemps les deux découvreurs.
Je le cite :
« Dans une note présentée quelques semaines plus tard, le 27 mars 1894, CALMETTE fait valoir l’action tout à la fois préventive, antitoxique et thérapeutique du sérum antivenimeux qu’il prépare, sans citer le travail antérieur de PHISALIX et BERTRAND. Ceux-ci répliquent aussitôt le mois suivant dans une note où ils rappellent leur antériorité, car ils pensent que des conséquences théoriques et pratiques importantes découleront des faits qu’ils ont établis. »
L’Académie des Sciences donnera raison d’abord à PHISALIX et BERTRAND en leur attribuant le prix MONTHYON en 1894 « pour la découverte d’un sérum antivenimeux », puis à PHISALIX seul avec le prix BRÉANT en 1898 pour « la découverte des sérums antivenimeux. »
La querelle durera longtemps et c’est le nom de CALMETTE que l’Histoire retiendra ; à cela il y a plusieurs raisons :
1 – la rivalité évidente qu’il y avait entre le Muséum et l’Institut Pasteur ;
2 – le mauvais état de santé de Césaire PHISALIX qui ne se déplace plus guère, alors que CALMETTE voyage et présente ses résultats dans le monde entier ;
3 – la stratégie efficace de CALMETTE qui dès 1895, à l’Institut Pasteur de Lille, s’attache à préparer des grandes quantités de sérum antivenimeux contre le venin de Cobra, avec lequel il obtient des guérisons humaines : en 1895 il applique avec succès la première sérothérapie antivenimeuse à un Vietnamien ; pratique que n’a pas pu réaliser PHISALIX, qui n’avait pas accès aux malades.
4 – une certaine « ingratitude » du Pastorien vis à vis de son confrère du Muséum, à laquelle s’ajoute le recrutement de BERTRAND par l’Institut Pasteur en 1900.
Avec le recul, nous sommes en mesure de dire qu’il y a manifestement une différence de tempérament entre les deux découvreurs : PHISALIX est prudent, modeste et élargit ses recherches, jusqu’à sa mort, pour découvrir d’autres antidotes. « À l’opposé, CALMETTE met toute son énergie à faire reconnaître l’intérêt de sa découverte… il vise avant tout l’efficacité… Élève et admirateur de ROUX autant que de PASTEUR, sa foi, son pouvoir de conviction et un dynamisme hors du commun balaieront aisément des approximations et des échecs en fin de compte mineurs, et réussiront à imposer ses opinions et ses résultats. » nous dit Max GOYFFON. Qui conclut : « CALMETTE sera prophète en dehors de son pays comme en son pays… ».
Nous laisserons, à propos de cette querelle, le dernier mot à Édouard R. BRYGOO (1985) qui a travaillé à l’Institut Pasteur et au Muséum d’Histoire Naturelle, je cite : « Même s’il ne s’en fallait que de très peu, PHISALIX et BERTRAND étaient gagnants aussi bien à la Société de Biologie qu’à l’Académie des Sciences, tandis que CALMETTE ne se montrait vraiment pas beau joueur. »
Nous ne pouvons pas quitter Césaire PHISALIX sans mentionner les nombreux travaux qu’il a consacrés à l’immunité naturelle de certains animaux (Mammifères ou Serpents) pouvant laisser espérer découvrir une propriété particulière transposable à l’espèce humaine. D’autres pistes ont été explorées par lui, alors qu’il cherchait des molécules naturelles susceptibles de traiter l’envenimation.
Césaire PHISALIX a été élu Officier de l’Instruction publique en 1899, Officier de l’Ordre du Lion et Soleil de Perse en 1903.
Il a été nommé chevalier de la Légion d’Honneur en 1900.
L’école et une place de Mouthier-Hautepierre ainsi qu’une petite rue de Besançon portent son nom.
Il n’a pas été membre de notre Académie.
Évoquons la carrière scientifique de Marie PICOT-PHISALIX
Elle a publié seule ou en collaboration plus de 270 articles, de vulgarisation ou très spécialisés. Deux ouvrages majeurs sont attachés à son nom : « Animaux venimeux et venins » en 1922 et « Vipères de France » en 1940. On peut y apprécier d’une part ses descriptions anatomiques, physiologiques précises et d’autre part ses talents d’artiste. Les deux volumes de 1922 comptent plus de 1400 pages, 521 figures, 9 planches en noir et blanc, 8 planches en couleurs et une impressionnante bibliographie. Marie PHISALIX observe soit des animaux qu’elle a récoltés elle-même (salamandres ou vipères), soit des spécimens qu’on lui envoie par voie postale dans des boîtes à bonbons (!).

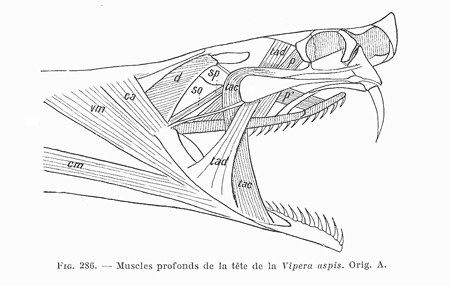
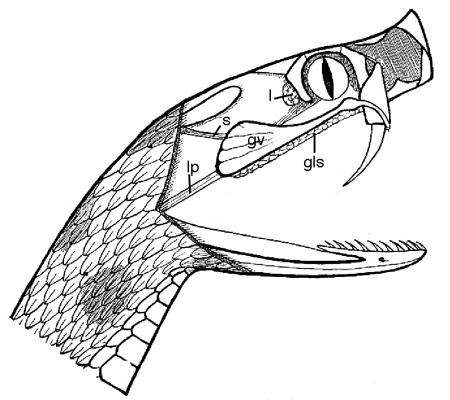



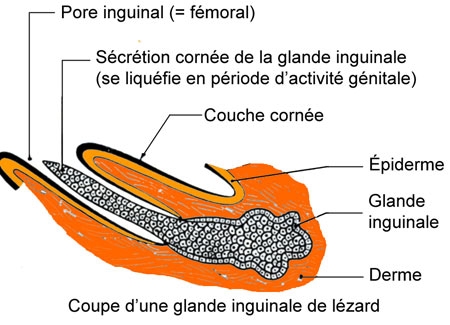
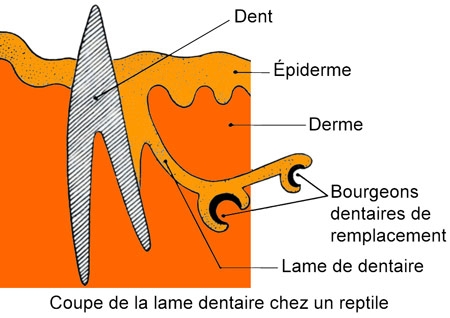
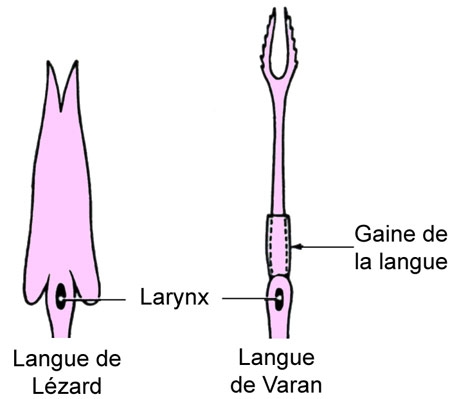
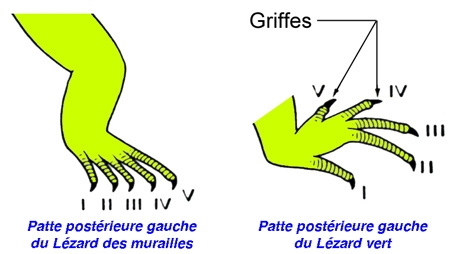
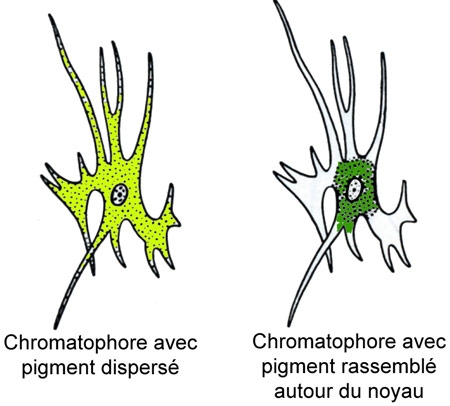
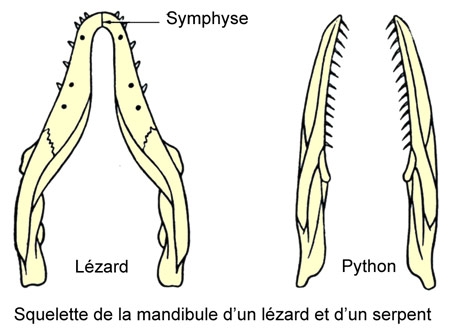
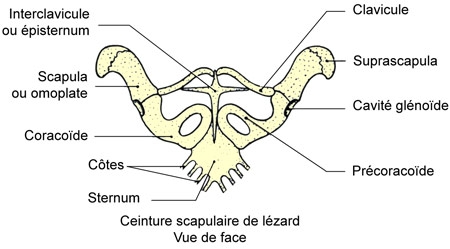
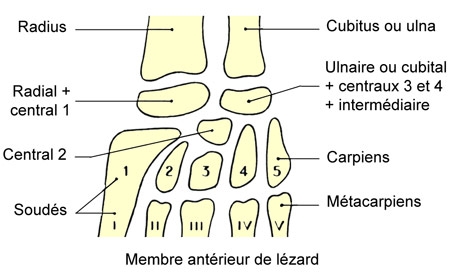
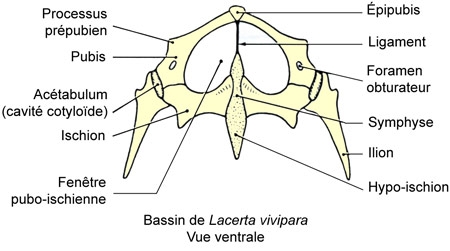
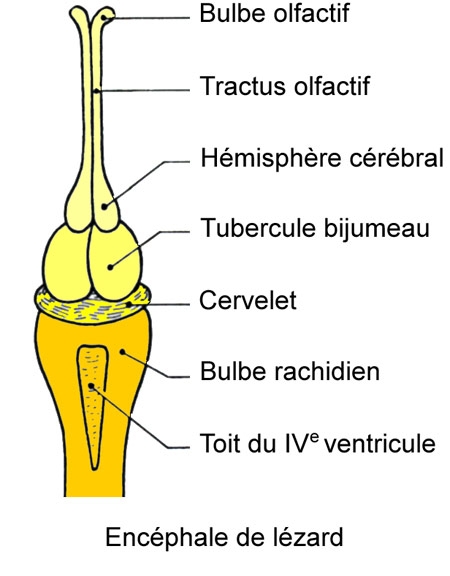
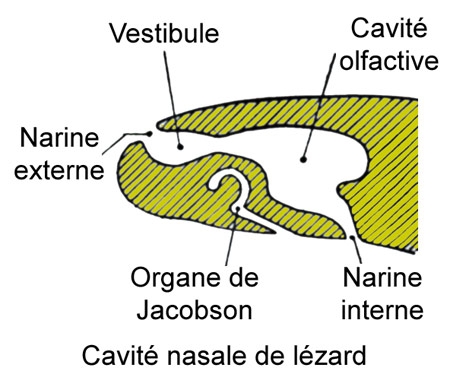
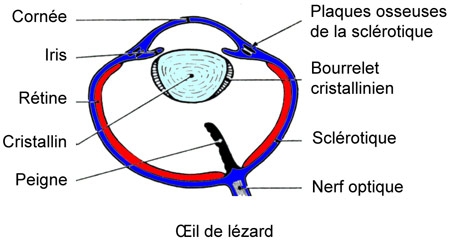
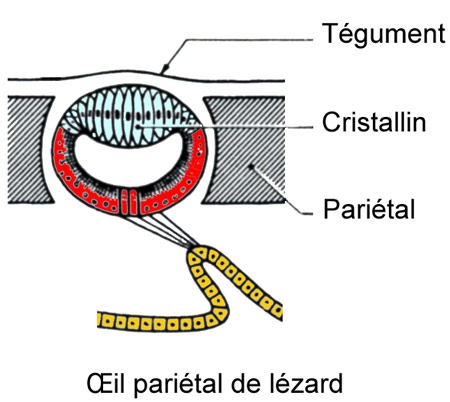
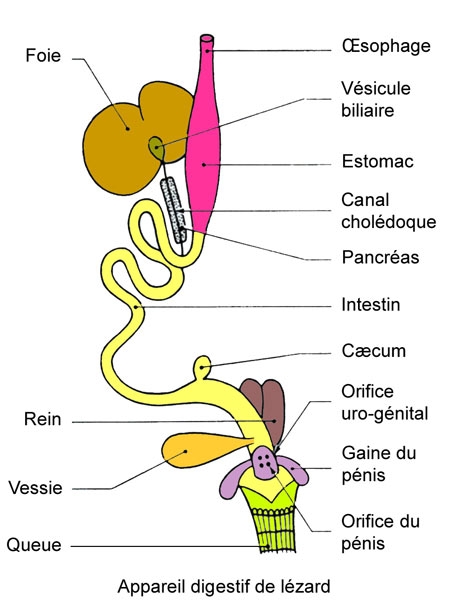
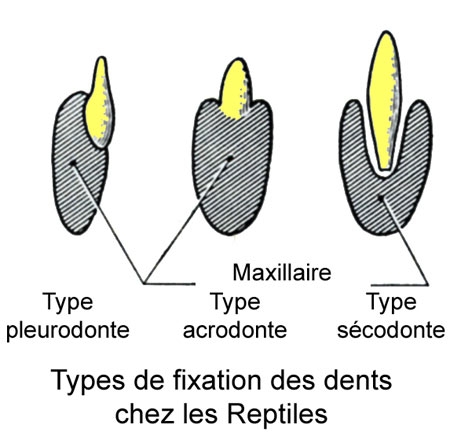
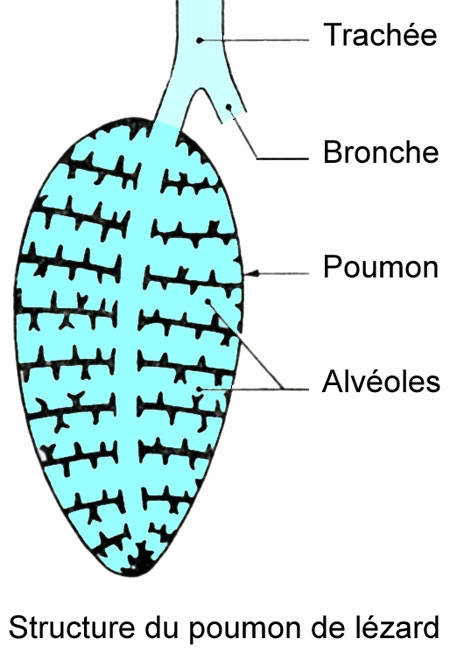
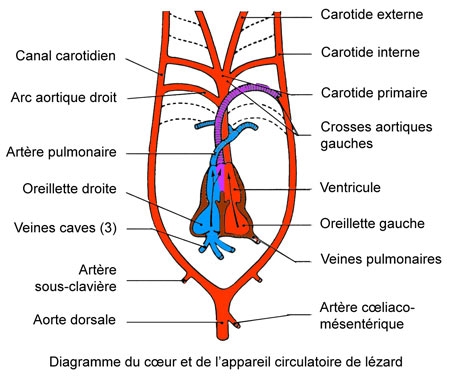
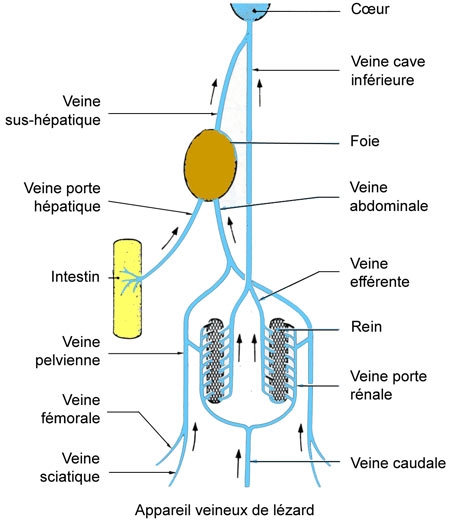
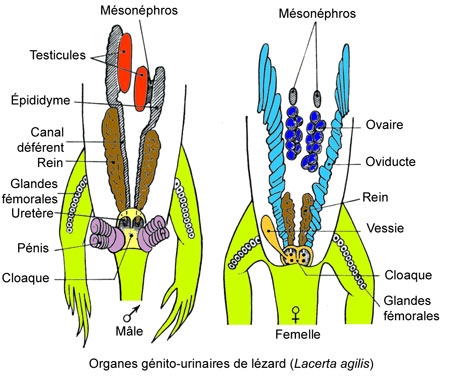
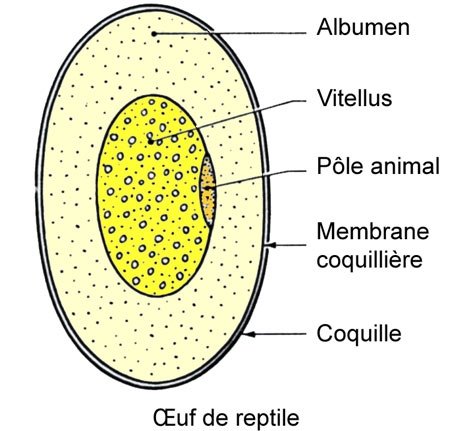
Cinq schémas extraits de « Animaux et venins » 1922
La manipulation des vipères ou du redoutable Heloderma lui vaudra plusieurs morsures, dont une à l’âge de 80 ans qu’elle supporte sans dommages (l’Histoire ne dit pas si elle a utilisé le sérum antivenimeux inventé par son mari). Une anecdote rapportée par F. ANGEL, son aide de laboratoire, illustre le « pragmatisme » de Marie PHISALIX. Citation : « Au moment des plus dures restrictions alimentaires imposés aux Parisiens par l’occupation allemande, au cours des années 1941-1944, nous avons vu bien souvent Mme le Dr Marie Phisalix … emporter chez elle dans un petit récipient les œufs non embryonnés des nombreuses femelles de vipères qu’elle gardait en captivité et qui, dans la journée, avaient été sacrifiées pour servir à ses expériences et à ses études. Ces animaux étaient disséqués, les œufs prélevés soigneusement dans le corps pour servir, disait-elle, « à faire son omelette du soir »… elle ajoutait, en riant : « je prélève également la graisse des mêmes animaux pour remplacer les autres matières grasses absentes ! »…. Par contre elle était navrée de voir sa domestique refuser énergiquement cette nourriture… Ce mode particulier d’alimentation souvent répété, n’altéra jamais sa santé… Il apportait une preuve nouvelle à ses opinions concernant la destruction, par la cuisson, du venin produit par les glandes et le sang des espèces dangereuses. »
Sa filleule, Marie-Louise BOURGEOIS, évoque un souvenir ému de sa marraine, avec qui en 1919, elle chassait les Salamandres à Mouthier-Hautepierre, la lanterne à la main. Même en vacances elle se faisait livrer des vipères du Morvan et « elle les disséquait, surtout la tête. Ensuite elle tannait les peaux pour s’en faire des ceintures et des garnitures. »
Nous avons pu observer, conservés dans le formol ou dans l’alcool de nombreux spécimens entiers préparés et étiquetés par Marie PHISALIX : salamandres, couleuvres, vipères, héloderme, mais également des crânes finement disséqués de vipéridés ou de crotale.
Le Dr Ivan INEICH, actuel curateur des collections du Muséum National d’Histoire Naturelle, à qui nous devons les clichés que nous projetons, nous a autorisé à les regarder de très près et constaté leur bon état de conservation. Nous pouvons faire de même dans le petit Musée Marie Phisalix de Mouthier-Hautepierre, que Christophe CUPILLARD entretient et fait visiter à la demande. Quelques spécimens de couleuvres et de vipères cédés en 1927 par « Mme le Docteur Phisalix » ont été également signalés dans les collections du Musée de la Citadelle et de la Faculté des Sciences de Besançon.
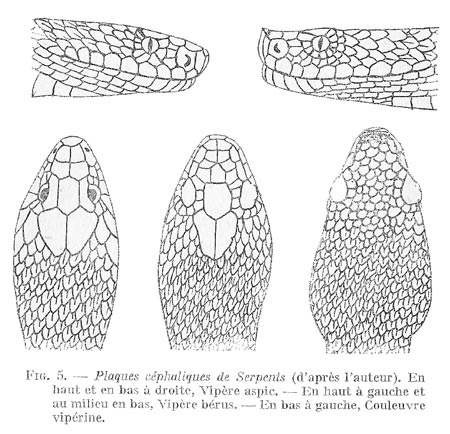
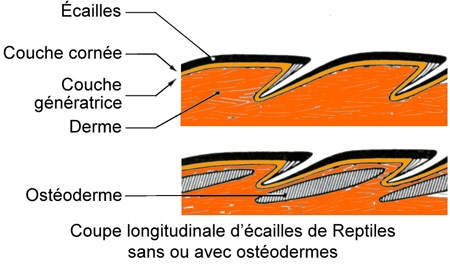
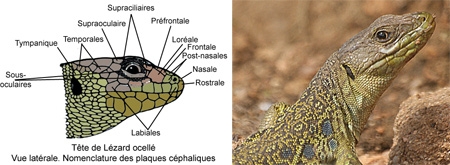
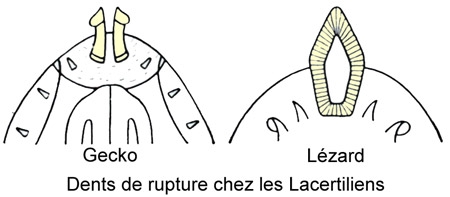
Schéma extrait de « Vipères de France » 1940
Outre ses propres travaux, cette « grande prêtresse des animaux venimeux », a apporté son concours à la relecture, à la finalisation de « La vie des Reptiles de la France centrale », 343 pages écrites et documentées par son ami Raymond Rollinat, décédé au moment où il achevait le manuscrit. Parmi ses disciples signalons notre compatriote naturaliste Charles DOMERGUE (décédé en 2008) qui lui a dédié une espèce de Colubridé découverte à Madagascar et qu’il a nommé Phisalixella.

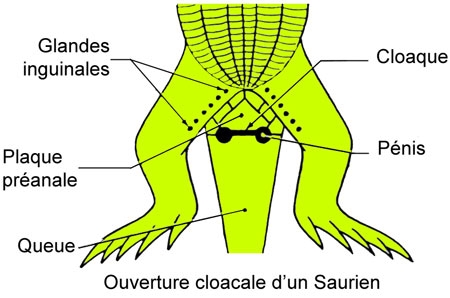
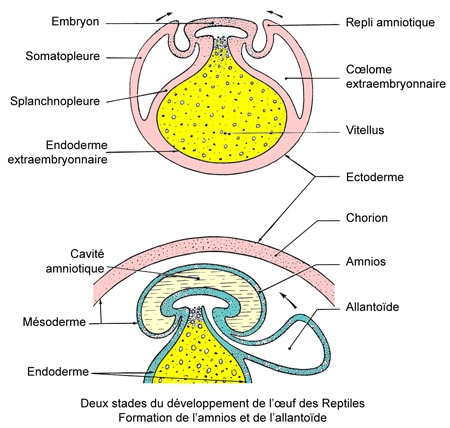
Schéma extraits du livre de Raymond ROLLINAT
« La vie des Reptiles de France » 1934.
Publié avec le concours de Marie PHISALIX
Les engagements de Marie PHISALIX
En tant que médecin et citoyenne, Marie PICOT-PHISALIX a apporté son aide dans le domaine sanitaire et dans la défense de la cause des femmes : Vice-présidente pour l’amélioration du sort de la Femme en 1935, elle présidera, à 84 ans, une réunion de la Ligue Française pour le Droit des femmes et sur le rôle des électrices dans la reconstruction du pays en 1945. La Présidente parlera du « féminisme souriant d’une grande Dame » ! En tant que médecin elle a procédé à des vaccinations contre la variole et la typhoïde, en 14-18, et a assuré la garde de la Ménagerie du Jardin des Plantes en 39-45.
Marie PHISALIX n’a jamais oublié Mouthier-Hautepierre, à qui elle a fait don d’un important mobilier scolaire en 1912.
Ses distinctions sont nombreuses : Officier d’Académie en 1901, Officier de l’Instruction publique en 1908, deux prix Bréant (1916, 1922), Grand Prix de l’Exposition d’Hygiène de Strasbourg (1923), Diplôme et médaille de l’Exposition vaticane (1925), Grand Prix Lasserre de l’Instruction publique.
Elle a été décorée de la Légion d’Honneur en 1923.
Elle a été élue Présidente d’honneur de la Société d’Histoire Naturelle du Doubs en 1924 et nommée Associée correspondante de notre Académie le 26 janvier 1933. Elue Présidente de la Société Zoologique de France en 1937. Elle a échoué de très peu à l’Académie de Médecine où l’on se souvient que Marie CURIE n’a été admise que très tard, après ses deux prix Nobel !
La tombe des PHISALIX
Dans le cimetière de Mouthier-Hautepierre, tout en haut, la sépulture des deux savants regarde la vallée. On peut y lire cette inscription :
Famille des Docteurs Césaire et Marie PHISALIX
Chevaliers de la Légion d’Honneur
CONCLUSION
La carrière de nos deux compatriotes est admirable.
Leurs travaux dans le domaine des venins, de la sérothérapie et de l’Herpétologie ont eu et ont encore des prolongements et des retombées considérables.
Notre Région peut s’honorer de les avoir formés et côtoyés et s’honorerait de les célébrer avec tout le respect qu’ils méritent.
Lors d’un Colloque consacré à Courbet, en septembre dernier, Madame le Conservateur en chef du Musée du Louvre faisait remarquer à l’auditoire que « la Franche-Comté ne reconnaît pas assez ses enfants ». Même si ce constat est vrai et dérangeant on objectera, tout de même, que Louis PASTEUR et Georges CUVIER ont reçu des hommages à la hauteur de la portée de leurs découvertes qui ont fait « beaucoup d’ombre aux autres savants comtois ! » ; à nous, désormais, de faire une place honorable à ce couple de chercheurs.
Quant à la paternité de la découverte du sérum antivenimeux, nous pensons, en toute objectivité, que Césaire PHISALIX, avec quelques heures d’avance, a bien fait l’annonce décisive.
NB : Ce litige nous rappelle, toutes proportions gardées, les conflits célèbres de DARWIN-WALLACE, ROUX-FLEMING ou PASTEUR-TOUSSAINT… et beaucoup d’autres, où c’est souvent le plus pugnace sinon le plus ambitieux qui a imposé son nom dans les pages de la célébrité !
BIBLIOGRAPHIE
Bochner R. et Goyffon M. 2007. L’œuvre scientifique de Césaire Phisalix (1852-1906), découvreur du sérum antivenimeux. Bull. Soc. Herpét. Fr., 123, pp. 15-46.
Brygoo E. R. 1985. La découverte de la sérothérapie antivenimeuse en 1894. Phisalix et Bertrand ou Calmette, Bull. Soc. Anc. Elèves Inst. Pasteur, 4, pp. 10-21.
Calmette A. 1894. L’immunisation artificielle des animaux contre le venin des serpents et la thérapeutique expérimentale des morsures venimeuses. C. R. Soc. Biol. 46, 10 février, pp. 120-124.
Calmette A. 1896. Le venin des serpents. Physiologie de l’envenimation. Traitement des morsures venimeuses par le sérum des animaux vaccinés. Société d’Editions scientifiques, 72 pages.
Charas M. 1685. Nouvelle expérience sur la Vipère, où l’on verra une description exacte de toutes ses parties, la source de son venin, ses divers effets, et les remèdes exquis que les artistes peuvent retirer de cet animal. In 8°. Paris. Premier livre écrit en langue française se rapportant à la Vipère.
Cupillard C. 2007. Auguste-Césaire Phisalix (1852-1906) : un savant au pays de Courbet. Bull. Soc. Herp. Fr., 123, 9-13.
Cupillard C. et Videlier P-Y. 2007. Césaire et Marie Phisalix. Deux savants au pays de Courbet. 24 pages.
Desgrez A. 1910. Notices biographiques. XVIII – Césaire Phisalix. Archives de Parasitologie. t. XIV, pp. 54-153.
Fontana F. 1781. Traité sur le venin de la vipère, sur les poisons américains, sur le laurier-cerise et sur quelques poisons végétaux. 318 pages.
Goyffon M. et Chippaux J-P. 2008. La découverte du sérum antivenimeux (10 février 1894), pp 32-35.
Lescure J. et Thireau M. 2007. Marie Phisalix (1861-1946), une grande dame de l’Herpétologie. Bull. Soc. Herp. Fr. 124, 9-25.
Phisalix C. et Bertrand G. 1894. Atténuation du venin de vipère par la chaleur et vaccination du cobaye contre ce venin. C. R. Acad. Sc., 5 février, pp. 288-291.
Phisalix C. et Bertrand G. 1894. Sur la propriété antitoxique du sang des animaux vaccinés contre le venin de vipère. C. R. Soc. Biologie. 46, 10 février, pp. 111-113.
Phisalix C. et Bertrand G. 1894. Sur la propriété antitoxique du sang des animaux vaccinés contre le venin de vipère. C. R. Acad. Sciences, 118, 12 février, pp.356-358.
Phisalix-Picot M. 1900. Recherches embryologiques, histologiques et physiologiques sur les glandes à venin de la Salamandre terrestre.Thèse de médecine. 140 p. 7 planches.
Phisalix M. 1922. Animaux venimeux et venins. La fonction venimeuse chez tous les animaux : les appareils venimeux, les venins et leurs propriétés ; les fonctions et usages des venins ; l’envenimation et son traitement. Masson Ed., 2 volumes ; 653 pages + 854 pages ; planches couleurs et noir et blanc.
Phisalix M. 1940. Vipères de France. Editions Stock. 228 pages.
Rollinat R. 1937. La vie des Reptiles de la France centrale. Libr. Delagrave. 343 p.
Professeur Claude-Roland MARCHAND
Membre correspondant, Académie des Sciences, Belles Lettres et Arts de Besançon
26 septembre 2011.
Ajout du 12 décembre 2016
Un lecteur, M. Christian Agnus nous communique la photo d'une chapelle qu'il a découverte dans le cimetière des Chaprais à Besançon. Dans cette chapelle, une épitaphe : "cette chapelle, hommage de pieuse reconnaissance est érigée par les soins du Docteur Phisalix et de Mlle Anna Maire 1895".

Clichés © Christian Agnus
Mais qui est cette mystérieuse personne Anna Maire qui a contribué aux côtés du Dr Phisalix à l'érection de cette chapelle ?
Claude Roland Marchand a contacté Christophe Cupillard, le conservateur du petit musée PHISALIX de Mouthier-Hautepierre qui lui a appris que Anna Maire, artiste, sculptrice (1828-1906) était la marraine de Césaire Phisalix (1852-1906). En fait "Anna Maire" est un pseudonyme et que son nom véritable était Anne Ferret.
Christian Agnus nous a adressé des photographies des deux personnages prises en 1893 par Henri d'Orival de Besançon au château de Lavigny appartenant à la famille Mareschal de Longeville.
Un grand merci à tous ces informateurs.



























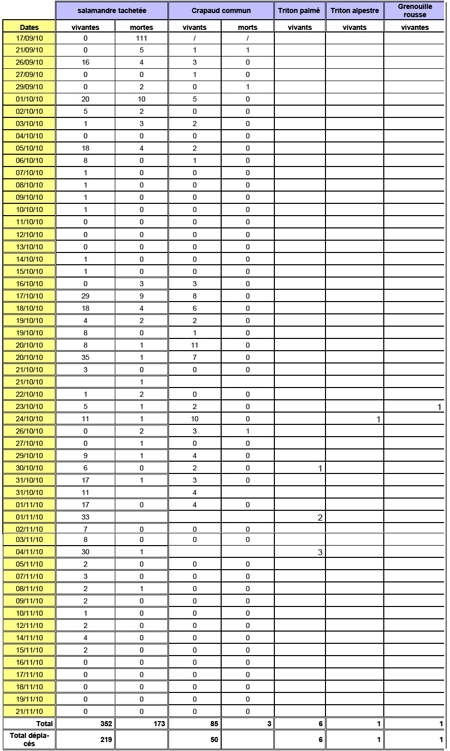
 Pontes en eau calme
Pontes en eau calme







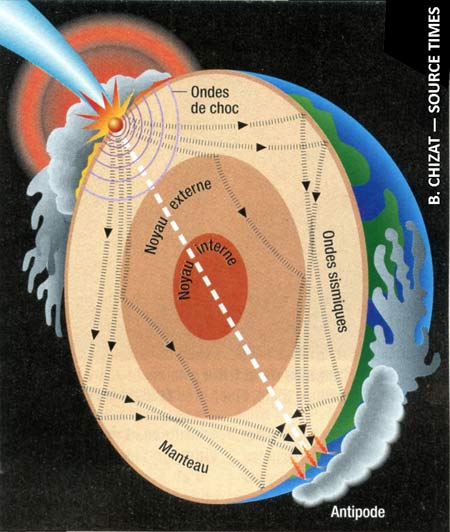
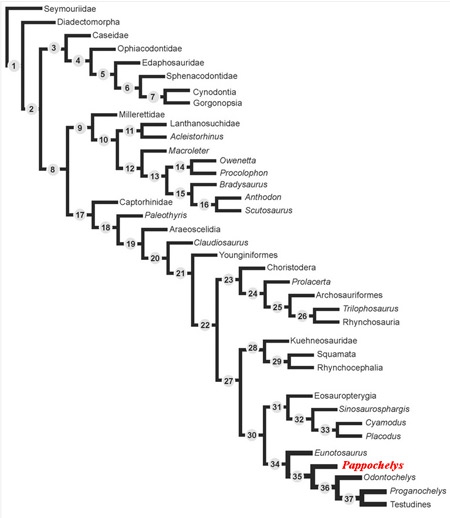
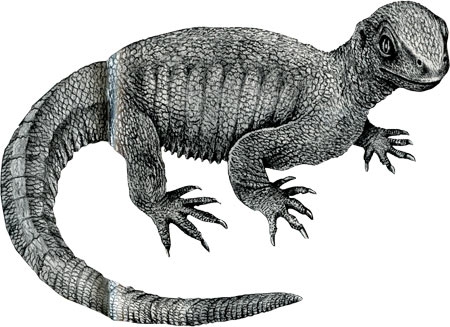
 Mise à jour de la phylogénie des tortues
Mise à jour de la phylogénie des tortues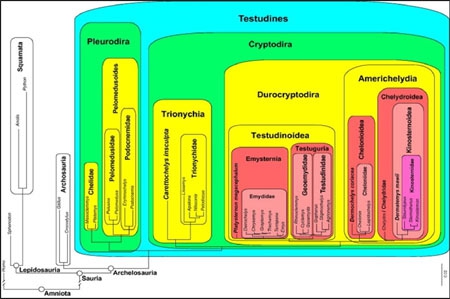

 La Couleuvre d'Esculape (Zamenis longissimus)
La Couleuvre d'Esculape (Zamenis longissimus)

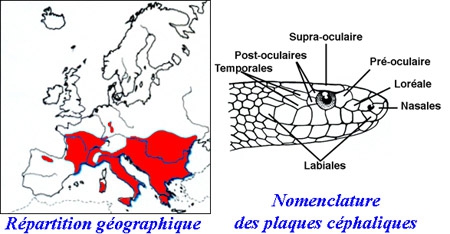

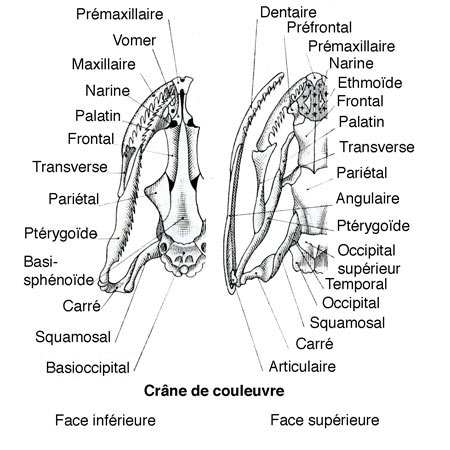
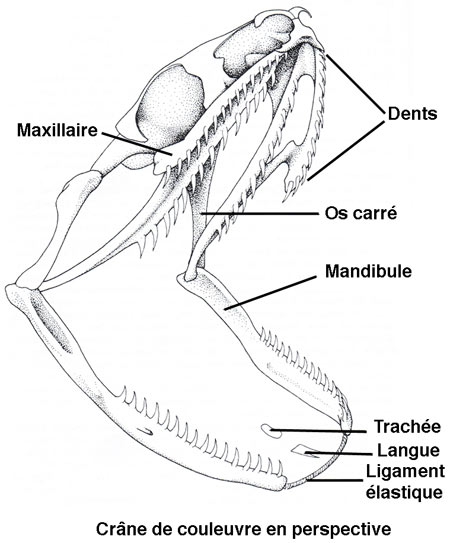



 La Couleuvre à collier
La Couleuvre à collier
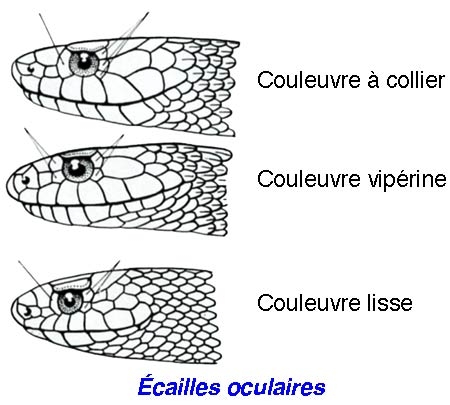















 La Couleuvre vipérine
La Couleuvre vipérine



 Une plaquette de sensibilisation pour la Couleuvre vipérine
Une plaquette de sensibilisation pour la Couleuvre vipérine










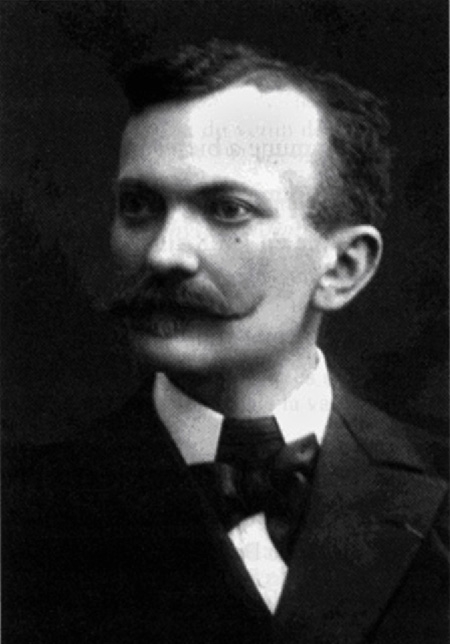













 Le Lézard ocellé
Le Lézard ocellé 









 La Vipère Aspic Vipera aspis
La Vipère Aspic Vipera aspis


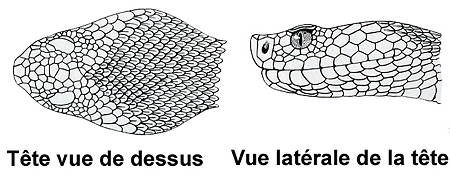






 La Péliade : Vipera berus
La Péliade : Vipera berus







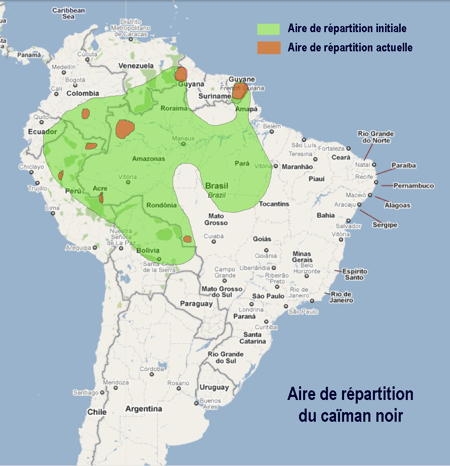
 Parc national des Pyrénées:
Parc national des Pyrénées:
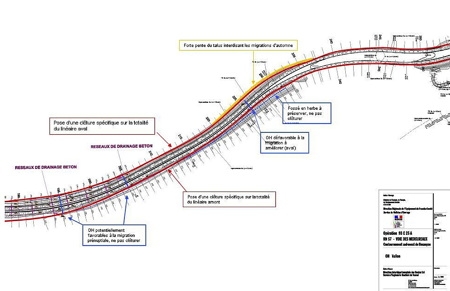
 Mortalité élucidée
Mortalité élucidée

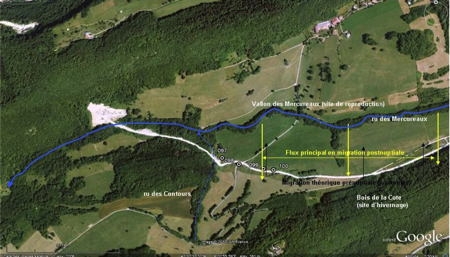





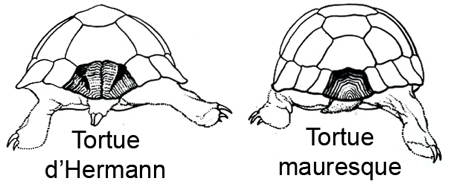
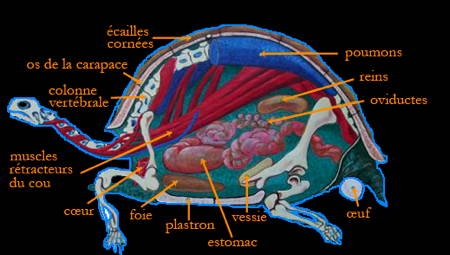
 La Tortue d'Hermann
La Tortue d'Hermann


 Le Lézard fouette-queue
Le Lézard fouette-queue
