04/06/2016
Le Sénat vote contre les coraux et pour le développement économique
Le Sénat vote contre les coraux et pour le développement économique
Écoutez également l'émission de France Inter.
La France, deuxième propriétaire du plus grand patrimoine corallien au monde, a vu lundi 23 mai 2016 le Sénat retoqué l’interdiction de la destruction des coraux dans le cadre de la loi sur la biodiversité. Pourtant, grâce à ses 10 % de récifs coralliens au monde, la deuxième plus grande barrière de corail et le plus grand lagon mondial, la France pourrait être un acteur majeur dans la conservation des récifs coralliens. Conscient de cette richesse, en 1999, le pays affichait pourtant un désir de conserver ce patrimoine avec l’Initiative Française pour les Récifs Coralliens, un objectif désormais bafoué par les sénateurs.
Se disant anxieux de « ne pas contraindre le développement des économies locales », le Sénat a posé un amendement contre le projet de loi qui vise à la protection des récifs coralliens, ainsi les sénateurs consentent au dragage et à la destruction des coraux. Un tel amendement encouragera sûrement des projets comme en Guadeloupe où, pour l’agrandissement du port de Pointe-à-Pitre, 7 millions de m3 de coraux ont été réduits à néant. Un autre projet portuaire à Fort-de-France, en Martinique, a lui été entravé par les écologistes qui, après 3 ans de batailles juridiques, ont réussi à ce que les constructeurs se fournissent dans les carrières plutôt que dans les coraux pour faire des remblais. Or, avec cet amendement, les sénateurs endiguent les actions de défense pour la nature, défendant des intérêts économiques à court terme contre un écosystème indispensable qui génère des revenus d’environ 375 milliards dans le monde, chaque année.
Cependant, les coraux engendrent bien plus que des revenus économiques liés au tourisme ; couvrant moins de 0,2 % des océans, ils abritent 30% de la biodiversité marine. Bien plus générateurs de richesse étant vivant que comme remblais, ces récifs sont des nurseries et des garde-manger pour les poissons qui alimentent la pêche. De plus, si les scientifiques notent une bonne reprise du corail dans le milieu naturel, malgré qu’il s’agisse d’un processus très long, il reste essentiel de ne pas détruire les récifs déjà en danger par l’augmentation de la température de l’eau.
Et pourtant, les coraux qui subissent un blanchissement extrême n'ont ps besoin de cette prise de position pour être menacés de disparition (voir l'article de Sciences et Avenir).
13:24 Publié dans Biologie, Cnidaires, Environnement-Écologie, Limnologie-hydrobiologie, Pollution | Tags : sénat, coraux, dragage des coraux | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
09/10/2012
Grenouille et Amanite phalloïde
Grenouille et Amanite phalloïde
Ci-dessous, une photo insolite de Jean-Marc Moingeon qui illustre bien le "toadstool" des anglophones.
Nos voisins d’Outre-Manche sont très méfiants, voire réticents, vis-à-vis de la consommation des champignons sauvages. Le terme « toadstool », littéralement « tabouret à crapaud » est alors employé depuis fort longtemps pour désigner les champignons en général, et plus particulièrement ceux qui sont vénéneux.
Cette jeune grenouille rousse, fort coopérante et patiente avec le photographe, ne pensait pas si bien illustrer ce mot anglais en s’installant sur le chapeau vert olive de l’amanite phalloïde.
Quant à ceux qui rêvaient d’accommoder des cuisses de grenouilles avec des champignons, ils en seront pour leurs frais…

08:35 Publié dans Cnidaires, Herpétologie | Tags : grenouille rousse, amanite phalloïde | Lien permanent | Commentaires (1) | ![]() Facebook | | |
Facebook | | |
23/07/2010
Coraux des Antilles (1)
Sous le vocable de corail, on désigne plusieurs formes animales coloniales qui appartiennent toutes au phylum des Cnidaires et dont le squelette est appelé polypier. Ce premier chapitre présente les principaux représentants des Cnidaires. Il définit et situe les coraux dans ce phylum.
14:15 Publié dans Cnidaires, Environnement-Écologie, Invertébrés, Océanographie | Tags : coraux, cnidaires, anthozoaires, madrépores, scléractiniaires, caraïbe, antilles, récif corallien | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
Coraux des Antilles (2)
Classification et inventaire des coraux hermatypiques (constructeurs de récifs) rencontrés aux Antilles
12:15 Publié dans Cnidaires, Environnement-Écologie, Invertébrés, Océanographie | Tags : coraux, antilles, anthozoaires, scléractiniaires, hydrozoaires, madrépores, caraïbe, récif corallien | Lien permanent | Commentaires (2) | ![]() Facebook | | |
Facebook | | |
22/07/2010
Coraux des Antilles (3)
Anatomie des coraux hermatypiques des Antilles
14:15 Publié dans Cnidaires, Environnement-Écologie, Invertébrés, Océanographie | Tags : coraux, province caraïbe, caraïbe, antilles, anthozoaires, scléractiniaires, madrépores, cnidaires, guadeloupe | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
21/07/2010
Coraux des Antilles (4)
Clé simplifiée de détermination des coraux des Antilles
14:14 Publié dans Cnidaires, Environnement-Écologie, Invertébrés, Océanographie | Tags : coraux, province caraïbe, caraïbe, antilles, anthozoaires, scléractiniaires, madrépores, cnidaires, guadeloupe | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
20/07/2010
Coraux des Antilles (5)
Hydrocoralliaires et Scléractiniaires en place dans le récif
14:14 Publié dans Cnidaires, Environnement-Écologie, Invertébrés, Océanographie | Tags : coraux, antilles, cnidaires, anthozoaires, scléractiniaires, madrépores, caraïbe | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
19/07/2010
Coraux des Antilles (6)
Nutrition, calcification, reproduction et développement des coraux de la Province caraïbe
14:14 Publié dans Cnidaires, Environnement-Écologie, Invertébrés, Océanographie | Tags : coraux, province caraïbe, caraïbe, antilles, anthozoaires, scléractiniaires, madrépores, cnidaires, guadeloupe | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
18/07/2010
Coraux des Antilles (7)
Croissance du Corail et répartition des récifs dans la Province Caraïbe
14:13 Publié dans Cnidaires, Environnement-Écologie, Invertébrés, Océanographie | Tags : cnidaires, anthozoaires, scléractiniaires, madrépores, antilles, récif corallien, caraïbe | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
17/07/2010
Coraux des Antilles (8)
Différents types de récifs coralliens. Morphologie et genèse des récifs coralliens des Antilles
14:13 Publié dans Cnidaires, Environnement-Écologie, Invertébrés, Océanographie | Tags : coraux, antilles, cnidaires, anthozoaires, scléractiniaires, madrépores, récif corallien, caraïbe | Lien permanent | Commentaires (2) | ![]() Facebook | | |
Facebook | | |
16/07/2010
Coraux des Antilles (9)
Biocénoses récifales remarquables de la Province caraïbe. Compétition, prédation, stratégies de défense, associations : commensalisme, symbiose.
14:12 Publié dans Cnidaires, Environnement-Écologie, Invertébrés, Océanographie | Tags : coraux, province caraïbe, caraïbe, antilles, anthozoaires, scléractiniaires, madrépores, cnidaires, guadeloupe | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
15/07/2010
Coraux des Antilles (10)
Chapitre annexe présentant d'autres organismes associés au récif corallien qui n'ont pas trouvé leur place dans les précédents chapitres
18:10 Publié dans Cnidaires, Environnement-Écologie, Invertébrés, Océanographie | Tags : province caraïbe, récif corallien, coraux, algues, foraminifères, éponges, spongiaires, porifera, gorgones, annélides, polychètes, brachyoures, macroures | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
Coraux des Antilles (11)
Évolution des récifs coralliens actuels de la Caraïbe.
Problème du blanchissement des coraux dans les océans du monde
05:07 Publié dans Cnidaires, Environnement-Écologie, Invertébrés, Océanographie, Poissons | Tags : coraux, antilles, cnidaires, anthozoaires, scléractiniaires, madrépores, récif corallien, caraïbe | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
05/10/2009
Les Cnidaires d’eau douce
 Hydres et autres Cnidaires
Hydres et autres Cnidaires
en eau douce
par André Guyard
(Texte mis à jour le 05/01/2013)
Les Cnidaires sont des Métazoaires (animaux pluricellulaires) diploblastiques (à deux feuillets), à symétrie radiaire parfois accompagnée d’une symétrie bilatérale. Ils comprennent environ dix mille espèces toutes aquatiques, la plupart marines et carnivores. Le corps possède une cavité unique, le coelentéron ou cavité gastrique. Des cellules urticantes ou cnidoblastes sont localisées dans des zones stratégiques de l’ectoderme et jouent un rôle dans la capture des proies. Les Cnidaires étaient autrefois regroupés avec les Cténaires (formes exclusivement marines) dans l’embranchement devenu caduque des Coelentérés.
ORGANISATION GÉNÉRALE
La plupart des Cnidaires ont deux stades dans leur cycle de vie sans parler de la phase larvaire : un stade fixé donc benthique - le polype - et un stade libre planctonique - la méduse.
Le corps du polype a la forme d’un sac fixé à une extrémité sur le substrat par une sole pédieuse. A l’autre extrémité, au sommet d’un petit renflement dessinant une zone hypostomiale, s’ouvre l’unique orifice du corps, la bouche entourée par des tentacules ; elle est dirigée vers le haut et met en communication avec l’extérieur la cavité gastrique dont les ramifications se terminent dans les tentacules. Le corps se divise ainsi en trois régions : corps du polype, tentacules et sole pédieuse. Le polype est capable de reproduction asexuée.
La méduse qui représente la forme libre a au contraire, l’orifice buccal dirigé vers le bas et offre l’image d’une cloche transparente dont le battant correspond à la région gastrique (manubrium).
La cloche ou ombrelle, est formée de fines digitations, les tentacules, implantés sur le pourtour d’un cercle rétréci (chez les Hydroméduses) par un voile ou velum, délimitant une cavité sous-ombrellaire dans laquelle pend le manubrium.
La bouche s’ouvre à l’extrémité de ce manubrium ; elle donne accès à un court oesophage qui aboutit dans un estomac situé au sommet de la cloche. Il en part des canaux radiaires au nombre de 4 ou d’un multiple de 4, qui rejoignent un canal circulaire ou marginal bordant l’ouverture de l’ombrelle. Ce canal envoie un diverticule dans chaque tentacule et est flanqué de deux cordons nerveux qui se prolongent également dans les tentacules.
Les gonades se développent sur les canaux ou sur le manubrium. La méduse possède des organes des sens : ocelles ou yeux rudimentaires disposés à la base des tentacules, et statocystes, ou organes d’équilibration situés entre les tentacules.
Parmi les formes d’eau douce de nos régions, on ne trouve que des représentants de la classe des Hydrozoaires. Cette classe groupe en principe des individus dont le cycle de vie est métagénétique avec alternance de générations de polypes asexués et de méduses sexuées. Cependant il existe des exceptions et c’est le cas des hydres d’eau douce (ordre des Hydrides) qui ne présentent que la forme polype et des Limnoméduses où le stade méduse devient nettement prépondérant.
LES HYDRES D’EAU DOUCE
Elles comportent plusieurs espèces commune à la belle saison. On les trouve fixées aux végétaux immergés dans les mares et les étangs.
MORPHOLOGIE EXTERNE
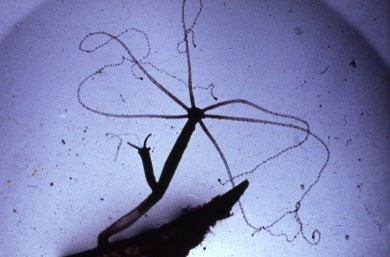
A l’état d’extension, l’hydre est un sac allongé, terminé par une couronne de six tentacules (ou 8) très longs et très contractiles qui entourent la bouche. Dans la région opposée, l’hydre est fixée par la sole pédieuse.
On distingue dans nos régions trois espèces : Pelmatohydra oligactis (fig. 1) a une colonne gastrique d’un brun noirâtre qui surmonte un pédoncule long mince et translucide, et porte des tentacules très étirés.
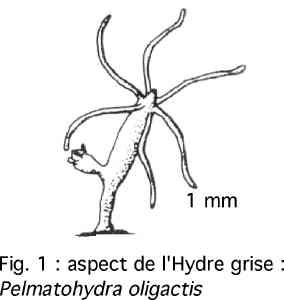
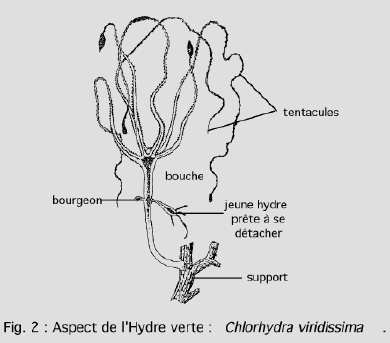
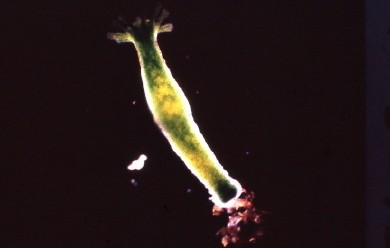
Elle doit sa couleur à la présence de
Hydra attenuata, gris brun, très pâle au niveau du pédoncule qui se prolonge par une colonne de même diamètre.
En période de reproduction, l’hydre présente à sa surface des renflements qui correspondent aux ovaires ou aux testicules. Elle peut également bourgeonner.
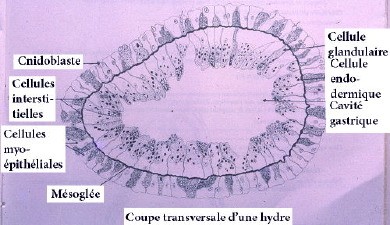
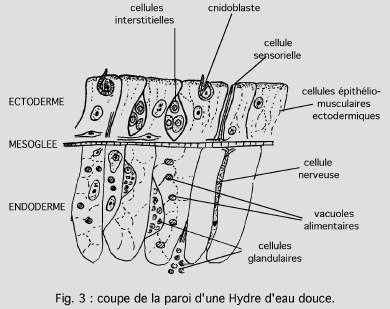
STRUCTURE
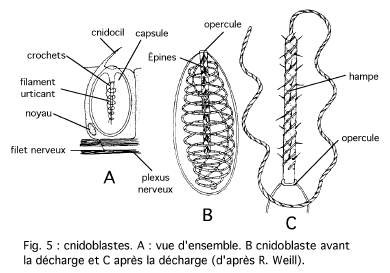
La paroi du corps (fig. 3) comporte un ectoderme unistratifié de cellules myo-épithéliales, avec des cellules nerveuses multipolaires, des massifs de cellules interstitielles, à caractères embryonnaires, pouvant redonner par multiplication et différenciation tout élément cellulaire ; des cnidoblastes ou cellules urticantes, munies d’un harpon creux injectant aux proies un poison l’actinocongestine.
L’endoderme tapisse la cavité digestive. Il est formé d’une unique couche de cellules très vacuolisées dont la base s’étendant sur la mésoglée, montre des myofibrilles transversales et leur bord libre du côté de la cavité présente des flagelles. Elles sont douées de phagocytose. On trouve également des cellules glandulaires et des cellules neuroépithéliales comme dans l’ectoderme.
La mésoglée est une substance colloïdale peu épaisse constituée par les lames basales des deux épithéliums.
BIOLOGIE
1. Locomotion et mouvements.
- Suivant le degré d’excitation, l’hydre peut se rétracter en une boule à peine visible à l’œil nu. Le réseau nerveux assure une certaine coordination aux mouvements des tentacules étalés normalement en position de chasse.
- Les déplacements se font par glissement sur la sole pédieuse ou par arpentage avec culbute (fig. 4). L’hydre présente un phototropisme variable suivant l’espèce.
- L’hydre peut quitter son support et nager par ses tentacules.

Les tentacules capturent les proies, les paralysent par les cnidoblastes et les amènent à la bouche. La digestion est extra-cellulaire dans la cavité gastrique avec un broyage dû aux mouvements du corps, puis intra-cellulaire après phagocytose dans les cellules endodermiques.
L’hydre s’accroît constamment par sa région orale par mitose de cellules interstitielles, si les conditions de vie sont favorables. Cette croissance est compensée par l’usure des cellules au niveau de la sole pédieuse. Une Hydre est ainsi totalement rénovée en un à deux mois.
4. Multiplication asexuée
- Bourgeonnement
- Scissiparité longitudinale par dédoublement de la zone de croissance.
- Régénération très facile.
À l'inverse, lorsque les biologistes allemands ont inactivé spécifiquement ce gène, les cellules souches de l'animal se sont différenciées en cellules adultes.
Bien que présent dans l'ensemble du monde animal, et donc chez l'Homme, le gène FoxO voit son expression diminuer au fil du processus normal de vieillissement... sauf chez l'hydre qui, de fait, ne vieillit pas et ne meurt jamais. En conclusion, un seul gène assure la régénération sans fin de tous les tissus du corps de l'hydre. Une propriété à exploiter pour lutter contre le vieillissement chez l'Homme ?
5. Reproduction sexuée
Elle apparaît quand les conditions de température deviennent défavorables : 10-12°C pour P. oligactis, 16-20°C pour C. viridissima et H. attenuata. P. oligactis et H. attenuata sont gonochoriques (sexes séparés). C. viridissima est hermaphrodite protandre (les spermatozoïdes sont mûrs avant les ovules).
Les gonades constituent des renflements apparaissant sur la colonne. Les testicules apparaissent dans le quart antérieur de la colonne, les ovaires à la moitié de la colonne.
Après fécondation, l’œuf commence sa segmentation totale et égale.
RÔLE BIOLOGIQUE DES HYDRES D’EAU DOUCE
Elles jouent un rôle qui passe inaperçu dans les biocénoses dulçaquicoles.
Utilisation dans les méthodes biologiques
Elles ne sont citées que dans la méthode des saprobies dans les zones :
β-mésosaprobe : Hydra vulgaris, Hydra oligactis = H. fusca et Hydra polypus existent déjà en zone α-mésosaprobe dans le périphyton des étangs des fossés et des eaux calmes.
oligosaprobe : Chlorohydra viridissima. Cordylophora lacustris : existe déjà dans la zone β-mésosaprobe.

Dans ce déversoir ferrugineux du lac Pavin (Auvergne),
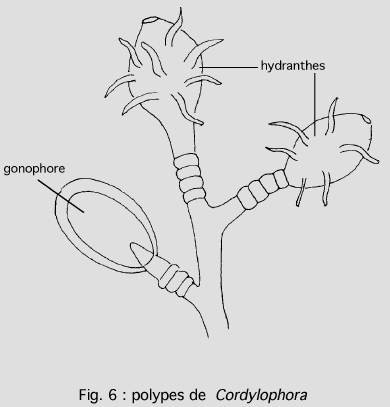
Dans les eaux saumâtres, on rencontre une espèce d’Hydraire gymnoblastique de la famille des Claviidae : Cordylophora caspia ( = lacustris). Cette espèce répandue sous toutes les latitudes, se présente sous la forme d’une colonie de polypes pouvant atteindre plusieurs cm (fig. 6). La colonie est fixée au substrat par un réseau de stolons, sur lesquels s’élèvent les hydrocaules portant les polypes (hydranthes) et les gonophores (polypes spécialisés dans la production de gamètes). Il n’y a pas de stade méduse.
Dans cet ordre, le stade méduse devient prépondérant et le polype, très régressé, de quelques millimètres de longueur, est souvent solitaire ou forme des colonies de 4 à 5 individus seulement. Les représentants vivent en eau douce ou saumâtre.
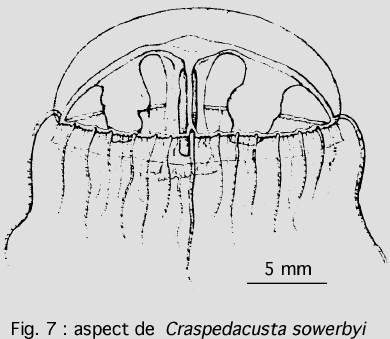

L’apparition de cette méduse en Europe vers 1880 pose des problèmes encore non résolus, par exemple celui de sa reproduction. Généralement, les méduses trouvées dans une même région sont de même sexe. Ce fait est dû probablement à l’existence d’une génération de polypes asexués décrits sous le terme de Microhydra ryderi. Mais il s’agit de la même espèce.
On ignore comment elle est arrivée là : cette méduse existe dans le bassin de l’Institut des Sciences Naturelles, place Leclerc à Besançon. Dans les années mille neuf cent soixante, elle s’est signalée par une prolifération étonnante, envahissant de ses ombrelles la totalité du volume du bassin. De nouveau dans les années quatre-vingt, autre prolifération. La forme polype, difficile à observer, persiste certainement sur les parois du bassin. Et la forme méduse, forme sexuée se manifeste lorsque les conditions de vie du polype deviennent difficiles.
Autre limnoméduse, dans les lagunes saumâtres du Sud de la France, Picard (1951) a observé la limnoméduse Odessia maeotica f. gallica qui présente annuellement deux périodes d’activité sexuelle et fait partie de la famille des Moerisiidae.
On ne connaît comme autre méduse d’eau douce que le genre africain Limnocnida.
16:23 Publié dans Cnidaires, Invertébrés, Limnologie-hydrobiologie | Lien permanent | Commentaires (5) | ![]() Facebook | | |
Facebook | | |


