25/03/2010
La Bernache nonnette
 La Bernache nonnette
La Bernache nonnette
Branta leucopsis (Bechstein, 1803)
par André Guyard
Oie de petite taille, la Bernache nonnette se reconnaît immédiatement à la coloration noire du cou et de la poitrine et à la tête blanche. Le dos est gris barré de noir et le ventre est plus pâle. dessus gris barré contrastant avec un dessous très pâle. La Bernache nonnette a un petit bec triangulaire noir, des pattes noires et un croupion blanc.

En été, la Bernache nonnette fréquente les falaises et les éboulis des îles arctiques. En hiver, elle habite les prés inondés et les marais côtiers, les rives basses des baies maritimes et les vasières à marée basse.
Provenant du Groenland, du Spitzberg et de la Nouvelle Zemble les Bernaches nonnettes commencent leur migration à la fin août ou au début du mois de septembre. Elles atteignent les rivages de l'Ecosse, de l'Irlande, la côte ouest de la Grande-Bretagne et le littoral de l'Allemagne et des Pays-Bas en ce qui concerne le dernier groupe. En France, l'espèce est très rare en temps normal, quelques dizaines d'individus qu'on trouve principalement en baie de Somme ou du Mont St-Michel. Cependant, lors d'hivers très rigoureux, la France a accueilli jusqu'à 8 000 bernaches nonnettes. Son aire de répartition est alors plus vaste et affecte toutes les petites baies et les estuaires abrités.

La saison de nidification commence peu après le retour dans l'Arctique. Les Bernaches nonnettes se réunissent pour nicher en colonies. Le nid, construit principalement de végétaux et tapissé de duvet, est situé sur la corniche d'une falaise, sur un îlot non éloigné du littoral ou à même la toundra dégagée. Le site est parfois partagé avec des guillemots. La femelle y dépose 3 à 5 œufs qu'elle couve seule pendant une période variant de 24 à 25 jours alors que le mâle monte une garde vigilante à proximité. Les jeunes sont actifs dès l'éclosion et savent voler vers 40 ou 45 jours. Le groupe familial reste uni pendant la migration et l'hivernage.
Comme toutes les oies, la Bernache nonnette est végétarienne et broûte les graminées. En hiver, lorsque l'herbe est moins drue, la Bernache mange aussi des algues, des insectes aquatiques, des mollusques et des crustacés. L'espèce se nourrit à toute heure du jour et préfère l'herbe de la zone côtière périodiquement submergée par les flots. Si elle n'en dispose pas, elle se rabat sur les prairies situées en arrière du littoral.
Vidéo et photos : André Guyard
Sources :
Peterson R, Mounfort G., Hollom P.A.D. (1962-. - Guide des Oiseaux d'Europe. 358 p. Delachaux & Niestlé Ed.
http://www.oiseaux.net/oiseaux/bernache.nonnette.html
Une vidéo impressionnante : sortie du nid d'un poussin d'oie bernache
15:03 Publié dans Limnologie-hydrobiologie, Océanographie, Ornithologie | Tags : anatidés, ansériformes, oies, oiseaux, bernache | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
23/03/2010
Les oiseaux du parc national de Celestún (Yucatan, Mexique)
 Les oiseaux du parc national de Celestún (Yucatan, Mexique)
Les oiseaux du parc national de Celestún (Yucatan, Mexique)
par André Guyard
Situé dans l'État du Yucatan à 92 kilomètres de Mérida, le parc national de Celestún s'étend sur 60 000 hectares comprenant l'estuaire d'une rivière et les marais environnants. L'estuaire a 25 kilomètres de long et une profondeur moyenne de 1,50 m. Sa température moyenne annuelle est de 26,2°C.
Le 19 Juillet 1979, le site a été déclaré "Celestún Wildlife Refuge" par le gouvernement fédéral mexicain et, plus tard, en 1986, Patrimoine de l'Humanité par l'ONU. La réserve, qui couvre une variété de milieux humides, est considérée comme l'une des plus grandes zones de mangrove du Golfe du Mexique.

La mangrove est un milieu naturel qui, par l'enchevêtrement des racines des palétuviers rouges constitue une défense naturelle contre l'érosion due aux cyclones et aux tsunamis mais surtout une zone de nursery pour de nombreuses espèces de poissons et de crustacés. Le palétuvier rouge est l'arbre que l'on trouve en bordure de mer. Ses racines échasses constituent un barrage pour les vagues et également un refuge pour de nombreux organismes fixés (huîtres, coraux, ascidies, etc.).
Celestún Nature Reserve est une des plus importantes zones protégées du pays en raison de l'abondance des espèces d'oiseaux indigènes et migrateurs qui s'y trouvent. Le parc de représente une importante aire d'alimentation et de repos pour un grand nombre d'oiseaux migrateurs. Il constitue l'un des deux sites de nidification et de reproduction des flamants rouges des Caraïbes. Dans cette zone de refuge, on a identifié de nombreuses espèces d'oiseaux migrateurs qui arrivent chaque année pour passer la saison d'hiver, comme le Grand Héron, le Canard Chipeau et le Balbuzard pêcheur, entre autres. On y rencontre également pélicans, albatros et cormorans.
Les Flamants de Celestún
La principale attraction de ce parc est la lagune des flamants rouges qui exigent un habitat avec des fonds vaseux, une eau saumâtre et peu profonde. Ils sont protégés des vagues et des inondations. Les lagunes sont bordées par une mangrove dense et luxuriante appelée Ria Celestún.
Pélicans blancs
Dans cette mangrove, on peut apercevoir des singes araignées (atèles) et, avec de la chance, des ocelots. On peut y voir également des tortues.
Cormorans
14:15 Publié dans Limnologie-hydrobiologie, Océanographie, Ornithologie | Tags : mexique, yucatan, celestun, flamants, pélicans, hérons, canards, cormorans | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
19/03/2010
L'Eider à duvet
 L'Eider à duvet
L'Eider à duvet
Somateria mollissima (L. 1758)
Par André Guyard
L'Eider appartient à l'ordre des Ansériformes et à la famille des Anatidés (canards).
L'Eider à duvet se distingue des autres canards par sa grande taille (60 cm), le profil droit de son bec et son vol qui alterne vol battu (vol habituel des canards) et vol plané.

Le mâle présente une calotte noire, une nuque verte, des joues blanc et vert.C'est le seul canard qui possède un dos blanc et un ventre noir.
La femelle présente une livrée brune striée de nombreuses barres foncées.

L'Eider à duvet est un habitant du littoral marin. On le rencontre aussi bien sur les côtes rocheuses ou sablonneuses. En hiver, on peut l'apercevoir occasionnellement à l'intérieur des terres sur les fleuves ou les lacs.
Son aire de nidification se situe sur l'Atlantique Nord, à la limite de la banquise. L'Eider à duvet est hivernant en France où on le retrouve sur les côtes de la Manche et en Bretagne. Formidable plongeur qui récolte crustacés et coquillages jusqu'à 15 mètres.

Le duvet de canard étant depuis longtemps connu pour ses propriétés isolantes, il est récolté après la période de nidification pour confectionner des édredons.
La période de reproduction commence fin mai-début juin. La femelle bâtit son nid tout près de l'eau sur le sable ou dans une anfractuosité de rocher. Il est construit de matériaux divers : débris végétaux, fragments de coquillages, et garni d'une épaisse couronne de duvet de la femelle. Elle y dépose 4 à 6 œufs couvés pendant 25 à 28 jours. Les jeunes sont nidifuges et s'envolent dans un délai de 65 à 75 jours.
Les femelles seules assurent la protection des poussins
Après la période de reproduction, couvaison et soins aux jeunes sont dévolus aux femelles. Pendant ce temps, les mâles se rassemblent en troupes nombreuses qui peuvent dépasser une centaine d'individus.
L'Eider se nourrit surtout de mollusques (moules, coques, bigorneaux mesurant de 7 à 40 mm) et de crustacés (crabes). Cependant, il ne dédaigne pas les insectes aquatiques, les poissons et les échinodermes (étoiles de mer) qui sont des ingrédients courants à son menu. Son alimentation est complétée par divers végétaux qu'il glane sur le littoral.
Vidéos et photos réalisées en Islande en juillet 2008 par André Guyard
Source :
http://www.oiseaux.net/oiseaux/eider.a.duvet.html
12:05 Publié dans Océanographie, Ornithologie | Tags : eider, oiseaux, somateria mollissima, islande, atlantique | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
La Conure à gros bec
 La Conure à gros bec
La Conure à gros bec
Rhynchopsitta pachyrhyncha (Swainson, 1827)
par André Guyard
La Conure à gros bec ou Perroquet des pins est une espèce d'oiseau appartenant à la famille des Psittacidae.
Ce perroquet ressemble à un ara dont il reproduit le comportement criard. Il mesure environ 38 cm. Il possède un corps robuste et trapu. Son plumage est vert avec des marques rouges sur le front, au-dessus des yeux, aux épaules et sur les culottes. Les cercles oculaires sont jaunâtres et les iris orange. Le bec est noir et les pattes grises.
La coloration rouge est moins étendue et le bec est grisâtre chez le juvénile.

La Conure à gros bec est un perroquet au gros bec noir de taille moyenne, allant jusqu'à 38 cm de longueur, au plumage vert vif avec des taches rouges sur le front, les épaules et les cuisses. Les yeux des adultes sont jaunes, tandis que les jeunes ont les yeux bruns.

Couple de conures à gros bec
La Conure à gros bec vit en zone tempérée dans des forêts de pins et de sapins, entre 1200 à 3600 mètres d'altitude. Son aire de répartition se limite à la Sierra Madre occidentale du Mexique et à la Californie.
L'espèce niche dans les cavités des arbres, occupant surtout les anciens trous de pics. Elle se nourrit surtout de graines de différentes espèces de pins, si bien que leur vie dépend de la production de cônes. D'ailleurs, la reproduction se produit au moment de la maturation des graines de pin. Ces perroquets montrent un comportement grégaire et les troupes se déplacent en fonction de l'abondance des cônes.
Conures à gros bec filmés à San Francisco
L'espèce est en voie de disparition et figure sur la liste rouge de l'UICN des espèces menacées. Ses effectifs sont estimés à seulement 1000-4000 couples. Cependant, cette espèce de perroquet indigène des États-Unis est relativement commune en captivité dans beaucoup de zoos à travers le monde. Ces oiseaux ont été réintroduits sans succès en Arizona dans les années 1980, mais cet effort s'est avéré infructueux, les perroquets étant victimes des prédateurs naturels.
Vidéo et photos : André Guyard octobre 2009 en Californie
Sources :
fr.wikipedia.org/wiki/Conure_à_gros_bec
Vidéo et photos : André Guyard
09:10 Publié dans Ornithologie | Tags : oiseaux, perroquet, conure, usa, californie, psittacidés, perroquets | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
18/03/2010
Les Iguanes dans la province caraïbe
 Les Iguanes dans la province caraïbe
Les Iguanes dans la province caraïbe
par André Guyard
Cette famille de reptiles est caractéristique de l'Amérique du Sud, de l'Amérique Centrale et de la partie sud de l'Amérique du Nord.
Les deux genres Iguana et Anolis sont bien représentés aux Antilles.
Le genre Iguana comporte deux espèces :
- Iguana Iguana est l'Iguane vert que l'on trouve en Amérique du Sud et, en ce qui concerne les Antilles, en Basse-Terre et aux Saintes ;
- Iguana delicatissima ou Iguane comestible se rencontre aux Saintes, en Grande-Terre, à la Désirade, Saint-Martin, Saint Barthélémy, Martinique, Dominique.

Iguana iguana (cliché R. Butler)
Le genre Anolis est représenté aux Antilles par quatre espèces:
- Anolis marmoratus, présent en Guadeloupe avec 11 sous-espèces ou races locales :
- Anolis roquet présent en Martinique avec 6 races locales ;
- Anolis gingivus présent à Saint-Martin et à Saint-Barthélémy ;
- Anolis wattsi rencontré à Saint-Martin et à Trinidad.

Anolis marmoratus mâle déployant son fanon
(cliché P. Nyman)
La famille des Iguanidés appartient au sous-ordre des Sauriens qu'on peut assimiler aux Lézards et à la super-famille des Iguanoïdes caractérisée par une peau écailleuse et des paupières mobiles.
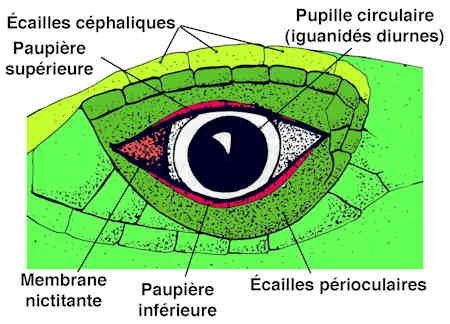
Œil d'Iguane et ses paupières
(d'après Ph. Currat)
Les Iguanidés comprennent des "Lézards" à vie terrestre et arboricole dont les membres sont terminés par des doigts munis de griffes bien développées favorisant le déplacement dans les arbustes et les arbres. La queue, plus longue que le corps, est comprimée latéralement. La langue de tous les Iguanidés est épaisse, courte et charnue.

Iguana delicatissima des Saintes (Guadeloupe)

Face dorsale de la tête d'un Iguane montrant l'emplacement de l'œil pinéal
L'œil pinéal est parfois bien visible. Il s'agit d'une vésicule, située sous la peau dans le trou pariétal du crâne au niveau de l'épiphyse. Cette vésicule limite un cristallin et une rétine à bâtonnets internes chez certains Reptiles actuels : genre Sphenodon de Nouvelle-Zélande, genres Lacerta (lézards) et Anguis (Orvets) d'Europe et peut alors être assimilée à un organe visuel. Cependant, chez la plupart des Sauriens actuels, l'œil pinéal est réduit à une vésicule sans structure oculaire.
Tous les représentants de cette famille sont mimétiques par homochromie. Plusieurs pigments dermiques leur permettent de changer de couleur et de se confondre avec le milieu (protection contre les prédateurs).
L'épiderme est protégé par des écailles épidermiques et limité à sa base par la couche germinative de Malpighi.
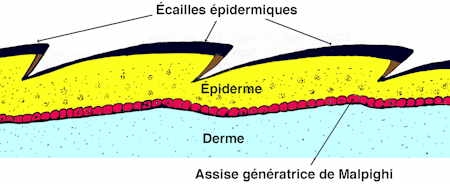
Coupe de la peau d'un Iguane montrant les écailles épidermiques
(d'après Ph. Currat)
Sous-jacent à l'épiderme, le derme, épais, contient de nombreux chromatophores à noyau central et cytoplasme ramifié, étoile, riche en pigments tégumentaires. Dans chaque chromatophore, sous l'influence de différents facteurs : illumination, stimuli visuels, chimiques, nerveux, hormonaux, les pigments peuvent soit se disperser dans le cytoplasme, ce qui a pour effet d'assombrir le chromatophore et la peau par effet de masse, soit se rassembler autour du noyau et éclaircir le chromatophore et la peau.
Chez les Iguanidés, trois types de chromatophores sont responsables des variations de coloration.
- Les lipophores ou xanthophores. Ce sont des cellules dermiques, superficielles, situées sous la couche de Malpighi. Ils contiennent des grains de pigments jaune orangé : xanthophylles-caroténoïdes et sont séparés par des gouttelettes lipidiques orangées (avec pigments jaunes ou rouges liposolubles). L'ensemble : lipophores + gouttelettes lipidiques, forme une couche pigmentaire jaune sous-épidermique.
- Les leucophores ou iridophores ou guanophores empilés sous les xanthophores, contiennent des microcristaux de guanine réfléchissant la lumière.
- Les mélanophores. Ce sont des cellules plus profondes, à cytoplasme digité très contractile qui contiennent un pigment granuleux brun-noirâtre : la mélanine. Ce pigment, normalement situé dans le cytoplasme périnucléaire, peut, dans certains cas, se disperser dans toute la cellule ou. se concentrer au maximum autour du noyau.
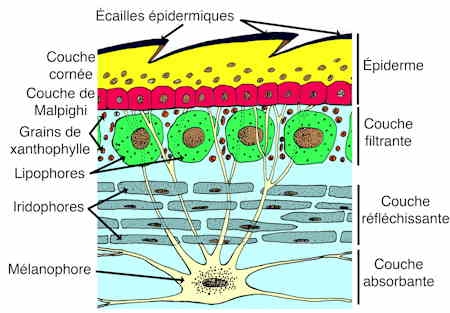
Le mécanisme de la régulation chromatique et le contrôle de cette régulation sont plus ou moins complexes suivant les espèces. En général, lorsque la lumière solaire traverse un milieu hétérogène (derme contenant les chromatophores), les radiations de grande longueur d'onde (rouges) sont absorbées; les autres radiations du spectre sont réfléchies par les guanophores, puis traversent les lipophores étalés ; les lipophores arrêtent les radiations bleues et violettes ; seul le vert est réfléchi et le saurien apparaît vert ou bleu vert lorsque lumière et chaleur ont des valeurs modérées (la teinte bleue, réfléchie, a pour origine des phénomènes d'interférence de la lumière, au niveau des cristaux de guanine, donnant une coloration irisée, et la diffraction des ondes courtes bleues en milieu hétérogène).
Cette teinte bleu vert est modifiée quand les mélanophores interviennent. S'ils se rassemblent au maximum dans les mélanophores contractés, les radiations sont peu absorbées, et les guanophores et lipophores étalés assurent la dispersion totale de la lumière avec abondance des radiations jaunes : la peau apparaît jaunâtre. Au contraire, si les granules de mélanine se dispersent dans la cellule étalée, la couleur de fond de la peau s'assombrit de même que les autres teintes : le saurien paraît gris-gris brun. En général cette livrée grise est fréquente à l'ombre ; lorsque la chaleur est excessive ou trop basse, la livrée devient brun sombre.
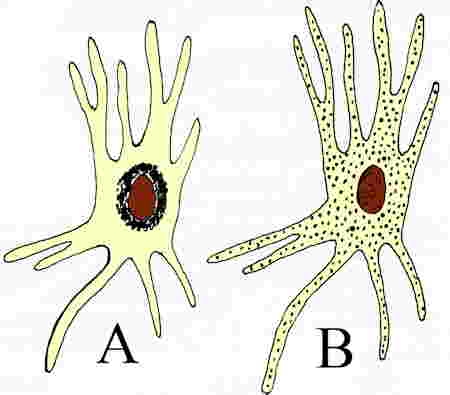
Chromatophores. A : pigment concentré (livrée claire). B : pigment dispersé (livrée sombre)
En conclusion, les changements de coloration de la livrée permettent aux Iguanidés de se dissimuler aux yeux des prédateurs et de jouer un rôle important dans la thermo-régulation.
Le genre Iguana
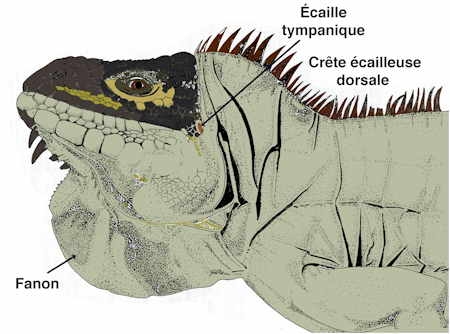
Tête d'Iguana delicatissima
(d'après Ph. Currat)
Les deux espèces d'Iguanes, présentes dans les îles et îlets antillais, sont protégées car en voie de disparition. Elles sont originaires du Nouveau-Monde, en particulier de l'Amérique Centrale tropicale. L'introduction de l'espèce Iguana iguana dans les Antilles françaises est postérieure à celle de l'espèce Iguana delicatissima. La prolifération actuelle de l'Iguana iguana met en péril la seconde espèce.

Tête d'Iguana iguana mâle
Les deux espèces vivent dans les régions basses, chaudes et sableuses, au voisinage des points d'eau ; elles ont donc des biotopes semblables mais se rencontrent rarement simultanément.

Tête d'Iguana iguana mâle avec le fanon étalé
Elles sont présentes toutes deux dans les îlets des Saintes : Terre de Haut, Ilet à Cabris, La Coche. Ailleurs, elles forment isolément, des peuplements reliques.
- En Basse-Terre, l'espèce Iguana iguana se rencontre essentiellement dans les Monts Caraïbes au Massif du Houelmont.
- À la Désirade, l'espèce Iguana delicatissima fréquente les ravines de la côte Nord et la région des Galets ; elle s'aventure rarement sur le plateau central.
- En Martinique, l'espèce Iguana delicatissima se trouve dans les forêts du Nord de l'île et sur l'îlet Chancel dans la baie du Robert.

Iguana delicatissima
Les Iguanes sont des Sauriens pouvant atteindre 1,60 m de longueur totale et peser 15 kg.
Le corps est trapu, comprimé transversalement. La tête est puissante avec deux yeux protégés par des paupières bien développées. Toute la surface du corps est couverte d'une peau écailleuse de teinte verte chez les mâles, grise chez les femelles (dimorphisme sexuel). Les deux espèces antillaises diffèrent par la disposition des plaques écailleuses autour des yeux et par la taille des écailles tympaniques : chez Iguana iguana. Les écailles tympaniques sont rondes et de grande dimension. Une crête écailleuse dorsale et caudale, formée d'épines libres et plus ou moins molles, s'étend de la tête à la queue. La face ventrale du cou porte un fanon dentelé épineux. Crête dorsale et fanon sont plus développés chez les mâles que chez les femelles (caractères sexuels secondaires permanents). La queue est longue et atteint les 2/3 du corps. Elle est garnie d'écailles souvent plus épaisses et présentent un bord coupant. - Les quatre membres pentadactyles, grêles, "hauts", sont terminés par des doigts fins et inégaux munis de griffes crochues et puissantes. Au niveau de la face interne des fémurs, chez les Iguanes mâles, des pores fémoraux rejettent une sécrétion de nature cireuse contenant des xanthophylles d'origine alimentaire.
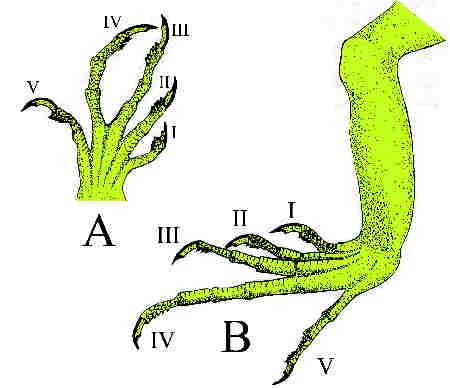
Extrémités des membres d'un Iguane
A : membre antérieur gauche, B : membre postérieur gauche
(d'après Ph. Currat)
Les Iguanes sont des Sauriens diurnes et arboricoles, localisés dans un territoire précis. Lorsqu'ils partent à la recherche de leur nourriture, ils sont guidés par leur odorat et les mouvements de leurs proies. Leur régime alimentaire peut être très varié : insectivore, carnivore - œufs et oiseaux -, mais les Iguanes sont surtout herbivores végétariens et marquent une préférence pour les fleurs, les fruits et les feuilles de Mapou (genre Cordia). En captivité, il est possible de les alimenter avec des fleurs, des fruits et de la salade.
La prise de nourriture est assurée par de fortes mâchoires munies de dents insérées sur le bord interne des maxillaires - dents à trois pointes spatulées - et par leur langue épaisse charnue, courte et large, villeuse, gluante, lobée antérieurement, et adhérente à la mâchoire inférieure par une large surface.
Le schéma ci-dessous montre le crâne d'un Iguane. À noter que maxillaire et dentaire sont munis de dents munies de trois pointes. 1 : prémaxillaire, 2 : maxillaire, 3 : nasal, 4 : préfrontal, 5 : frontal, 6 : postorbitaire, 7 : pariétal, 8 : squamosal, 9 : carré, 10 : basioccipiatal, 11 : prootique, 12 : supraoccipital, 13 : dentaire, 14 : coronoïde, 15 : supraangulaire, 16 : articulaire, 17 : angulaire.
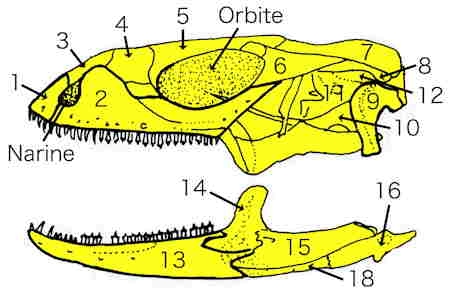
Crâne d'Iguana iguana
(d'après Ph. Currat)
Au sol, les quatre pattes grêles et hautes servent à la marche, à la course et au saut. Le mouvement des membres se fait dans un ordre déterminé : au déplacement d'une patte antérieure vers l'avant, succède le déplacement vers l'avant de la patte postérieure du côté opposé. Ainsi, lors d'un déplacement lent, trois pattes seulement reposent suc le sol pendant un court instant. Lors de la course, deux pattes seulement touchent le sol, et le tronc et la queue sont un peu surélevés. Comme chez tous les Sauriens capables de se mouvoir rapidement, la queue de l'Iguane est longue. Lors d'un saut, le corps est projeté vers l'avant ; cette projection est facilitée par les mouvements de la queue. Au-dessus du sol, la disposition et la longueur des doigts - des pattes postérieures surtout - la présence de griffes puissantes, longues et courbes, assurent une progression aisée dans les branches des arbres : l'Iguane grimpe très facilement et peut sauter d'une branche à l'autre ; la queue sert de balancier et maintient l'équilibre. Dans l'eau : l'Iguane nage avec aisance. Les points d'eau, près desquels il vit, constituent des refuges en cas de danger.
Dans leur biotope naturel, les Iguanes sont difficiles à observer du fait de leur mimétisme et de la discrétion de leurs mouvements, lents ou rapides, mais toujours silencieux.
Différents Iguana iguana observés dans le Yucatan
Les mâles, généralement inoffensifs, deviennent belliqueux au moment de la reproduction. L'accouplement a lieu en mars et la ponte se situe de mai - juin à août. Les Iguanes sont ovipares. La femelle change de biotope au moment de la ponte ; dans le sol meuble, le sable, ou un trou au pied d'un arbre, elle dépose, en une seule fois, 15 à 20 œufs ovoïdes (5 cm/ 2,5 cm) à membrane souple. L'incubation des œufs abandonnés par la femelle est fonction de la température ambiante et dure de 6 à 14 semaines. A l'éclosion, les jeunes, de couleur vert-émeraude, ont une crête dorso-caudale peu développée.
Jeune iguane en captivité
L'Iguane est un animal craintif, très vulnérable pendant la mue (mue par lambeaux) au cours de laquelle il apparaît sombre et amaigri. Ses ennemis comprennent les prédateurs naturels occupant le même biotope, et l'homme. La Mangouste dévore ses œufs ; les jeunes Iguanes sont la proie des Mammifères carnivores (Mangoustes - Chats) des Oiseaux et des Hommes, Les Iguanes adultes, comestibles, sont très recherchés, notamment Iguana delicatissima. Lorsqu'il y a danger, l'Iguane prend une teinte sombre, "siffle" et, pour se défendre, peut mordre et utiliser sa queue à écailles coupantes à la manière d'un fouet dangereux. Pour se protéger, l'Iguane s'immobilise, prend la teinte du substrat ce qui le dissimule à la vue des prédateurs ; seule la queue, pendante, de couleur gris brun, est visible. Souvent l'Iguane se déplace dans les épineux xérophiles de son biotope : acacias, campêches, orangers... Il peut fuir rapidement, s'enfouir dans des terriers profonds, sauter dans l'eau lorsqu'il est inquiété.
Note : Les Iguanes rencontrés dans les Antilles françaises diffèrent, par leur biologie et leur morphologie, des Iguanes marins des Iles Galapagos, des Iguanes à queue préhensile d'Amérique du Sud et des Iguanes de la Jamaïque.
Alors qu'ils sont communs en Amérique, les iguanes ne sont présents en Océanie que sur les archipels de Tonga et de Fidji, comment y sont-ils arrivés ? Jusqu'à présent, les biologistes privilégiaient "l'hypothèse du radeau", selon laquelle ce sont des iguanes américains qui auraient colonisé ces îles, traversant le Pacifique sur des débris végétaux. Mais pour Brice Noonan, chercheur à l'université du Mississippi, cette hypothèse ne tient plus. D'abord parce qu'un périple de près de 8000 km apparaît hautement improbable. Ensuite parce que "des éléments géologiques ont révélé que, contrairement à ce que l'on pensait jusqu'alors, ces îles ne sont pas pleinement océaniques: elles ont été rattachées à l'Asie. De ce fait, les iguanes ont pu les coloniser en marchant, il y a environ 40 millions d'années", explique-t-il. Le chercheur vient justement d'établir un arbre généalogique qui montre que les iguanes du Pacifique sont bien plus proches de ceux dont on connaît quelques fossiles en Asie que des iguanes américains. Fidji et Tonga seraient donc le dernier refuge des iguanes asiatiques, qui ont disparu depuis.
Le genre Anolis (en créole = Anoli)
Dans les Antilles françaises, les quatre espèces présentes, appartenant au genre Anolis, se subdivisent au moins en 17 sous-espèces. À la Désirade, certains spécimens ont une livrée verte ponctuée de gris. Les Anolis proviennent des régions intertropicales du continent américain.

Les Anolis sont des Sauriens sédentaires, arboricoles, nombreux dans les arbres et arbustes des régions basses et sèches, dans les zones cultivées, autour des habitations. Ce sont des sauriens de petite taille avec une queue bien développée (12 à 20 cm de longueur totale - corps + queue -, au maximum). Leur corps, comprimé est recouvert d'écailles épidermiques de petite dimension. La couleur de la livrée des Anolis est fonction de la lumière ambiante, de la température du substrat liée d'ailleurs à la luminosité et de l'humeur. La faculté de changer rapidement de couleur est en rapport, comme chez les Iguanes, avec la structure de la peau. Ces changements de teinte assurent, dans certaines limites, la régulation thermique.
Cependant, lorsque la température du substrat, plus importante que la température de l'air, s'éloigne par trop du préférendum thermique, les Anolis changent de milieu. En général, à la lumière et lorsque la chaleur est modérée, la livrée est vert vif ; la teinte s'assombrit et devient gris brun à l'ombre ou lorsque la chaleur est excessive. Chez les Anolis, le mécanisme de la régulation chromatique a fait l'objet d'études expérimentales précises et nombreuses. Il est sous contrôle hormonal et a pour point de départ la réception visuelle de la lumière :
- Une hormone sécrétée par le lobe intermédiaire de l'hypophyse : hormone mélanodispersante = hormone mélanophorodilatatrice = intermédine, provoque la dispersion de la mélanine dans les mélanophores en extension, d'où. assombrissement de la livrée.
- Une hormone antagoniste : l'adrénaline, produite par la zone médullaire des capsules surrénales, concentre la mélanine dans les mélanophores rétractés : l'action de l'adrénaline est suivie de l'éclaircissement de la peau.
Chez les Anolis, le dimorphisme sexuel se traduit dans la taille des individus et la couleur de la livrée.
- Les mâles, verts en général, présente un repli cutané extensible formant un fanon (couteau, majole ou sac gulaire) inséré sous la gorge et tendu sur un cartilage en bâtonnet médio-ventral. Le fanon est blanchâtre, plus ou moins taché ou rayé. Lorsqu'il n'est pas tendu, il apparaît vivement coloré, en rouge-orangé ou jaune, par des ptéridines, lorsqu'il est en extension. Les Anolis mâles déploient leur sac gulaire au cours de parades nuptiales, ou pour avertir et menacer les intrus pénétrant dans leur territoire.
- Les femelles, généralement plus petites que les mâles, ont une teinte plus grise et ne possèdent pas de fanon. Souvent, femelles et jeunes présentent dorsalement une ligne claire plus ou moins festonnée latéralement.

Anolis wattsi mâle

L'Anolis "maître des lieux" se place plus haut que l'intrus, et s'aplatit sur le support pour paraître plus imposant.
- II tend son fanon à plusieurs reprises, et de plus en plus vite, en signe d'avertissement et de menace.
- II effectue des mouvements de la tête, séparés par des extensions du fanon.
- Son excitation se manifeste ensuite par "des pompes" : élévation et abaissement du corps sur les quatre pattes à un rythme rapide, et des balancements d'arrière en avant et inversement.
- Enfin apparaissent les mouvements de la queue, et l'Anolis "maître du territoire", au paroxysme de l'intimidation, sort sa langue lobée et "se coiffe" d'une crête cervico-dorsale menaçante.
L'intrus réplique par le même comportement ou se retire. S'il reste, après les manœuvres d'intimidation, le conbat a lieu et le vaincu prend la fuite. De gris-cendré lors de la phase d'approche, le vaincu devenu gris-jaune bat en retraite, tandis que le vainqueur arbore une livrée d'un vert très vif.
Quand un Anolis pénètre en terrain neuf, en quête de nourriture, il signale sa présence en tendant son fanon.
Iguanidé insectivore, il chasse à l'affût et reste parfois immobile très longtemps avant de saisir ses proies. Lorsqu'il guette ses victimes, en pleine lumière, ses paupières mobiles contribuent à la fermeture du diaphragme pupillaire.
La langue, courte et large, lobée antérieurement, charnue, gluante, aide à la préhension de la nourriture: insectes (mouches et moustiques, pucerons, fourmis, termites, papillons) et arachnides. A l'occasion, l'Anolis peut consommer des fruits : mangues, bananes... et du sucre.

Anolis marmoratus mâle
(cliché R. Hoogveld)
Comme l'Iguane, l'Anolis peut se déplacer à la surface du sol soit en marche lente avec la queue appliquée contre le substrat, soit en marche rapide, course, saut avec la queue surélevée.
Il peut aussi grimper et sauter dans les branches des arbustes et sur les feuilles. Ses quatre membres pentadactyles possèdent des doigts et orteils griffus, munis de coussinets plantaires. Ces coussinets, dilatés et mous, assurent l'adhérence sur les supports lisses et verticaux. L'adaptation à la vie arboricole se manifeste surtout au niveau des membres postérieurs : les pieds très longs possèdent des métatarsiens inégaux et l'orteil externe, éloigné des autres doigts griffus, forme pince avec eux pour saisir les branches.
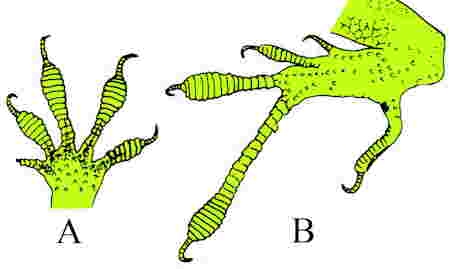
Extrémités des membres d'un Anolis
A : membre antérieur, B : membre postérieur
(d'après Ph. Currat)
Les Anolis sont ovipares. L'accouplement est précédé d'une parade nuptiale, avec extension rythmée du sac gulaire du partenaire mâle, puis mouvements du corps des deux partenaires. Le mâle saisit ensuite la femelle entre ses mâchoires - par le cou ou les flancs - et, au cours de l'accouplement, la retient grâce à l'une de ses pattes postérieures.
Les œufs sont pondus isolément ou par deux (quatre au maximum), de mai à septembre, dans la terre meuble et humide, dans l'humus, sous les feuilles mortes, puis sont abandonnés. Ils sont ovoïdes (1/2 cm de longueur) et protégés par une membrane souple. L'incubation dure de 6 à 10 semaines suivant l'espèce et la température ambiante.
Une particularité intéressante chez Anolis sagrei : les femelles de cet anoli brun ont la possibilité de choisir le sexe de leur progéniture selon la taille du père. Si le mâle est de grande taille, les petits seront mâles. Si le mâle est petit, davantage de femelles viendront au monde. Découvert par des chercheurs de l'université d'Hanover (U.S.A.), ce mécanisme permet de s'assurer que les caractéristiques avantageant les mâles comme la taille, soient bien transmises à des lézards de même sexe.
Les Anolis Sauriens anthropophiles, ont de nombreux prédateurs : Oiseaux ( Merles - Gli-gli = faucons) Mangoustes - Chats - Chiens terriers et hommes. Leur durée de vie, en liberté, ne dépasse pas un an pour 98 % d'entre eux, alors qu'en terrarium, ils peuvent vivre quatre ans.
Les Anolis sont vulnérables à l'époque des mues. Deux fois par an, la couche cornée de l'épiderme se détache par lambeaux (mue mangée par l'animal) et les Anolis moins vivaces et alertes qu'en temps normal, sont la proie de nombreux prédateurs. Les moyens de défense des Anolis sont réduits : avertissement, menace, morsure d'adversaires plus faibles. Leurs moyens de protection sont semblables, en partie, à ceux des Iguanes :
- dissimulation dans le milieu environnant = mimétisme par homochromie ;
- fuite avec ou sans autotomie caudale, (la queue régénérée, souvent de plus petite taille que la queue antérieure, peut être simple ou bifide).
- lorsque le danger ne peut être évité, les Anolis font une chute spontanée et restent immobiles, inanimés, pour feindre une mort apparente.
Sources :
Currat Ph. 1980. Reptiles des Antilles. Bulletin de l'APBG Guadeloupe. 122 p. CDDP Guadeloupe Ed.
16:51 Publié dans Herpétologie | Tags : iguane, anolis, reptiles, antilles, caraïbe, mexique, sauriens | Lien permanent | Commentaires (14) | ![]() Facebook | | |
Facebook | | |
15/03/2010
La Ciguatera aux Antilles françaises
 La Ciguatera aux Antilles françaises
La Ciguatera aux Antilles françaises
par André Guyard
Les touristes qui se rendent en bord de mer en zone intertropicale ignorent pour la plupart l'existence d'un risque encouru en consommant du poisson de mer. Dans certains cas, tout comme la population locale, ils peuvent subir une intoxication alimentaire : c'est la Ciguatera.
1. Historique
La Ciguatera est une maladie singulière provoquée par l'absorption de la chair de plus de quatre cents espèces de Poissons et d'Invertébrés marins. L'intoxication ciguatérique ou ichtyosarcotoxisme fait partie des toxi-infections alimentaires collectives (TIAC). Le nom de Ciguatera viendrait de "Cigua", un petit Mollusque vivant à Cuba et provoquant des troubles analogues.
Cette maladie est connue depuis fort longtemps ; le premier auteur l'ayant signalée fut Martyr en 1555. Christophe Colomb, Vasco de Gama, Magellan l'ont rencontrée dans les Caraïbes au XVIe siècle. Harmensen l'a signalée dans l'Océan Indien en 1601. Les marins de Fernandez de Quiros ont été intoxiqués en 1606 aux Nouvelles Hébrides : l'équipage avait pêché de nombreux poissons dont des "Pargos" (Lutjanidés) ; les matelots qui en mangèrent furent rapidement à toute extrémité. En 1675, John Locke (philosophe anglais) donna une description clinique et épidémiologique de la maladie aux îles Bahamas.
Plus récemment, le 8 mai 1949, 57 Philippins mangèrent aux îles Mariannes une très grosse murène. Tous furent très malades, onze entrèrent dans le coma et deux moururent.
Le 11 juillet 1951 à Terre de Bas (Saintes), 12 personnes de deux familles furent empoisonnées en mangeant une grosse bécune (barracuda). Les malades souffrirent beaucoup. Trois moururent et un autre devint fou trois mois plus tard.
En 1959, la Martinique a eu à déplorer quelques cas graves d'empoisonnement par des poissons pêchés à St Barthélémy.
Le 7 octobre 1960, 58 malades de l'hôpital de Pointe-à-Pitre ont été victimes d'une intoxication collective après avoir mangé de la "Vieille" en court-bouillon et en friture.
Ainsi chaque année dans les îles volcaniques et coralliennes tropicales des trois océans, plusieurs milliers de personnes sont victimes de la Ciguatera. Les Antilles françaises ne sont bien sûr pas épargnées.
Depuis 1992, la DDASS de Guadeloupe recueille, de façon hebdomadaire, les cas de TIAC par l'intermédiaire d'un réseau de surveillance sanitaire, le réseau Sentinelle.
De 1997 à 1999, 28 incidents ciguatériques impliquant 90 personnes ont été déclarés par l'intermédiaire du réseau Sentinelle. L'endémie est variable selon l'année et touche toutes les classes d'âge (46 % des cas recensés concernent les adultes de 30 à 49 ans).
2. Symptômes de la maladie
Les premiers signes d'intoxication surviennent généralement dans les 12 h qui suivent l'ingestion d'un poisson toxique. La Ciguatera est caractérisée par des effets digestifs précoces, cardio-vasculaires transitoires et neurologiques persistants. Le tableau du syndrome ciguatérique en Guadeloupe est similaire à celui observé dans d'autres îles de la Caraïbe ou en Floride avec une prédominance des signes digestifs, de l'asthénie et des paresthésies des extrémités.
Les symptômes cliniques de la Ciguatera apparaissent dans les heures suivant l'ingestion des poissons. Ils sont aussi bien gastro-intestinaux que neurologiques. Le début est marqué par des vomissements, diarrhées, crampes intestinales ; ensuite viennent des sensations alternatives de chaud et de froid, un goût amer dans la bouche, l'engourdissement de la langue et des lèvres, l'endolorissement des mâchoires avec sensation de perdre les dents, des douleurs dans les articulations, de fortes démangeaisons dans les membres et une fatigue musculaire très nette. On observe de plus une baisse de la tension artérielle, un ralentissement et une irrégularité du rythme cardiaque, une dilatation de la pupille.
Les atteintes cardio-vasculaires, (hypotension et bradycardie) ainsi que les troubles de la sensibilité comme l'inversion de la sensation de chaud et de froid interviennent également mais dans des proportions moindres. Certains signes comme le prurit et les signes neurologiques, peuvent se déclarer plusieurs jours après l'ingestion du poisson.
Dans les formes graves, on peut observer une incoordination des mouvements, des difficultés respiratoires ou urinaires, des troubles visuels. Les cas mortels sont exceptionnels et consécutifs à un état de choc cardiovasculaire.
En général l'évolution est favorable en une semaine environ, mais il n'est pas rare que les troubles de la sensibilité, les douleurs et les démangeaisons persistent plusieurs semaines et soient ravivées par toute nouvelle consommation trop hâtive de poisson même sain (hypersensibilisation). Des malaises neurodigestifs chroniques et des lésions de grattage subsistent d'où le nom de "gratte" donné parfois à l'affection. La durée moyenne de rétablissement paraît être de six mois environ.
Remarque : L'empoisonnement par la Ciguatera diffère dans ses origines comme par ses symptômes des autres sortes d'empoisonnements dus à des poissons comme les Tetraodontidae (Tetrodon sphaeroïdes), les Scombridae (thazards) ou des empoisonnements alimentaires causés par une contamination bactérienne (poissons avariés).
3. Traitements
Dans toutes les îles où sévit la Ciguatera existent des traitements locaux utilisant les propriétés de certaines plantes. Bien souvent ces médications empiriques soulagent les malades et aident à leur guérison.
Aux Antilles françaises et aux îles Vierges on utilise des infusions faites avec des feuilles de Passiflora foetida (Passifloracées), de Rhizophora mangle (Rhizophoracées), de Conocarpus erectus (Combrétacées).
Henri Stéhlé signale également des plantes efficaces comme Bontia daphnoïdes (Myoporacées), Annona muricata (Annonacées), Ricinus communis (Euphorbiacées).
La patate douce râpée crue mélangée à du lait frais et le jus de papaye donneraient aussi de bons résultats.
Pour le docteur Bagnis, chef de l'Unité Océanographique Médicale à l'institut Louis Malardé de Tahiti, les médicaments les plus efficaces sont les sels de calcium, l'atropine, les vitamines du groupe B, les antihistaminiques de synthèse et les corticoïdes dont l'indication respective est fonction des symptômes.
4. Quelques observations faites à propos de la Ciguatera
La Ciguatera est inconnue dans les zones tempérées. Les zones où l'on trouve des espèces toxiques sont nombreuses et très diversifiées (bancs coralliens, récifs barrières, lagons, etc.) mais elles sont souvent limitées.
Aux Bahamas, aux îles de la Société, les poissons de l'un des versants des îles sont beaucoup plus dangereux que ceux de l'autre côté. Les zones accores (à pente rapide) situées au vent ou à l'Est sont plus dangereuses que les zones sous le vent et peu profondes. Une zone toxique peut devenir saine après une longue période de toxicité et inversement.
La phase aiguë d'une recrudescence de Ciguatera classique couvre une période de dix à quinze ans. Les poissons toxiques sont des poissons de récif ou des poissons prédateurs de ces derniers. Les plus dangereux sont les grands prédateurs. À l'intérieur d'une même espèce, plus le poisson est gros, plus il a de chance d'être toxique. Toutes les parties du poisson n'ont pas la même toxicité, le foie et les viscères sont toujours plus toxiques que la musculature. Un poisson très frais peut être toxique. Un poisson peut être toxique à n'importe quelle époque de l'année. Le mode de préparation ou de cuisson ne modifie pas la toxicité.
5. Causes de la Ciguatera
Pendant très longtemps les causes de la maladie sont restées mystérieuses et de nombreuses croyances ont essayé de les expliquer. Certaines sont totalement fantaisistes comme celle affirmant que les vertus toxiques se développent si les poissons ont été exposés au clair de lune. Une autre, encore persistante, suppose qu'une substance chimique contamine le milieu ; le cuivre est le plus souvent impliquée probablement parce que des navires à coque doublée de ce métal ont coulé et parce que des dépôts naturels de cuivre ont été associés à des poissons vénéneux. Cette hypothèse n'explique pas pourquoi des poissons toxiques sont trouvés très loin de ces sources chimiques et pourquoi tous les poissons de la zone ne sont pas dangereux.
Ce n'est que vers 1958 que l'on a commencé à entrevoir la solution en impliquant des toxines sécrétées par des microalgues microscopiques. Les symptômes de la Ciguatera sont dus à l'imbrication plus ou moins marquée d'un mécanisme pharmacologique et d'un mécanisme immunologique résultant de l'action isolée ou conjuguée de toxines ; trois principales ont été mises en évidence.
- La ciguatoxine (C.T.X.) isolée à Hawaï dans les muscles d'une grosse murène et trouvée ensuite chez de nombreux autres poissons. Elle est très active et une dose de 0,1 pg produit des troubles chez l'Homme ;
- La scaritoxine (S.T.X.) isolée à Tahiti en 1976 chez un poisson perroquet (Scarus) est également très toxique ;
- La maitotoxine (M.T.X.) isolée en 1975 au Japon dans les viscères d'un poisson chirurgien. On ne la trouve que dans les viscères des poissons herbivores. Il semble qu'elle puisse se transformer en C.T.X.
Gambierdiscus toxicus Adachi and Fukuyo, 1979 (microalgue dinoflagellée) est l'agent causal principal de la Ciguatera dans la province caraïbe et en Polynésie française. Il a été découvert par T. Yasumoto et R. Bagnis aux îles Gambier à la fin des années 1970. Pour cette raison, les auteurs l'ont appelée Gambierdiscus toxicus.
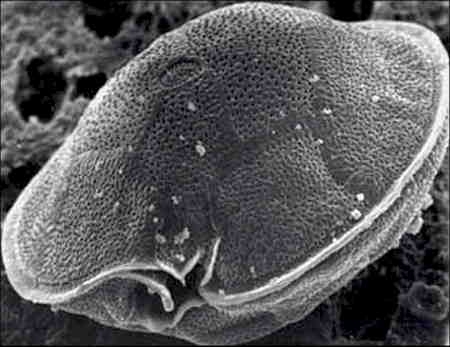
Il s'agit d'un Dinoflagellé appartenant à la classe des Dinophyceae ordre des Péridiniales, famille des Heterolacaceae. Cette microalgue était autrefois rattachée au genre Diplopsalis. D'un diamètre moyen de 80 µm, elle est enveloppée d'une thèque armée et possède une "bouche" profondément échancrée en forme d'encoche oblique, (voir photos). Les auteurs ont pu démontrer que cette microalgue était capable de fabriquer tant en milieu naturel qu'en milieu artificiel les deux toxines (CTX et MTX) responsables de la maladie. Cette microalgue unicellulaire testacée se trouve généralement attachée à des macrophytes qui prolifèrent sur les substrats coralliens morts.
À l'état endémique, l'algue existe dans la plupart des écosystèmes récifaux du Pacifique, de l'Océan indien et des Antilles, mais avec une très faible densité. Le genre Gambierdiscus est caractérisé par une circumdistribution entre 35° N et 35° S. il prolifère sur les coraux morts et les algues brunes en particulier du genre Turbinaria. Remarquons à ce propos que l'espèce Turbinaria turbinata ne se trouve aux Antilles que de la Guadeloupe à la Floride. Elle n'existe pas au Sud et ceci explique peut-être que les accidents ciguatoxiques soient plus fréquents en Guadeloupe et dans les îles du Nord qu'à la Martinique par exemple.
Gambierdiscus est endémique dans des densités relativement faibles dans la plupart des zones de Tahiti. Toutefois, des efflorescences épisodiques de ce dinoflagellé peuvent se produire, et les densités de cellules jusqu'à 10.000 cellules/g de microalgues ont été rapportées occasionnellement. Chacune de ces efflorescences contribue à maintenir un réservoir toxique riche en poison et peut être suivie par des flambées de ciguatera. Les facteurs précis de démarrage de ces efflorescences ont fait l'objet d'une enquête à long terme des populations de Gambierdiscus à Tahiti, de 1993 à 1997. La température joue un rôle important dans le cycle saisonnier de ce dinoflagellé car les populations de Gambierdiscus tendent à atteindre l'abondance maximale pendant la saison chaude (septembre à mars). La morbidité du corail, résultant soit d'événements cycloniques, des épisodes de blanchissement du corail, la pollution marine ou des activités anthropomorphiques, constitue un autre facteur critique dans la genèse naturelle des proliférations de ce dinoflagellé en créant des zones aussitôt colonisées par des macroalgues opportunistes qui sont des hôtes de choix pour les cellules de Gambierdiscus.
En revanche, Gambierdiscus toxicus prolifère énormément dans certaines circonstances, au sein des gazons recouvrant des zones coralliennes mortes. Ainsi après des tempêtes, cyclones, séismes ou par suite de travaux sous-marins en tous genres, de vastes zones de coraux morts peuvent se constituer et permettre la prolifération soudaine de la microalgue. La chaîne alimentaire de la Ciguatera est essentiellement inféodée aux poissons. Il peut cependant arriver que les Mollusques, les Crustacés, les Échinodermes soient touchés.
La toxicité des efflorescences de Gambierdiscus - exprimées en MU/1000 cellules - varie considérablement. Aucune corrélation directe n'a été établie entre cette toxicité et l'efflorescence de la biomasse cellulaire et le caractère saisonnier de divers paramètres environnementaux (température, salinité...).
Le responsable de l'intoxication est donc Gambierdiscus qui constitue la source des puissantes toxines marines vues plus haut. Le problème est que ces composés toxiques vont s'accumuler dans la chaîne alimentaire, depuis les herbivores se nourrissant sur les récifs coralliens jusqu'aux prédateurs de ces herbivores.
La consommation de poissons de récifs qui ont accumulé les divers ciguatoxines induit en quelques heures après le repas toxique, un large éventail de symptômes gastro-intestinaux, neurologiques et cardio-vasculaires. La gravité des symptômes dépend de l'espèce de poisson, du taux de ciguatoxine ingérée et de la susceptibilité individuelle. La physiopathologie est caractérisée par un ensemble de symptômes neurologiques pour lesquels les signes déterminants sont essentiellement des modifications de la sensibilité sensorielle cutanée telles que paresthésies (sur les extrémités et/ou de la zone péri-orale) et dysesthésie (inversion de la perception de chaleur et la froideur). En outre, l'ataxie, arthralgie, myalgie, vertiges, hypersalivation, des démangeaisons et une asthénie plus ou moins durables dans le temps sont des symptômes très fréquents. [Institut Malardé, Tahiti, Site Web, 2002]. Ces efflorescences de Gambierdiscus peuvent être comparées aux marées rouges entraînées par la pullulation de certains dinoflagellés planctoniques des zones tempérées qui fabriquent une variété de toxines connexes, tels que la saxitoxine et la brévétoxine.
Les toxines sont introduites dans la chaîne alimentaire par les poissons herbivores. Si la MTX reste localisée aux contenus digestifs (pour des raisons d'ailleurs inconnues), la CTX se retrouve aussi bien dans le tube digestif que le foie et les muscles des herbivores. La toxine va se concentrer par le jeu de la chaîne alimentaire : on retrouvera donc cette toxine principalement dans les poissons carnivores benthiques et pélagiques. Plus le prédateur sera gros, plus son organisme contiendra de toxines accumulées et plus il sera dangereux. On a en effet démontré qu'un poisson toxique n'éliminait pas ses toxines même si artificiellement en aquarium, on le nourrit plusieurs mois avec de la nourriture privée de substances ciguatoxiques. Ainsi, une "Bécune" (Barracuda) qui mange un "Chirurgien" absorbe dans un seul repas toute l'accumulation de toxines qu'à reçu cet herbivore pendant sa vie.
6. Précautions à prendre pour lutter contre la Ciguatera
- Protéger le milieu marin
Les agressions naturelles du milieu généralement saisonnières ou cycliques entraînent des perturbations écologiques diffuses et passagères responsables de "flambées" épisodiques de Ciguatera. En temps normal donc, seules les espèces de poissons carnivores de très grande taille ont accumulé suffisamment de toxines dans leurs tissus pour être dangereuses à consommer.
En revanche, les agressions anthropiques du milieu marin perturbent considérablement les écosystèmes coralliens. L'aménagement de ports, de marinas, de zones urbanisées, les dragages, la pollution chimique, thermique ou organique croissante, risquent à brève échéance de multiplier les zones où la microalgue toxique pourra pulluler.
- Éviter de consommer les espèces risquant d'être toxiques
D'après I. Pottier (2002), les spécimens toxiques appartiennent à quatre familles de poissons carnivores et de haut niveau trophique : carangues, pagres, mérous et barracudas. Les pourcentages de poissons toxiques pour l'homme s'élèvent à 29 % chez la Carangue gros yeux, 27 % chez la Carangue jaune, et 33 % chez la Carangue noire. Une corrélation positive entre le poids et la toxicité a été trouvée pour l'espèce Carangue gros yeux et pour les pagres toutes espèces confondues. Les poissons carnivores de petite taille appartenant à différentes espèces de Mérous ont montré une toxicité moyenne tandis que les espèces atoxiques sont
- des poissons pélagiques (les Dorades Coryphènes, les Bonites blanches et les Thons rélés),
- des petits mangeurs d'invertébrés ou des microphages,
- les bourses blanches et les vives,
- des poissons appartenant à des espèces à risque mais de petite taille,
- des poissons appartenant à des familles habituellement comestibles.

Dorade coryphène
L'arrêté préfectoral du 22 novembre 1960 interdit la consommation aux Antilles françaises des espèces suivantes :
Sphyraena barracuda : Bécune ou Barracuda.

Sphyraena barracuda
Seriola dumerili : Badiane ou fausse Carangue.

Seriola dumerili
Caranx latus : Carangue gros yeux,"Mayol".

Caranx latus
Caranx bartolomaei : Carangue jaune.

Gymnothorax funebris : Murène verte "Congre vert".

Gymnothorax funebris
Sphaeroïdes greeleyi : "Tchouf Tchouf" "Pelpète".

Sphaeroïdes greeleyi
Les espèces suivantes sont toxiques à Saint Martin et Saint Barthélémy :
Espèces déjà citées ci-dessus.
Mulloidichtys martinicus : "Barbarin blanc" "Souris".

Mulloidichtys martinicus
Scomberomorus regalis : "Thazard".

Scomberomorus regalis
Caranx ruber : Carangue à Pisquette. Carangue franche.

Caranx ruber
Caranx lugubris: Carangue noire.

Caranx lugubris
Malacanthus plumieri : "Vive".

Malacanthus plumieri
Les espèces suivantes sont parfois toxiques à Saint Martin et Saint Barthélémy :
Epinephelus morio : "Nègre" - "Vieille" - "Couronné" - "Tanche".

Epinephelus morio
Epinephelus guttatus : "Vieille rouge".

Epinephelus guttatus
Mycteroperca bonaci : "Vieille".

Mycteroperca bonaci
Mycteroperca venenosa : "Vieille à carreaux".

Mycteroperca venenosa
Echeneis naucrates : "Sucet" ou Rémora. Le rémora est ce poisson qui, grâce à sa ventouse céphalique, se fixe sur un poisson plus gros, notamment un requin.

Echeneis naucrates
Lactophrys bicaudalis : Coffre.

Lactophrys bicaudalis
Lactophrys triqueter : Coffre.

Lactophrys triqueter
Lachnolainus maximus : "Capitaine" "Aigrette".

Lachnolainus maximus
Balistes vetula : "Bourse".

Balistes vetula
- Ne jamais donner suite aux affirmations empiriques supposées distinguer les poissons toxiques des poissons sains
On ne connaît pas à l'heure actuelle aucun test simple et rapide pour détecter la toxicité des poissons ni d'ailleurs de moyens de protection efficaces des consommateurs. Les seules techniques biochimiques que l'on peut utiliser sont incompatibles avec les impératifs d'une commercialisation du poisson.
Il est toujours possible de faire un test sur un chat, mais celui-ci vomit souvent le poisson vénéneux. Par contre Banner et Boroughs ont remarqué que la mangouste est très sensible à la Ciguatera ; elle ne vomit jamais le poisson et montre des symptômes caractéristiques tels que la perte de certains réflexes et l'incoordination des membres postérieurs puis antérieurs. Un coma précède la mort de l'animal.
Quant aux moyens empiriques qui permettraient de détecter une éventuelle toxicité, ils sont très nombreux, plus ou moins fantaisistes et ne doivent pas être pris au sérieux. Citons-en quelques-uns pour mémoire.
On place un objet argenté avec le poisson pendant sa cuisson : si l'objet noircit, le poisson est toxique.
Les mouches évitent les poissons vénéneux ; si les mouches viennent, elles volent de manière désordonnée et meurent.
Si l'on incise la chair du poisson avec un couteau et que l'on arrose la partie incisée avec du jus de citron, la chair noircit si le poisson est vénéneux ; elle blanchit dans le cas contraire.
Si l'on respire profondément au niveau des ouïes du poisson, on doit éternuer si celui-ci est toxique.
- Informer les scolaires, les pêcheurs et la population en général
Les professeurs de SVT ont une mission importante à accomplir vis-à-vis de leurs élèves. En effet à propos de l'étude de la nutrition et des chaînes alimentaires, ils peuvent aisément expliquer les causes de la Ciguatera et les moyens de l'éviter en faisant reconnaître les principales espèces dangereuses grâce à des montages audio-visuels. Un rôle d'information que pourraient reprendre périodiquement les médias : presse écrite et surtout télévision.
Conclusion
Si l'on connaît maintenant l'origine et la transmission de la Ciguatera dans la nature, tous les problèmes sont loin d'être pour autant résolus et on explique encore mal la manière dont l'affection agit sur l'Homme. Les objectifs scientifiques à atteindre sont donc :
- la découverte d'un diagnostic simple, rapide et fiable de la toxicité des poissons avant leur commercialisation ;
- la mise au point d'une méthode de traitement spécifique de la maladie ;
- la prévention de l'intoxication humaine. C'est à la recherche active de ces objectifs, que s'appliquent les équipes travaillant actuellement sur la Ciguatera à Hawaï, au Japon et à Tahiti.
Bibliographie
Adachi R., and Y. Fukuyo. 1979. The thecal structure of the marine toxic dinoflagellate Gambierdiscus toxicus gen. et sp. nov. collected in the ciguatera-endemic area. Bull. J. Soc. Sci. Fish. 45:67-71.
Anderson D.M., and P.S. Lobel. 1987. The continuing enigma of ciguatera. Biol. Bull. 172:89-107.
Baden D., L.A. Fleming, and J.A. Bean. 1994. Marine toxins. In Handbook of Clinical Neurology 21:1-34.
Baden D. G., K.S. Rein, M. Kinoshita, and R.E. Gawley. 1990. Computational modeling of the polyether ladder toxins brevetoxins and ciguatoxin. In T.R.Tosteson (Ed.). Ciguatera. Polyscience Publishing, Quebec.
Bagnis R. 1972. Quand le corail se venge in Science et Vie, septembre 1980.
Bagnis R., A.M. Legrand, and A. Inoue. 1990. Follow-up of a bloom of the toxic dinoflagellate Gambierdiscus toxicus on a ringing reef in Tahiti. Pp. 98-103 in E. Graneli, B. Sundstrom, L. Edler, and D.M. Anderson (Eds.). Toxic Marine Phytoplankton. Elsevier, Amsterdam.
Ballentine, D.L., T.R. Tosteson, and A.T. Bardales. 1988. Population dynamics and toxicity of natural populations of benthic dinoflagellates in southwestern Puerto Rico. Journal of Experimental Marine Biology and Ecology 119:201-212.
Bomber, J.W., M.G Rubio, and D.R. Norris. 1989. Epiphytism of dinoflagellates associated with the disease ciguatera: substrate specificity and nutrition. Phycologia 28:360-368.
Bomber, J.W., R.R.L. Guillard, and W. G. Nelson. 1988. Roles of temperature, salinity and light in seasonality, growth and toxicity of ciguatera-causing Gambierdiscus toxicus Adachi et Fukuyo (Dinophyceae). Journal of Experimental Marine Biology and Ecology 115: 53-65.
Bomber, J.W., D.R. Norris, and L.E. Mitchell. 1985. Benthic dinoflagellates associated with ciguatera from the Florida Keys II. Temporal, spatial and substrate heterogeniety of Prorocentrum lima. Pp. 45-50 in D.M. Anderson, A. White, and D.G. Baden (Eds.). Toxic Dinoflagellates. Elsevier, New York.
De Sylva, D. 1994. Distribution and ecology of ciguatera poisoning in Florida, with emphasis on the Florida Keys. Bulletin of Marine Science 54: 944-954.
Durand-Clement, M. 1986. A study of toxin production by Gambierdiscus toxicus in culture. Toxicon 24:153-1157.
Ébroin A. 1972. Poissons venimeux et vénéneux des Antilles Françaises. Ed. Désormeaux Fort-de-France.
Faust, M.A. 1996. Dinoflagellates in a mangrove ecosystem, Twin Cays, Belize. Nova Hedwiga 112:445-458.
Gillespie, N.C., M.J. Holmes, J.B. Burke, and J. Doley. 1985. Distribution and periodicity of Gambierdiscus toxicus in Queensland, Australia. Pp. 183-188 in D.M. Anderson, A. White, and D.G. Baden (Eds.). Toxic Dinoflagellates. Elsevier, New York.
Holmes, M.J., R.J. Lewis, M.A. Poli, and N.C. Gillespie. 1991. Strain dependent production of ciguatoxin precursors (gambiertoxins) by Gambierdiscus toxicus (Dinophyceae) in culture. Toxicon 29:761-775.
Landsberg, J.H. 1995. Tropical reef-fish disease outbreaks and mass mortalities in Florida, USA: What is the role of dietary biological toxins ? Dis. aquat. org. 22:83-100.
Lawrence, D. N., R.M. Enriquez, A. Lumesh, and A. Maceo. 1980. Ciguatera fish poisoning in Miami. Journal of the American Medical Association 224:224-254.
Lewis S.J. 1992. Ciguatoxins are potent ichthyotoxins. Toxicon 30:207-211.
Morice J. 1961 Liste préliminaire des poissons vénéneux côtiers de l'île de St Barthélémy. Institut des pêches maritimes. Gustavia St Barth.
Palafax, N., L. Jain, A.Z. Pinano, T.M. Gulick, R.K. Williams, and I.J. Schatz. 1988. Successful treatment of ciguatera fish poisoning with intravenous mannitol. Journal of the American Medical Association 259:2740-2742.
Pottier I. (2002). La ciguatera aux Antilles : épidémiologie, analyse de la C-CTX-1 et étude de la diversité des ciguatoxines dans les poissons toxicophores. Université de Caen.
Randall J. 1961. Empoisonnement par des poissons tropicaux. University of Miami Florida.
Renoux G. 1982. La Ciguatera. Bull. APBG Guadeloupe 9:68-75.
Shimizu Y. 1987. Dinoflagellate toxins. In F.J.R. Taylor (Ed.). The Biology of Dinoflagellates. Blackwell Scientific Publications, Oxford.
Stauch A. 1981. La Ciguatera. Une maladie causée par l'absorption d'aliments d'origine marine. F.A.0. Port au Prince Haïti.
Steidinger, K.A. 1993. Some taxonomic and biologic aspects of toxic dinoflagellates. In I. Falconer (Ed.). Algal Toxins in Seafood and Drinking Water. Academic Press, New York.
Tindall, D.R., and S.L. Morton. 1998. Community dynamics and physiology of epiphytic/benthic dinoflagellates associated with ciguatera. In D.M. Anderson, A.D. Cembella, and G.M. Hallegraeff (Eds.). Physiological Ecology of Harmful Algal Blooms. Springer-Verlag, Berlin.
Tomas, C. 1996. An overview of toxic episodes in the Western Hemisphere. In D. Baden (Ed.). Proceedings of the Workshop Conference on Seafood Intoxications: Pan American Implications of Natural Toxins in Seafood.
Pour en savoir plus sur le web
http://www.ilm.pf/ : la page de l'Institut Louis Malardé de Papeete
http://www.com.univ-mrs.fr/IRD/atollpol/glossaire/cigua.htm
http://www.tahiti1.com/fishing/ciguatera-fr.htm
18:03 Publié dans Nature et santé, Pollution | Tags : ciguatera, poissons toxiques, ichtyosarcotoxisme, poissons tropicaux, gambierdiscus, polynésie, pacifique, atlantique | Lien permanent | Commentaires (4) | ![]() Facebook | | |
Facebook | | |


