08/06/2017
Les potentialités infinies des cellules souches
 Les potentialités infinies des cellules souches
Les potentialités infinies des cellules souches
(Dernière mise à jour : 27 juin 2018)
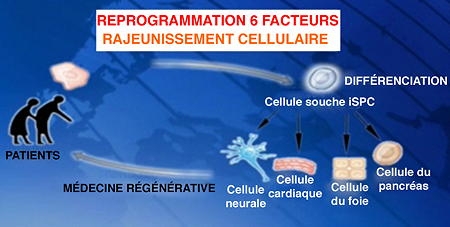
La médecine régénératrice tend à développer des techniques permettant la réparation des tissus à partir de cellules souches. Au début des années 2000, des chercheurs de l'INSERM de Montpellier ont réussi à déprogrammer des cellules adultes différenciées pour les transformer en cellules souches démontrant ainsi que le processus du vieillissement est réversible et annonçant une thérapeutique pour en corriger les pathologies.
Le corps humain représente un assemblage de 100 000 milliards de cellules, toutes dérivées d'une cellule unique l'ovule fécondé par le spermatozoïde. D'une façon schématique, chez les animaux pluricellulaires, cette cellule originelle se divise plusieurs fois donnant une masse sphérique de cellules ou blastomères (la morula) qui va se creuser d'une cavité, le blastocèle se transformant une sphère creuse (la blastula). Cette blastula va s'invaginer comme une balle de caoutchouc crevée. C'est la gastrulation qui ébauche le tube digestif. Ce germe à deux feuillets, l'un externe l'ectoderme et l'autre interne l'endoderme va se compliquer l'apparition d'un feuillet intercalé : le mésoderme. Ces trois feuillets cellulaires seront à l'origine des cellules des différents tissus et organes.
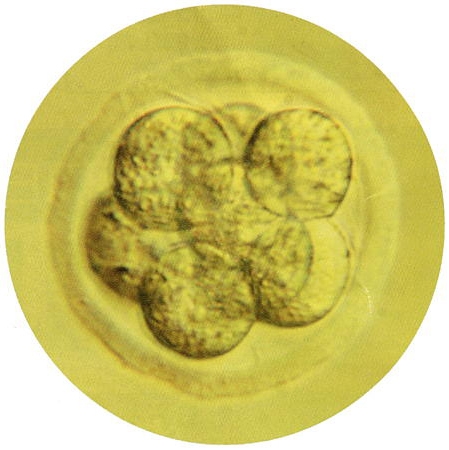
Embryon humain au début de
la segmentation (8 blastomères)
Cliché © Institut Pasteur
Trouver ICI une vidéo de l'Institut Pasteur sur les cellules souches
D'où proviennent les cellules souches iPS ?
Que se passe-t-il juste après la fécondation d'un ovule par un spermatozoïde ? Dans un article publié en septembre 2015 dans la revue "Nature communications", des généticiens de l'Institut Karolinska de Stockholm viennent d'éclairer cette étape fondamentale, et pourtant méconnue, du développement en identifiant les gènes exprimés par l'œuf fécondé lors de ses toutes premières divisions. Ils ont pour cela étudié des ovules humains tout juste fécondés et congelés, mais ne faisant plus l'objet d'un projet parental. Deux jours après la fécondation (l'embryon est alors formé de 4 cellules), seuls 32 gènes s'activent sur les quelque 23 000 de notre génome. Au troisième jour (embryon de 8 cellules), 129 gènes sont exprimés.
Parmi ces 32 gènes, certains codent directement pour des protéines, tandis que d'autres sont impliqués dans la régulation de l'expression d'autres gènes. Par exemple, le gène ZSCAN4 est fortement exprimé lorsque l'embryon ne se compose encore que de 4 cellules. On ne sera donc pas surpris lorsqu'on sait que ce gène intervient dans la mise au point des cellules souches pluripotentes induites (iPS), capables de se multiplier à l'infini et de se différencier en tout type de cellule. Cette découverte pourrait permettre d'améliorer les procédés de fabrication des iPS et de remédier aux problèmes de fertilité.
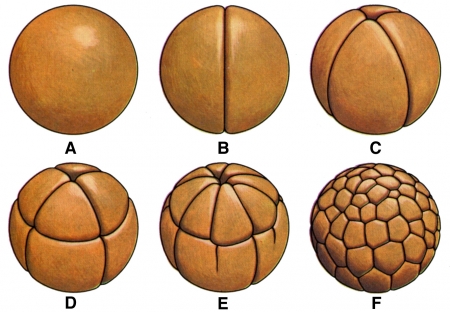
Premiers stades de la division d'un œuf d'amphibien
Schéma © Encyclopedia Universalis
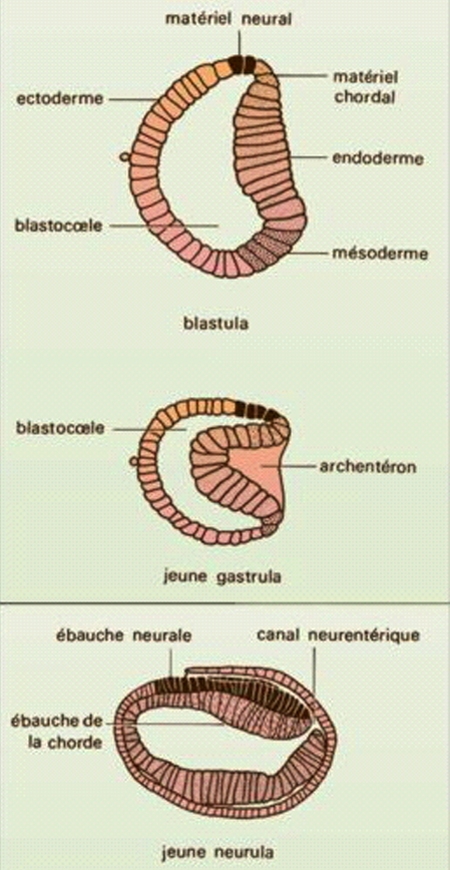
Gastrulation et neurulation chez l'Amphioxus (Procordés)
Schéma © Encyclopedia Universalis
— Le feuillet externe ou ectoderme va engendrer les cellules de l'épiderme et du système nerveux.
— Le feuillet interne ou endoderme va engendrer les cellules du tube digestif.
— Le feuillet intermédiaire ou mésoderme va engendrer toutes les autres cellules des autres organes et appareils circulatoire, respiratoire, musculaire, squelettique, cellules sanguines, etc.
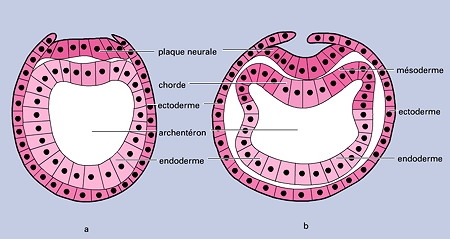
Coupes transversales d'une gastrula avec la mise en place
du mésoderme chez un vertébré
Schéma © Encyclopedia Universalis
Au total, notre corps est constitué de quelque deux cents types cellulaires différents, et ce dès la naissance. Cependant, au cours de notre vie, nos cellules vont se renouveler. De sorte que, quel que soit notre âge, la plupart de nos cellules sont plus jeunes que nous : nombre d'entre elles ont une durée de vie limitée et sont régulièrement remplacées à l'exception de certains neurones du cortex occipital. Ainsi, certaines cellules intestinales ont une durée de vie de 16 ans alors que les cellules de la paroi ne vivent que quelques heures. Le squelette est totalement renouvelé en 10 ans, un globule rouge vit quatre mois, une cellule du foie 300 à 500 jours, une cellule de l'épiderme deux semaines et une cellule de la cornée sept jours.
Qu'est-ce qu'une cellule souche ?
Il s'agit d'une cellule non différenciée et qui est apte à engendrer n'importe quelle cellule de n'importe quel tissu. Selon leur potentialité, on distingue trois types de cellules souches :
- cellules totipotentes
Cellules de l'embryon humain jusqu'à 4 jours. Les seules capables de produire un individu complet. En ce qui concerne les premiers stades embryonnaires, chaque blastomère peut être considéré comme une cellule souche embryonnaire, puisque isolément, il est capable de redonner un organisme complet.
- cellules pluripluripotentes
Présentes dans l'embryon humain entre le 5e et le 7e jour. Capables de se différencier en tous les types de cellules de l'organisme. En médecine régénératrice, elles peuvent être utilisées telles quelles (CSE). Mais on peut les produire à partir de cellules adultes reprogrammées (CSPi), soit in vitro, soit in vivo.
- cellules multipotentes
Présentes tout au long de la vie et capables de se différencier en certains types (par exemple, les cellules de moelle osseuse donnent les cellules sanguines). Chaque organe va conserver quelques cellules souches susceptibles de procéder à des renouvellements de cellules, régénérant ainsi les organes différenciés.
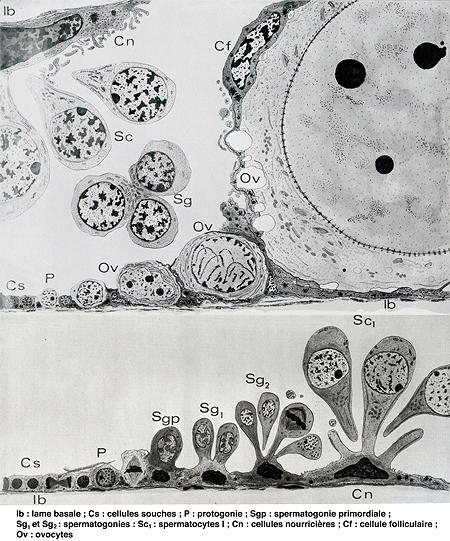
Les cellules souches de la glande hermaphrodite
d'escargot évoluent soit en spermatozoïdes soit en ovules
Schéma © André Guyard
Nichées dans différents tissus ou organes de notre corps, ces cellules souches présentent deux caractéristiques fondamentales : elles sont capables de s'autorenouveler (ainsi, notre stock de cellules souches reste constant au fil du temps) et de se différencier, c'est-à-dire de se transformer en cellules spécialisées. Et l'exploitation des potentialités de ces cellules souches ouvrent un grand espoir à la médecine dite régénératrice en palliant la disparition ou la déficience de certaines cellules du corps. Ces cellules souches adultes sont dites pluripotentes (PSC = Pluripotent Stem Cells).
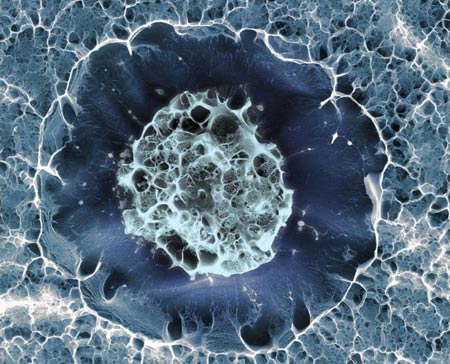
Cellule souche humaine
©Sílvia A Ferreira, Cristina Lopo and Eileen Gentleman
King’s College London
Image primée aux "plus belles photos du Wellcome Image Awards 2016"
L'image ci-dessus est celle d'une cellule souche humaine issue de l'os de hanche d'un donneur de moelle osseuse. Le diamètre de la cellule est d'environ 15 micromètres (0,015 mm).
Si l'on pouvait greffer aux diabétiques des cellules pancréatiques sécrétrices d'insuline, à un homme au cœur abîmé par un infarctus des cellules cardiaques, à un malade de Parkinson des neurones dopaminergiques, à un accidenté de la route des cellules pouvant reconstituer sa moelle épinière et lui éviter la paralysie ? C'est l'espoir d'une médecine régénératrice dopée ces dernières années par le spectaculaire développement des recherches sur les cellules souches. Et les chercheurs de l'Institut Pasteur s'emploient à explorer différentes voies thérapeutiques utilisant les cellules souches.
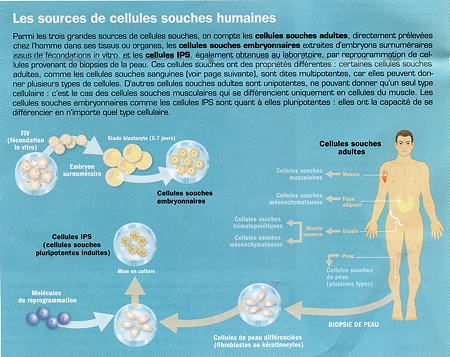
Sources de cellules souches humaines (hESC, PSC et iPSC)
Infogramme © Institut Pasteur
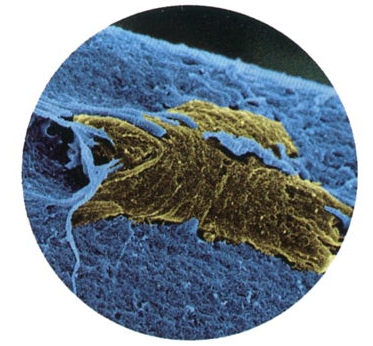
Cellule souche de muscle sur une fibre musculaire
Document © Institut Pasteur
Voir avec profit présentée par Fabrice Chrétien une vidéo définissant les cellules souches et leurs potentialités filmée à TEDxParis le 6 octobre 2012 à l'Olympia.
Issu d'un parcours à la fois scientifique et médical, Fabrice Chrétien est neuropathologiste à l'Hôpital Raymond Poincaré à Garches, Professeur d'histologie (étude des tissus biologiques) à l'Université Versailles Saint-Quentin et responsable à l'Institut Pasteur de l'unité Histopathologie humaine et modèles animaux. Ses travaux ont permis de mettre en évidence la résistance des cellules souches adultes en démontrant qu'elles pouvaient survivre chez l'homme jusqu'à 17 jours après la mort.
Voir également présentée par Laurent Alexandre cette vidéo sur l'espérance de vie filmée à TEDxParis le 6 octobre 2012 à l'Olympia.
Chirurgien et urologue de formation, Laurent Alexandre est également diplômé de Science Po, d'HEC et de l'ENA. Hyperactif et pionnier d'internet, ce coureur de marathon est le co-fondateur, dans les années 90, de Doctissimo.fr. Auteur en 2011 d'un essai intitulé « La mort de la mort », il s'intéresse aujourd'hui aux bouleversements que va connaître l'humanité conjointement aux progrès de la science en biotechnologie.
Comment déclencher la différenciation cellulaire d'une cellule souche ?
Pour amener une cellule souche à se différencier en tel ou tel type cellulaire, il faut ajouter à la culture certains facteurs comme des molécules de signalisation, c'est-à-dire en mimant les signaux moléculaires reçus par la cellule souche au cours du développement de l'organisme. Mais la nature est complexe : la différenciation d'une cellule souche implique souvent des interactions avec d'autres types cellulaires, qui, en plus, évoluent au cours du temps. Reproduire ces événements en culture est un autre grand défi. Nous ne savons pas encore, par exemple, différencier efficacement une cellule pluripotente, comme une cellule souche embryonnaire, en cellule musculaire. Des protocoles pour obtenir des cellules neuronales ou cardiaques sont en revanche mieux définis. Les défis scientifiques concernent désormais le rein, la peau, les muscles... Les expériences en cours visent à récapituler la succession des molécules de signalisation que les cellules souches pluripotentes rencontrent chez l'embryon, afin de pouvoir mimer ces événements au laboratoire.
Au-delà des cellules souches adultes
Mais pour beaucoup d'applications, la biologie des cellules souches adultes est peu connue et il reste difficile de les identifier, de les manipuler et d'obtenir leur multiplication sans qu'elles ne perdent leur caractère "souche". Il faut pouvoir les cultiver en grande quantité, chaque thérapie cellulaire nécessitant des millions de cellules. Et, s'ils sont moindres qu'en cas de greffes d'organes, les problèmes de compatibilité existent pour les transplantations de cellules d'une personne à une autre. Plusieurs alternatives sont envisagées.
— Une première méthode est l'utilisation de cellules souches prélevées sur des embryons surnuméraires de 5 jours issus de la fécondation in vitro (hESC).
Leur masse interne est alors constituée d'une centaine de cellules souches "pluripotentes" : elles ont la capacité de se différencier en tous les types cellulaires. On peut ensuite les cultiver indéfiniment et constituer des banques de cellules, dont le développement permettrait de disposer de lignées cellulaires compatibles avec de nombreux individus. Depuis l'obtention des premières cellules souches embryonnaires humaines en 1998, les recherches, très réglementées, ont permis d'apprendre à les spécialiser en cellules de la peau, du cœur, en neurones, en photorécepteurs de la rétine... mais les scientifiques n'ont pas réussi à les différencier en plusieurs autres types cellulaires. C'est l'un des grands défis du futur. Malgré ces obstacles, leur maîtrise est devenue suffisamment fiable dans certains cas pour que trois essais cliniques aient été autorisés aux États-Unis : l'un vise à utiliser chez des accidentés des précurseurs d'oligodendrocytes (cellules intervenant dans la remyélinisation de la moelle épinière) dérivés de cellules souches embryonnaires : le premier patient a déjà commencé à être traité, en octobre dernier. Deux autres essais à venir ont pour objectif la réparation de la rétine, pour une maladie rare et pour la dégénérescence maculaire liée à l'âge (un million de patients en France). Des essais se préparent aussi en France, comme celui porté par le Pr Menasché[1] (hôpital européen Georges Pompidou, Paris), qui prévoit d'utiliser des précurseurs de cellules cardiaques dérivés de cellules souches embryonnaires en vue de réparer le cœur.
— Une deuxième méthode est l'utilisation de cellules souches humaines adultes (PSC et iPSC).
Transformer une cellule de votre peau en cellule cardiaque ou en neurone est désormais possible grâce à la technologie des cellules souches pluripotentes induites (iPSC). Cette technique procède d'une véritable révolution scientifique : en 2005, le Japonais Shinya Yamanaka a réussi à "reprogrammer" une cellule spécialisée de la peau adulte, un fibroblaste, pour la faire revenir à l'état de cellule souche pluripotente, tout comme une cellule souche embryonnaire. On peut dès lors orienter de nouveau son devenir. Autrement dit, une cellule de notre peau pourrait être transformée en cellule de foie, de cœur, etc. Des chercheurs français de l'Institut de génomique fonctionnelle (Inserm/CNRS/université de Montpellier) ont réussi à redonner leur jeunesse à des cellules de donneurs âgés de plus de 100 ans, en les reprogrammant au stade de cellules souches, démontrant ainsi que le processus du vieillissement est réversible (voir plus bas). Ces cellules souches pluripotentes induites (iPSC) sont un formidable espoir pour la médecine régénératrice, et peut-être pour une médecine "personnalisée". À court terme, elles devraient déjà être très utiles comme modèles de maladies et pour tester des médicaments.
Cellules souches adultes (PSC), cellules souches embryonnaires (hESC) et cellules souches pluripotentes induites (iPSC), sont au cœur d'une recherche en pleine effervescence. Au vu des limites des greffes d'organes (manque de greffons, problèmes de compatibilité), de l'impossibilité de transplanter certains organes qui pourraient néanmoins être traités avec des cellules souches et de la possibilité, au-delà de la médecine régénératrice, d'utiliser ces cellules pour le criblage de médicaments, elles semblent les candidates idéales pour la médecine de demain.
— Une troisième méthode est la xéno-transplantation, c'est-à-dire la greffe d'organes animaux chez l'Homme. (Sciences et Avenir, n° 806 avril 2014, p. 11).
Les cellules souches pluripotentes iPs seront sources de greffes cellulaires ou même d'organes reconstitués in vitro. À l'Institut de transplantation urologie-néphrologie (Itun) de l'INSERM UMR 1064 de Nantes, un protocole clinique avec ces iPs est en cours pour le traitement de maladies héréditaires du foie. L'équipe du Pr Ignacio Anegon travaille également aussi sur la xéno-transplantation, c'est-à-dire la greffe d'organes animaux chez l'Homme.
Quels animaux pourraient nous donner leurs organes ?
Les primates sont porteurs de rétrovirus pouvant sauter la barrière des espèces. Par ailleurs, il serait éthiquement peu acceptable de disposer de fermes de primates comme réserves de greffons. Les donneurs les plus probables demeurent donc les cochons. Il y a déjà des élevages et la taille de leurs organes est compatible avec celle des nôtres. Cependant, ils ont aussi des rétrovirus endogènes (PERV), capables d'infecter les cellules humaines in vitro. C'est pourquoi, en janvier 1999, le Conseil de l'Europe avait voté un moratoire sur la xénotransplantation. Celui-ci est aujourd'hui remis en question. Car, lors d'un essai clinique néo-zélandais mené à la fin des années 1990, des centaines de patients ont reçu des cellules pancréatiques sécrétrices d'insuline porcines comme traitement du diabète de type 1 et, à ce jour, aucun signe d'infection par les PERV n'a été détecté.
Une greffe d'organes de porc ne nécessiterait-elle pas des traitements antirejet colossaux ?
En effet. notamment pour des organes très vascularisés (rein, cœur ou foie). Car les cellules endothéliales qui en tapissent les vaisseaux expriment des antigènes contre lesquels nous possédons des anticorps très actifs, provoquant un rejet hyperaigu. L'Itun a conçu des porcs transgéniques qui n'expriment pas quatre de ces antigènes. Malgré cela, il y a quand même rejet (car ce ne sont pas les seuls), mais atténué. En attendant que la recherche progresse, on peut envisager de greffer des cellules ou des tissus non vascularisés. Les résultats de l'essai en Nouvelle-Zélande sont très encourageants. La cornée ou les neurones sont aussi de bons candidats, dans cinq à dix ans.
Quelle est l'autre greffe d'avenir ?
Les chimères inter-espèces. Chez des animaux, on inactive des gènes indispensables à la génération d'un organe (on dit qu'ils sont knock-out ou KO). Puis, dans les embryons KO, on injecte des cellules souches d'une autre espèce qui vont générer l'organe. L'université de Tokyo a ainsi obtenu en 2010 des souris dotées d'un pancréas de rat et vient de produire des verrats blancs porteurs de pancréas de cochons noirs. L'Itun peut donc envisager demain des porcs générateurs de pancréas humain.
Le premier consortium français de recherche sur les cellules souches
Nommé Laboratoire d'Excellence, REVIVE, premier consortium français de recherche sur les cellules souches, regroupe quinze laboratoires de l'Institut Pasteur, une dizaine d'autres équipes (Inserm, INRA, Paris 5, Paris 6...), des cliniciens, et cinq partenaires industriels. " Grâce aux synergies qui existent entre toutes les équipes fédérées, nous espérons donner une impulsion importante à la recherche dans ce domaine», souligne Philip Avner, Directeur du département de Biologie du développement de l'Institut Pasteur, d'où a émergé REVIVE. Recherche fondamentale, médecine régénératrice, criblage de molécules d'intérêt thérapeutique, mais aussi enseignement et réflexion éthique sont au cœur du projet.
Reprogrammer les cellules différenciées en iPSC
Redonner leur jeunesse à des cellules de donneurs âgés de plus de 100 ans, en les reprogrammant au stade de cellules souches, démontre ainsi que le processus du vieillissement est réversible. Ces travaux sur la possibilité d'effacer les marques de vieillissement des cellules, publiés dans la revue spécialisée "Genes & Development" du 1er novembre 2011, marquent une nouvelle étape vers la médecine régénérative pour corriger une pathologie, note Jean-Marc Lemaître, responsable de ces recherches. Autre débouché important : mieux comprendre le vieillissement et corriger ses aspects pathologiques, selon le chercheur de l'Inserm.
Les cellules âgées ont été reprogrammées in vitro en cellules souches pluripotentes induites (iPSC) et ont ainsi retrouvé leur jeunesse et les caractéristiques des cellules souches embryonnaires (hESC) qui peuvent se différencier à nouveau en cellules de tous types après la cure de jouvence concoctée par les chercheurs.
Depuis 2007, on sait reprogrammer des cellules adultes humaines en cellules souches pluripotentes (iPSC) dont les propriétés sont similaires à celles des cellules souches embryonnaires (hESC). Mais jusqu'alors, la reprogrammation de cellules adultes se heurtait à une limite, la sénescence, point ultime du vieillissement cellulaire. L'équipe de Jean-Marc Lemaître vient de franchir cette limite.
En culture cellulaire, l'équipe de Montpellier a multiplié des cellules de la peau (fibroblastes) d'un donneur de 74 ans pour atteindre la sénescence caractérisée par l'arrêt de la prolifération des cellules. Les chercheurs ont ensuite procédé à la reprogrammation in vitro de ces cellules en ajoutant à la culture un cocktail de quatre facteurs génétiques (OCT4, SOX2, C MYC et KLF4) enrichi de deux facteurs supplémentaires (NANOG et LIN28).
Infogramme Inserm/CNRS/université de Montpellier
Grâce à ces six ingrédients, les cellules sénescentes ont retrouvé des caractéristiques de cellules souches pluripotentes de type embryonnaire.
"Les marqueurs de l'âge des cellules ont été effacés, et les cellules souches iPSC que nous avons obtenues peuvent produire des cellules fonctionnelles, de tous types avec une capacité de prolifération et une longévité accrues", explique Jean-Marc Lemaître.
Par la suite, l'équipe a testé ce cocktail sur des cellules plus âgées de 92, 94, 96 jusqu'à 101 ans.
Cellules sénescentes avant reprogrammation
Cliché © Inserm/CNRS/université de Montpellier
Ces travaux ouvrent la voie à terme à l'utilisation des cellules reprogrammées iPSC comme source idéale de cellules adultes tolérées par le système immunitaire, pour réparer des organes ou des tissus chez des patients âgés, ajoute le chercheur.
Des risques à contrôler
La propriété d'autorenouvellement - caractéristique des cellules souches - peut être dangereuse si elle n'est pas contrôlée. Le risque serait alors l'apparition de cellules souches cancéreuses. Un défi majeur pour les scientifiques aujourd'hui est de s'assurer que des cellules souches transplantées ne dérivent pas vers une prolifération anormale. Ce problème ne se pose pas avec les cellules souches isolées de l'adulte, déjà déterminées, mais avec les cellules souches pluripotentes (soit induites - les iPSC -, soit embryonnaires - les hESC-) : leur différenciation, si elle est incomplète, pourrait déclencher un mécanisme de cancérisation. De nombreux travaux visent donc à mieux maîtriser ce phénomène afin d'écarter les risques.
Sources :
La lettre de l'Institut Pasteur n° 74 sept 2011.
Lemaître J.-M. et al (2011) Genes & Development 1er nov 2011.
Cellules souches : premier essai européen
(Sciences et Avenir, janvier 2012 n° 779 p. 43).
Le premier essai clinique européen réalisé à partir de cellules souches embryonnaires humaines (hESC) sera mené en 2012 à Londres au Moorfields Eye Hospital.
Le 22 septembre 2011, l'agence du médicament du Royaume-Uni (MHRA) a en effet donné son feu vert à la compagnie américaine de biotechnologie, Advanced Cell Technology (ACT), pour tester un traitement expérimental visant à corriger une pathologie rare de la vue, la dégénérescence maculaire de Stargardt. Liée à une altération progressive de la région centrale de la rétine, cette affection de l'œil est d'origine génétique et atteint les personnes avant l'âge de 20 ans, essentiellement entre 7 et 12 ans, filles comme garçons. On estime qu'elle touche un individu sur 30 000.
Outre-Atlantique, deux essais d'ACT sont déjà en cours. L'un pour cette même affection, l'autre pour la dégénérescence maculaire liée à l'âge (DMLA). À ce jour, un seul patient a bénéficié du traitement mis au point par ACT pour la maladie de Stargardt et qui consiste en une greffe de cellules de l'épithélium pigmentaire de la rétine obtenues par dérivation de hESC. La société ACT a annoncé avoir entamé des discussions avec d'autres centres de recherche européens en vue de mener de nouveaux essais cliniques. Mais, pas en France qui interdit toujours, sauf dérogations, la recherche sur l'embryon et les hESC.
Désormais, de nombreux laboratoires travaillent pour mettre au point des thérapeutiques fondées sur les cellules souches dans tous les domaines de la médecine. Ci-dessous, un panorama remis à jour qui explore les premiers résultats obtenus.
La greffe de moelle osseuse, pionnière des thérapies cellulaire
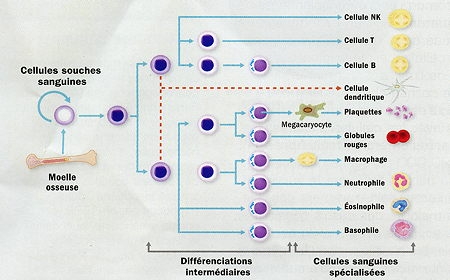
L'utilisation de cellules souches en médecine existe déjà depuis... une quarantaine d'années. En effet, la greffe de moelle osseuse permet la transplantation de cellules souches sanguines, capables de se spécialiser en une dizaine de types de cellules du sang : globules rouges, plaquettes, différents types de globules blancs.
Potentialités des cellules souches de la moelle osseuse
Infogramme © Institut Pasteur
Leucémies, lymphomes, myélomes, anémies, immunodéficience sévère de patients cancéreux après des chimio ou radiothérapies intensives... plus de 26 000 personnes bénéficieraient chaque année en Europe d'une telle greffe. Pionnière des thérapies cellulaires, elle a cependant une limite majeure : le risque de rejet du greffon en cas de mauvaise compatibilité avec le donneur. D'où l'espoir des recherches en cours sur les cellules souches sanguines.
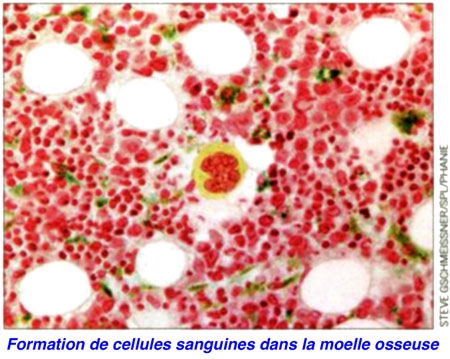
Les cellules souches sanguines permettent déjà de traiter de nombreuses maladies par greffe de moelle osseuse, et les recherches en cours pourraient rendre plus utiles encore. Ana Cumano, responsable de l'unité de Lymphopoièse à l'Institut Pasteur, a découvert leur lieu originel en 2001 chez la souris : l'artère aorte, où apparaissent au cours du développement des cellules souches sanguines immatures semblant dériver des cellules de la paroi du vaisseau. Pour Philippe Herbomel et Karima Kissa (unité Macrophages et développement de l'immunité) qui ont pu visualiser ce phénomène en 2010 dans l'embryon transparent du poisson zèbre, « il serait peut-être possible de générer des cellules souches sanguines au laboratoire à partir d'une biopsie prélevée sur les propres vaisseaux sanguins des malades ».
Cellules souches de poisson zèbre
Document © Institut Pasteur
À ce stade, les chercheurs doivent encore apprendre comment induire à partir de cellules vasculaires de l'adulte la transformation en cellules souches sanguines qui a lieu naturellement chez l'embryon. Puis à orienter leur évolution vers telle ou telle catégorie de cellule spécialisée du sang : globule rouge, globule blanc, plaquette.
Ana Cumano et son équipe s'intéressent à la production de certains globules blancs, les lymphocytes. «Déficients chez les personnes âgées - ce qui les rend plus fragiles face aux infections et mauvais répondants vis-à-vis de la vaccination -, ils ne se multiplient pas assez vite après une greffe de moelle chez les leucémiques, d'où une longue période de "lymphopénie", de six mois à un an, qui les rend extrêmement sensibles aux infections. Connaître ce qui détermine la production des lymphocytes permettrait de trouver des traitements palliant ces problèmes de déficit », explique la chercheuse. D'autres équipes tentent quant à elles de produire des globules rouges en grande quantité pour la transfusion sanguine... Les cellules souches sanguines ont incontestablement un immense potentiel médical.
Voir également sur ce même blog le myélome multiple et son traitement par autogreffe de cellules souches de la moelle osseuse.
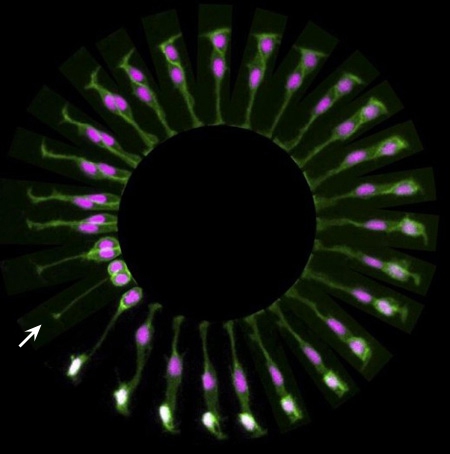
Division d'une cellule souche dans
le cerveau d'un poisson zèbre
©Sílvia A Ferreira, Cristina Lopo and Eileen Gentleman
King’s College London
Image primée aux plus belles photos du Wellcome Image Awards 2016
Le point de départ est situé à 8h (flèche blanche). Petit à petit la cellule se divise pour créer deux cellules différentes : une cellule nerveuse qui va passer du violet au blanc, et une autre cellule souche qui a la possibilité de se diviser elle-même pour produire de nouvelles cellules spécialisées. La séquence, observée en une seule image ici, dure en réalité 9 heures.
Utilisation de cellules souches sanguines en cardiologie
- Greffes de cellules souches hématopoiétiques dans les maladies coronariennes
-
Pourquoi avoir recours aux cellules souches ?
Lors d’un infarctus, des millions de cellules cardiaques meurent, privées d’oxygène parce qu’une artère s’est brusquement bouchée. En France, plus de 1,2 million de personnes souffrent d'insuffisance cardiaque, dont 250 000 à un stade avancé. Selon l’atteinte, le cœur peut finir par s’épuiser : le muscle cardiaque ne peut alors plus assurer correctement son rôle de pompe, c’est l’insuffisance cardiaque. Si elle est sévère, le seul remède est la greffe de cœur. Cette intervention lourde, et relativement rare compte tenu du manque de greffon, implique des traitements antirejet à vie. C’est pourquoi les chercheurs évaluent d’autres stratégies de prise en charge. Ils essaient notamment de remplacer les cellules cardiaques mortes par des cellules souches : des cellules indifférenciées capables de s’autorenouveler et de donner naissance à des cellules spécialisées, ici des cellules cardiaques.
L'intérêt de la greffe de cellules souches hématopoiétiques dans les maladies coronariennes se confirme grâce à une méta-analyse de 50 études regroupant au total plus de 2600 patients. C'est pour une insuffisance coronarienne chronique ou un infarctus du myocarde que ces malades ont reçu des injections intracardiaques ou intracoronariennes de cellules mononuclées de la moelle osseuse ou d'autres types de cellules. (CD 34 ou CD 133). Comparativement aux sujets non greffés, les patients traités ont une fonction ventriculaire gauche améliorée de façon prolongée (24 mois). Le risque de récidive d'infarctus du myocarde est significativement diminué ainsi que la mortalité , que celle-ci soit de cause cardiaque ou pas.
- Réparer le cœur en fabriquant un pansement cellulaire à partir de cellules souches (Science & Vie n° 1153 octobre 2013, p. 37-38)
En 2013, des chercheurs de l'université américaine de Pittsburgh ont réussi à faire pousser des cellules cardiaques humaines sur la charpente d'un cœur de souris.
Le cœur du rongeur est traité au détergent pour le débarrasser de ses cellules. N'en subsiste qu'un moule translucide composé de protéines de structure comme le collagène. Cette armature est ensuite ensemencée avec des cellules humaines préparées à partir de cellules souches, capables de donner naissance aux principaux types de cellules cardiaques. En quelques semaines, ces cellules souches recouvrent la charpente, reconstruisant le cœur dans ses moindres détails. Et ce n'est pas tout, ce cœur chimérique peut même se contracter... Sous perfusion de liquide nutritif, il bat in vitro, au rythme de 40 à 50 pulsations par minute !
Ces battements, désynchronisés, sont encore trop faibles pour pomper le sang dans les vaisseaux. Mais il s'agit d'un premier pas avant de tester cette technique pour fabriquer des pansements ou patchs cardiaques, à partir de matrices de collagène humaines repeuplées par les propres cellules des malades.
Se développe ainsi l'espoir qu'un jour, un cœur malade soit réparé par de simples rustines de muscle cardiaque cultivées in vitro, capables d'assurer localement les contractions normales de l'organe défectueux.
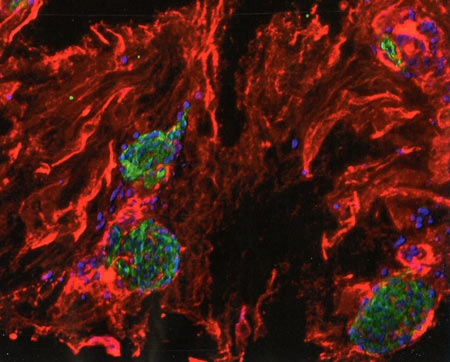
Recouvert de cellules humaines, un cœur de souris réduit à
une charpente de collagène s'est remis à battre.
- Cellules souches en thérapie régénératrice du muscle cardiaque
(par Guillaume Bayre - le 29/01/2014 Le Figaro.fr SANTÉ)
La mise sur le marché d'un traitement à l'horizon 2016 pour réparer un cœur fragilisé semble se préciser.
Des cellules souches intelligentes pour réparer un cœur fragilisé par une attaque cardiaque. Cette piste, poursuivie depuis plus d'une décennie, s'éclaircit de jour en jour avec en ligne de mire la mise sur le marché d'un traitement à l'horizon 2016.
L'autorité américaine de santé, la FDA, vient de donner son feu vert à Cardio3 BioSciences, une société biopharmaceutique belge, pour tester sur 240 patients son traitement baptisé C-Cure. Il s'agit d'un remède à l'insuffisance cardiaque d'origine ischémique, autrement dit un affaiblissement du cœur consécutif à un infarctus.
Cet essai dit de phase III représente les travaux les plus avancés dans le domaine des thérapies cellulaires pour les maladies cardiaques, qui permettraient d'éviter le recours à une transplantation. En France, le Pr Ménasché de l'Hôpital européen Georges-Pompidou ou encore la société CellProthera mènent des recherches comparables, mais à un stade un peu plus précoce.
Cardio3 a déjà débuté des tests dans plusieurs pays européens. Au total, les données concernant 500 patients seront ainsi recueillies dans l'espoir de confirmer les résultats obtenus lors d'un test à plus petite échelle, présentés l'an dernier dans la revue scientifique de l'American College of Cardiology. En phase II, une seule administration de C-Cure a conduit à une amélioration de la fonction cardiaque mesurée par la fraction d'éjection ventriculaire, qui traduit la capacité du muscle cardiaque à se contracter. La condition physique des patients s'est aussi améliorée: ils ont parcouru une distance supérieure de 20 % (+ 77 mètres) au test de marche des six minutes par rapport au groupe témoin.
C-Cure s'appuie sur une technologie, dite cardiopoïétique, issue de recherches menées à la Mayo Clinic (Minnesota) par les professeurs André Terzic et Atta Behfar. Premier avantage, il s'agit d'une thérapie dite autologue, qui élimine les risques de rejet immunitaire. Des cellules souches adultes sont prélevées dans la propre moelle osseuse du patient au niveau de la hanche, puis programmées in vitro pour devenir des cellules de lignée cardiaque. Schématiquement, les chercheurs reproduisent les signaux protéiniques qui, dans l'embryon, permettent aux cellules de se différencier en cellules d'un organe particulier. Les cellules cardioréparatrices (600 millions par administration) sont ensuite injectées dans le myocarde au moyen d'un cathéter spécialement développé. Cette opération ne nécessite aucune chirurgie cardiaque. Manipulable par un seul intervenant, le cathéter guidé par échographie est inséré via l'artère fémorale, depuis l'aine, sous légère anesthésie.
Les cellules injectées ne forment pas un matériau pour colmater les lésions cardiaques, mais elles sont capables d'induire véritablement une régénération du tissu nécrosé. « On envoie les cellules à l'école, et à la sortie elles ont appris comment remplir la fonction réparatrice cardiaque », résume le Pr Terzic, directeur du Centre de médecine régénérative de la Mayo Clinic.
- Ajout du 23 février 2015 : Des cellules souches pour le cœur
(Sciences et Avenir, mars 2015, n° 817, p. 22)
L'opération s'est déroulée en octobre 2014 mais n'a été révélée qu'en janvier 2015 : Philippe Ménasché, de l'hôpital européen Georges-Pompidou, à Paris, a essayé pour la première fois au monde d'utiliser des cellules souches cardiaques pour réparer les régions lésées du cœur chez une patiente. L'opération s'est accompagnée d'un pontage coronarien.
(Sciences & Vie, mars 2015, n° 1170, p. 33)
Pour la première fois, des médecins ont utilisé des cellules souches d'origine embryonnaire pour réparer le cœur d'une patiente souffrant d'une grave insuffisance cardiaque. L'équipe de Philippe Menasché (hôpital européen Georges-Pompidou, Paris) a déposé, au niveau de la cicatrice laissée par un infarctus, un patch couvert de cellules. Depuis l'opération, l'état de santé de la patiente s'est nettement amélioré et la zone du muscle cardiaque traitée a recommencé à battre, comme le prouve l'échographie. Cette opération inouïe a nécessité dix ans de préparation. Le temps nécessaire à Jérôme Larghero et son équipe (hôpital Saint-Louis, Paris) pour réussir à transformer les cellules souches embryonnaires en une lignée de toutes jeunes cellules cardiaques (des cardiomyocytes progéniteurs). La mise au point du patch de fibrine (sorte de colle biologique) a également nécessité de longs essais pour s'assurer de la bonne cohésion des cellules une fois posées et de leur survie. "Pour l'instant, rien ne permet de conclure que ce sont bien les cellules qui réparent le cœur, précise le Pr. Menasché. Il se peut que ce soient les substances qu'elles sécrètent". Ce qui ouvre une piste thérapeutique plus simple : administrer directement dans le cœur ce cocktail de substances.
Des greffes cellulaires pour traiter les infarctus — Le Figaro.fr SANTÉ (12 avril 2017)
Une équipe canadienne espère, grâce à des cellules-souches, pouvoir «effacer» la cicatrice laissée par un accident cardiaque.
Sous l’œil du microscope, les cellules battent la mesure dans leur boîte de Petri. Ce sont des cardiomyocytes, les cellules qui forment le muscle cardiaque. Nous sommes dans le laboratoire du Pr Gordon Keller, au McEwen Center for Regenerative Medicine, à Toronto (Canada). Ces cellules sont obtenues à partir de cellules-souches embryonnaires humaines capables de se transformer en n’importe quel type de cellules, sur commande. Il faut tout de même trouver à chaque fois la bonne "recette" pour obtenir le type désiré: mettre les bons facteurs de croissance, au bon moment, dans les bonnes conditions.
Les équipes de Gordon Keller sont particulièrement douées dans la "programmation" de cellules cardiaques. Les chercheurs parviennent à créer des lignées très "pures", c’est-à-dire présentant un type cellulaire très particulier en grande majorité. Mais à quoi servent ces cellules ? L’idée poursuivie par le Pr Michael Laflamme, venu rejoindre le laboratoire en juillet 2015, est de les injecter chez des patients victimes de crises cardiaques pour repeupler les tissus morts et limiter le risque d’insuffisance cardiaque. Pr Michael Laflamme : "Nous avons montré chez le rat, le cochon d’Inde, puis le singe que les cellules transplantées dans des cicatrices d’infarctus battaient correctement et vieillissaient bien".
Une crise cardiaque survient lorsqu’une artère alimentant le cœur se bouche. Privées d’oxygène, les cellules touchées meurent. Comme le cœur ne se régénère pas, cette cicatrice reste à vie et la zone morte ne battant plus, elle induit des contraintes plus importantes sur la déformation des parois voisines (qui doivent "se tordre" plus), provoquant leur dégradation accélérée. La cicatrice a tendance à s’agrandir. À terme, les patients victimes d'infarctus importants finissent par avoir besoin d’une transplantation.
Des travaux prometteurs
Injecter des cellules cardiaques suffirait-il à repeupler la cicatrice et prévenir le risque d’insuffisance? Les travaux chez l’animal se montrent prometteurs. « Nous avons montré chez le rat, le cochon d’Inde, puis le singe que les cellules transplantées dans des cicatrices d’infarctus battaient correctement et vieillissaient bien, détaille Michael Laflamme. Nous n’avons pas non plus observé de tumeur après un an chez le rat ou trois mois chez le singe. Mais le cœur de ces animaux bat plus vite. Nous nous tournons maintenant vers le porc, dont le cœur est plus similaire au nôtre, pour confirmer ces résultats préliminaires. »
Les premières injections chez le porc ont fait apparaître un problème: les cellules transplantées ne battent pas exactement au même rythme que les autres. « Cette arythmie est très gênante, reconnaît Michael Laflamme. Nous pensons que c’est parce que les lignées que nous avons injectées n’étaient pas assez pures et contenaient des cellules “pacemaker” qui commandent la contraction du muscle cardiaque. Je pense que c’est un problème que nous pourrons régler facilement. Mais il reste à démontrer que la “greffe” de quelques milliards de cellules (soit une seringue de 6 ml, NDLR) est suffisante pour observer des effets fonctionnels. » Il faudra encore au moins une douzaine d’essais chez le porc avant de pouvoir envisager un essai clinique chez l’homme. « Pas avant 4 à 5 ans », pronostique le chercheur. Bayer et VersantVentures ont investi 225 millions de dollars dans une nouvelle entreprise, BlueRock Therapeutics, qui vise à tester ce genre de nouvelles approches en médecine régénérative, en partenariat avec six instituts, dont le Centre Mc Ewen.
« Ce sont des travaux très intéressants, mais sur le plan clinique, je ne sais pas quel sera leur avenir », prévient le Pr Philippe Ménasché, chirurgien cardiaque à l’hôpital européen Georges Pompidou, qui a lui-même déjà greffé sur six patients des « patchs » de cellules cardiaques dérivés de cellules-souches embryonnaires. « Il faut fournir un traitement immunosuppresseur à vie aux patients pour éviter le rejet, c’est très lourd pour des personnes souvent âgées et qui présentent d’autres pathologies. » De son côté, les bénéfices des cellules greffées semblent plutôt provenir des substances qu’elles sécrètent et libèrent dans le cœur. « Nous allons donc nous contenter de libérer ces molécules lors d’un prochain essai. » Il s’agira donc plutôt d’un médicament biologique que d’une greffe cellulaire.
À Toronto, les chercheurs ont deux pistes pour lutter contre le risque de rejet. La première consiste à prélever des cellules chez le patient, de peau par exemple, à les faire « redevenir » cellules souches (on parle de cellules souches induites) avant de les cultiver pour en faire des cellules cardiaques. Le procédé est néanmoins très coûteux et complexe à encadrer sur le plan juridique. La deuxième solution consisterait à manipuler génétiquement les cellules souches embryonnaires pour les rendre « invisibles » au système immunitaire. Ce qui s’annonce aussi compliqué.
- Ajout du 8 juin 2017 :
Cellules souches : une nouvelle jeunesse pour le cœur : article de la Fondation pour la Recherche Médicale
-
Article réalisé avec le Pr Philippe Menasché, service de chirurgie cardiovasculaire de l’Hôpital européen Georges-Pompidou (AP-HP, Paris) et souvent cité dans cette note sur les cellules souches.
Une première mondiale française !
Les cellules souches embryonnaires ont la particularité d’être faciles à manipuler, qu’il s’agisse de leur culture au laboratoire ou leur transformation en cellules cardiaques. Ces cellules, issues d’un embryon, sont capables de s’autorenouveler et de donner naissance à tous les types de cellules spécialisées (peau, muscle, cœur, etc.).
Avec ces cellules souches embryonnaires, le Pr Menasché en 2014 a réalisé une première mondiale au sein du service de chirurgie cardiovasculaire de l’Hôpital européen Georges-Pompidou (Paris). Elles ont d’abord été transformées en « jeunes » cellules cardiaques (iPCS), purifiées et incorporées dans un patch selon une procédure mise au point par l’équipe Inserm du Pr Larghero de l’hôpital Saint-Louis (Paris). En octobre 2014, un tel patch a été greffé à une patiente de 68 ans atteinte d’insuffisance cardiaque sévère, à l’endroit précis où l’infarctus avait eu lieu. Un an plus tard, l’état de la patiente s’est considérablement amélioré. Quatre autres personnes devraient recevoir le même traitement, en 2016, dans le cadre d’un essai clinique. Toutefois, il existe un risque de rejet de la greffe de cellules souches embryonnaires car elles sont étrangères à l’organisme. Pour l’éviter, le patient doit prendre des traitements immunosuppresseurs (qui visent à réduire ou à supprimer la réaction immunitaire) très lourds.
D’autres travaux pour éviter le risque de rejet
Des équipes testent des greffes de cellules souches, prélevées chez le patient lui-même (greffes dites « autologues »), de sorte qu’il n’y ait aucun risque de rejet et pas de traitements immunosuppresseurs.
Greffe de cellules souches mésenchymateuses
Pour régénérer le muscle cardiaque de patients atteints d’insuffisance cardiaque sévère, le Dr Roncalli et son équipe du CHU de Toulouse réalisent des injections locales de cellules souches mésenchymateuses, prélevées dans la propre moelle osseuse des patients. Ces cellules sont capables de se différencier en cellules osseuses, cartilagineuses ou adipeuses, et probablement de participer à la formation de nouveaux vaisseaux sanguins. Chez les 10 personnes déjà traitées, les symptômes se sont améliorés : on a constaté une meilleure expulsion du sang par le cœur. Une seconde phase d’essai clinique devrait bientôt être lancée par le Dr Roncalli, incluant 90 patients dans plusieurs hôpitaux en France.
Greffe de cellules souches hématopoïétiques
En 2016, un protocole utilisant des cellules souches hématopoïétiques sera évalué chez une quarantaine de patients par l’entreprise française CellProthera. Les cellules souches hématopoïétiques sont présentes dans la moelle osseuse mais aussi dans le sang, et sont à l’origine de toutes les cellules sanguines (globules rouges, globules blancs, plaquettes). La start-up a mis au point une sorte d’automate-incubateur qui multiplie et purifie ces cellules souches, prélevées par une simple prise de sang chez le patient lui-même. Quelques semaines plus tard, elles sont réinjectées directement dans le cœur, via un cathéter passant par une artère. Ces cellules ont déjà fait l’objet d’une étude clinique préliminaire menée entre 2002 et 2005 sur sept patients, qui ont tous retrouvé « une fonction cardiaque quasi normale compatible avec une vie active » selon la start-up.
Des questions en suspens…
Durant certains essais cliniques, comme celui de l’équipe du Pr Menasché ou celui de CellProthera, un pontage est réalisé en même temps que la greffe de cellules souches. Le pontage permet de rétablir une bonne circulation sanguine grâce à une dérivation, et la greffe de cellules souches est réalisée dans l’espoir de réparer le muscle cardiaque. À l’heure actuelle, il est difficile d’évaluer la part respective de ces deux interventions dans la réparation du muscle cardiaque. Les cellules souches sont-elles directement impliquées dans la réparation du muscle cardiaque ? Pas si sûr. « Il semble que les bénéfices des cellules sont principalement liés aux substances qu’elles sécrètent. L’administration directe de ces substances, sans passer par une greffe de cellules, est donc une piste à explorer », selon le Pr Menasché.
Aussi enthousiasmantes soient ces pistes de recherche sur la réparation du myocarde, les scientifiques sont loin d’avoir fini de les défricher.
Sepsis : réparer les séquelles musculaires (ajout du 7 mars 2016)
Une greffe de cellules souches pourrait permettre de restaurer des capacités musculaires altérées à la suite d'une septicémie.
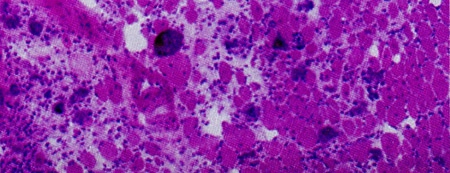
Tissu musculaire après sepsis.
Les espaces clairs entre les fibres musculaires, en rose, correspondent aux défauts de régénération du muscle.
La septicémie ou sepsis est une réponse inflammatoire généralisée de l'organisme en réaction à une infection sévère, qui touche 28 millions de personnes par an dans le monde (dont 8 millions décèdent), et laisse de graves séquelles, notamment neurologiques et musculaires. Des chercheurs de l'Institut Pasteur[1] viennent de montrer comment les cellules souches des muscles squelettiques — dites cellules satellites — sont altérées durablement après un sepsis, ce qui empêche la restauration des fonctions musculaires et conduit à un déficit musculaire persistant. Ils ont réussi à contrer ce phénomène dans des modèles expérimentaux en effectuant une greffe en intramusculaire de cellules souches dites "mésenchymateuses": ces cellules viennent assister les cellules satellites en souffrance (sans s'y substituer), qui récupèrent leur capacité à se diviser. Les chercheurs espèrent maintenant pouvoir poursuivre leurs investigations sur cette nouvelle thérapie cellulaire chez l'Homme.
[1] Unité d'Histopathologie humaine de l'Institut Pasteur, dirigée par le Pr Fabrice Chrétien, en collaboration avec le groupe de Miria Ricchetti dans l'unité Cellules souches et développement à l'Institut Pasteur, avec l'Université Paris-Descartes et le Centre hospitalier Sainte-Anne (Paris).
La thyroïde recréée à partir de cellules souches embryonnaires
(Pierre Kaldy , Sciences et Avenir n° 790, décembre 2012, p. 36.)
Une thyroïde fonctionnelle a été produite à partir de cellules souches embryonnaires par une équipe de l'Université libre de Bruxelles. Depuis la découverte de ces cellules en 1981, les chercheurs ont réussi à les faire se différencier en un grand nombre de types cellulaires différents, mais ils n'avaient pas encoure trouvé le moyen de reconstituer un organe entier et fonctionnel. La thyroïde était un candidat de choix. Cette glande, qui produit des hormones indispensables au développement et au métabolisme de l'organisme, a en effet une structure relativement simple, en forme de grappe.
L'équipe dirigée par Sabine Coslagliola ne s'est pas contentée d'induire la différenciation de cellules souches embryonnaires en cellules thyroïdiennes : elle a aussi découvert que l'addition d'une hormone, la TSH, provoquait leur regroupement en structures arrondies comparables à celles de la thyroïde. Lorsque des souris à la thyroïde déficiente ont été greffées, les taux d'hormones thyroïdiennes dans le sang sont revenus à la normale. Preuve que le greffon s'était bien substitué à l'organe défaillant pour produire une hormone fonctionnelle. Ce résultat publié dans la revue Nature ranime un espoir de traitement de l'hypothyroïdie congénitale, maladie dépistée chez près d'un nouveau-sur 3500 et dont le seul traitement est la prise à vie de l'hormone thyroïdienne.
Diabète et cellules souches (décembre 2013)
Plusieurs laboratoires se sont lancés dans la production de cellules insulinosécrétrices humaines à partir de cellules souches embryonnaires. Cela revient à recréer des îlots de Langerhans pour pallier une fonction pancréatique déficiente dans le cas du diabète de type 1. "Cela simplifierait considérablement la greffe mais le traitement antirejet resterait de mise", souligne François Pattou, chirurgien au CHRU de Lille.
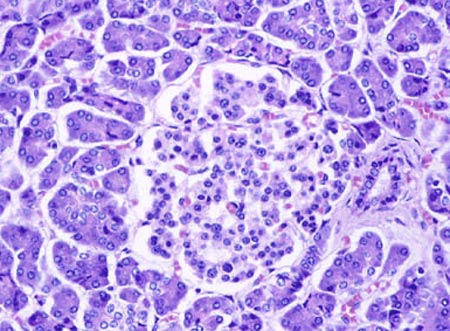
Îlot de Langerhans avec des cellules β sécrétrices d'insuline
Reconstruire la peau brûlée
Une autre utilisation médicale des cellules souches s'est développée depuis les années 80 : la reconstitution d'épiderme à partir de cellules souches de la peau pour les grands brûlés, bien maîtrisée dans certains laboratoires spécialisés.
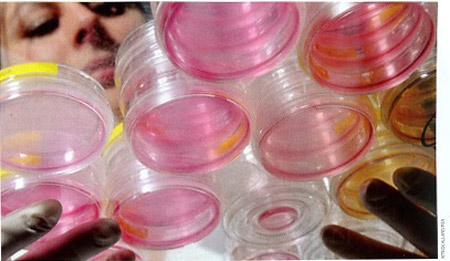
Culture de cellules souches destinées
à la régénération d'un épiderme humain
« À 80 ans, une cellule souche ne va pas avoir les mêmes propriétés qu'à 20 ans, mais elle peut avoir gardé suffisamment de capacités régénératrices. Les avancées les plus importantes en médecine régénératrice, historiquement parlant, ont concerné les cellules souches du sang, puis d'autres cellules souches ont été identifiées et utilisées comme celles de la peau. Mais une grande partie des tissus et organes n'a pas été analysée de manière assez approfondie. Dans chaque organe ou tissu, la population des cellules souches est hétérogène. Il nous faut creuser davantage, trouver d'autres marqueurs pour isoler et caractériser les cellules souches les plus intéressantes, puis les amplifier en culture sans qu'elles ne perdent leurs caractéristiques, car pour la thérapie chez l'homme, des millions, voire des milliards, de cellules sont souvent nécessaires ».
Réparer le cerveau
L'espoir de compenser les pertes de neurones liées à des maladies neurodégénératives (Alzheimer, Parkinson...) ou à des accidents vasculaires cérébraux (AVC) motive de nombreuses recherches, d'autant que deux régions du cerveau contenant des cellules souches neuronales ont été identifiées : dans l'hippocampe, en ISSB, par une équipe américaine, puis dans la "zone sous-ventriculaire", en 2003, par celle de Pierre-Marie Lledo (unité Perception et mémoire à l'Institut Pasteur). « Contrairement au dogme central de la neurobiologie, il y a donc production de nouveaux neurones dans le cerveau, et ceci quel que soit l'âge du sujet», souligne ce chercheur. « Par ailleurs, lors d'un AVC ou d'un traumatisme, de nouvelles cellules nerveuses ont été observées dans le cortex - siège de nos capacités cognitives, de notre conscience, de notre mémoire -, sans que leur origine soit établie ; le cerveau a donc des capacités d'autoréparation. » Si quelques essais de greffes de cellules souches ont été réalisés, notamment pour la maladie de Parkinson, « les résultats ont été peu probants jusqu'ici et beaucoup de scientifiques s'orientent vers d'autres pistes », ajoute Pierre-Marie Lledo. Son équipe espère pour sa part pouvoir utiliser les propres cellules souches neuronales du malade, en les déroutant et en les attirant vers les zones lésées du cerveau grâce à une "molécule-aimant". La méthode fonctionne bien dans des modèles expérimentaux, mais les neurones nouvellement implantés ne survivent que quelques semaines. Un protocole consistant à rendre les néo-neurones sensibles à la lumière - les flashs lumineux semblant alors augmenter leur durée de vie - est à l'étude.
Les cellules souches aident le cerveau à récupérer d'un AVC
(Sciences et Avenir n° 833, juillet 2016, p. 28).
Avec cette technique, sept patients sur 18 ont connu une amélioration significative de la fonction motrice.
Améliorer la rééducation de personnes victimes d'un accident vasculaire cérébral (AVC) en greffant des cellules souches dans le cerveau : c'est ce qu'a réussi une équipe de l'université Stanford (États-Unis). Dix-huit malades atteints de troubles de la motricité, sans réel espoir d'amélioration, se sont vu proposer une opération audacieuse : ouvrir le crâne pour injecter à même le cerveau, sur les zones lésées, un cocktail de leurs cellules souches. Sept d'entre eux ont connu une amélioration significative de la fonction motrice. Un patient de 71 ans a même pu se lever de son fauteuil.
« Ces résultats sont très encourageants et livrés par une équipe connue pour son sérieux. Le nombre réduit de sujets invite à la prudence, mais la stratégie est bonne », confirme Olivier Detante, neurologue au CHU de Grenoble. Il dirigera à partir de 2017 un essai européen sur 400 malades, pour mieux évaluer l'efficacité des cellules souches dans la régénération des tissus cérébraux.
Soigner les séquelles d'AVC avec des cellules souches mésenchymateuses
Source : Science & Vie n° 1187, août 2016, p. 28.
Injecter des cellules souches dans le cerveau après un accident vasculaire cérébral (AVC), pour aider le patient à récupérer ? L'idée n'est pas neuve. Depuis les années 2000, différents types de cellules ont été testés, mais sans résultat chez l'Homme. Placées dans un environnement cérébral auquel elles ne sont pas adaptées, ces cellules manquaient en effet de résistance. Une équipe américaine de l'université Stanford a peut-être trouvé la parade en utilisant des cellules souches mésenchymateuses (faciles à obtenir dans la moelle osseuse ou le tissu adipeux), qu'elle a modifiées génétiquement.
Testé sur dix-huit volontaires souffrant de troubles moteurs après un AVC, le traitement n'a provoqué aucun effet indésirable grave. Surtout, un an après l'opération, certains patients ont vu leur état s'améliorer : l'un a retrouvé l'usage d'une jambe, un autre une élocution claire. Des bénéfices qui seraient liés à la libération de substances réparatrices par les cellules souches plus qu'à un remplacement des cellules endommagées. Ces améliorations se confirmeront-elles sur d'autres patients et persisteront-elles ? Un nouvel essai sur 156 personnes démarre aux États-Unis, pour tester différentes doses de cellules souches.
Cultiver le cerveau humain ?
Un véritable exploit réalisé par une équipe autrichienne et qui a fait la une des revues scientifiques en 2013 : à partir de quelques cellules de peau prélevées sur un donneur et génétiquement "reprogrammées" au stade de cellules souches, les chercheurs ont obtenu, deux mois et demi plus tard, la réplique quasi parfaite du cerveau du donneur... tel qu'il devait être aux prémices de son développement embryonnaire, après neuf semaines de gestation. La "fabrication" in vitro de l'organe le plus complexe du corps humain, même à un stade primaire, repousse les frontières du possible. En même temps qu'elle interroge les limites de la culture d'organes (voir l'article de Aude Rambaud paru dans Science & Vie de novembre 2013 et rapporté sur ce blog).
Cellules souches et vieillissement
Avec le vieillissement de la population, on voit se développer certaines atteintes des tissus, comme la sarcopénie, une dégradation des muscles squelettiques qui a pour conséquence une perte de mobilité. Comment l'empêcher ? On peut imaginer stimuler les cellules souches des muscles du malade pour pouvoir régénérer ou réparer le tissu en dégradation. D'après Shahragim Tajbakhsh, responsable de l'Unité Cellules souches et Développement et co-coordinateur du consortium REVIVE : « À 80 ans, une cellule souche ne va pas avoir les mêmes propriétés qu'à 20 ans, mais elle peut avoir gardé suffisamment de capacités régénératrices ». L'idée est de stimuler ces cellules souches endogènes dans un contexte de maladie grave, chronique, ou lors du vieillissement, ou de reconstruire une partie du tissu en culture et d'effectuer ensuite une transplantation chez le patient. De nombreux programmes ont été lancés dans ce sens. « On sait relativement bien obtenir des cellules neuronales ou cardiaques, par exemple, à partir de cellules pluripotentes. Les défis concernent l'utilisation thérapeutique de ces cellules et l'obtention d'autres types cellulaires. »
Toujours à l'Institut Pasteur, le groupe de Delphine Bohl (Unité des Rétrovirus & Transfert Génétique, dirigée par Jean-Michel Heard) a ainsi obtenu des neurones modèles d'une pathologie neurodégénérative de l'enfant, la maladie de Sanfilippo, par mise en culture de cellules de peau de jeunes patients, modification de l'expression de trois de leurs gènes pour induire le retour à l'état de cellules souches - d'IPS -, puis ajout de molécules "d'Induction" à la culture pour provoquer la différenciation des IPS en neurones. « Ces "neurones de Sanfilippo" vont nous servir à mieux comprendre cette maladie et pourront aider au screening de molécules thérapeutiques », précise Delphine Bohl. Son groupe a également obtenu des cellules modèles de sclérose latérale amyotrophique (SLA ou maladie de Charcot), une maladie aujourd'hui incurable, aussi fréquente que la sclérose en plaques. « À partir de cellules de peau de malades, nous avons des cultures de motoneurones, cellules touchées par la SLA, qui vont permettre de classer les différentes formes de maladies, génétiques ou sporadiques, pour bien orienter le criblage de médicaments», explique la chercheuse.
Des essais en cours pour des dizaines de maladies
Aujourd'hui, les essais d'utilisation de cellules souches adultes chez l'homme, pour régénérer la cornée, l'os, le pancréas (diabète de type 1), le foie, les muscles (certaines myopathies), le cœur... concernent des dizaines de pathologies. Les succès les plus évidents ont été obtenus par une équipe italienne chez des patients atteints de brûlure de la cornée, cause de cécité. L'utilisation de leurs propres cellules souches "limbales", situées à la base de l'œil, a permis une régénération efficace de la cornée chez les trois-quarts d'entre eux, avec un recul de 10 ans.
Près de la moitié des essais cliniques avec les cellules souches vise à régénérer le muscle cardiaque partiellement détruit après un infarctus (qui touche chaque année 120 000 personnes en France). L'infarctus provoque une insuffisance cardiaque parfois telle que la survie du patient nécessite la transplantation d'un cœur sain, rarement possible pour cause de pénurie de greffons. La majorité des essais consiste à injecter dans le myocarde des cellules souches de la moelle osseuse dites "mésenchymateuses", souvent prélevées chez le malade lui-même : sans remplacer les cellules cardiaques détruites, elles semblent stimuler la réparation du cœur.
Des cellules souches contre la sclérose en plaques
Le premier essai thérapeutique à base de cellules souches prélevées sur les patients pourrait ouvrir une voie prometteuse pour soigner cette maladie neurologique très invalidante.
Le 29 mai 2013, à Gênes, lors de la 5e édition de la journée mondiale sera consacrée à la sclérose en plaques (SEP), cette maladie neurologique encore bien énigmatique. C'est en effet d'Italie que va être piloté le premier essai thérapeutique à base de cellules souches adultes. Baptisé Mesems (Mesenchymatal Stem Cells for Multiple Sclerosis), l'essai européen démarre ce printemps dans le service d'Antonio Uccelli, au département de Neurosciences de l'université de Gênes, avant de s'étendre à la France, à l'Allemagne, au Danemark, au Royaume-Uni et à l'Espagne. L'étude concernera 160 patients au total, dont 12 Français répartis dans plusieurs centres (Lille, Marseille. Toulouse, Bordeaux). Un espoir de traitement immense face à une maladie représentant la première cause de handicap non traumatique en France, avec plus de 80 000 personnes touchées, dont deux tiers de femmes, sans que cette particularité soit expliquée.
La SEP affecte les neurones, les cellules du système nerveux central, en détruisant la myéline, membrane biologique qui isole et protège les fibres nerveuses. Constituée de graisses et de protéines, cette gaine protectrice est, pour des raisons inconnues, le lieu d'une réaction inflammatoire due à une attaque par les propres cellules immunitaires du malade, les lymphocytes B et T. Cette destruction entraîne une moins bonne conduction de l'influx nerveux.
Le principal mystère que les chercheurs aimeraient lever dans cette affection auto-immune est de comprendre pourquoi le système immunitaire des malades s'emballe pour attaquer ses propres cellules nerveuses. En l'occurrence, ce sont les lymphocytes T et B — les cellules censées défendre l'organisme contre les agressions — qui détruisent peu à peu la myéline, une gaine graisseuse qui entoure les fibres nerveuses et assure la bonne propagation de l'influx nerveux. Résultat : une moins bonne transmission des messages en provenance ou à destination du cerveau, d'où une paralysie.
Ce qu'il faudrait, c'est réinitialiser le système immunitaire par une greffe de cellules souches, pour lutter contre la sclérose en plaques : des chercheurs américains de l'école de médecine de Chicago ont appliqué ce protocole début 2015, avec des résultats encourageants. Les signes cliniques de la maladie ont diminué ; un avant-goût de ce qui se profile en matière de médecine régénératrice. Demain, il sera en effet possible de réaliser des greffes sur mesure. Totalement compatibles avec l'organisme receveur, les pansements tissulaires seront constitués de cellules souches mises en différenciation en fonction de l'organe malade — un patch de cellules cardiaques, artérielles, hépatiques... — et ce, sans risque de rejet. La méthode n'a qu'un inconvénient : son prix. Car un trouble cardiaque comme l'ischémie détruit plusieurs dizaines de milliards de cellules. Combien coûterait la fabrication d'un « patch cellulaire » personnalisé d'une telle taille ? Personne pour le moment ne se risque à le chiffrer. Tout porte à penser que les greffes de cellules souches seront réservées aux plus fortunés.
Les hormones thyroïdiennes régulent les cellules souches neurales (mai 2012)
L'équipe de Barbara Demeneix, du laboratoire « Évolution des régulations endocriniennes » (Muséum national d'Histoire naturelle/CNRS), vient de mettre en évidence un nouveau rôle des hormones thyroïdiennes dans la régulation des cellules souches neurales chez la souris adulte.
Ces résultats montrent l'importance de la régulation endocrinienne dans l'homéostasie de la niche neurogénique. Essentielles pour le développement du cerveau, les hormones thyroïdiennes peuvent causer le crétinisme chez l'enfant si elles sont produites en quantités insuffisantes. Les chercheurs ont étudié le lien entre les hormones thyroïdiennes et la neurogenèse chez la souris adulte. Leurs résultats montrent que l'expression de Sox2, gène clé impliqué dans la physiologie des cellules souches neurales, est directement régulée par les hormones thyroïdiennes dans une des niches neurogéniques du cerveau adulte. Ces travaux parus dans la revue Cell Stem Cell., devraient à terme permettre de mieux comprendre certains troubles neurologiques associés à l'hypothyroïdie chez l'adulte ou la personne âgée.
Cellules souches post-mortem : un état dormant pour mieux revivre... plus tard (juin 2012)
Des chercheurs de l'Institut Pasteur, de l'université de Versailles Saint-Quentin-en- Yvelines, de l'AP-HP et du CNRS, dirigés par Fabrice Chrétien en collaboration avec Shahragim Tajbakhsh ont démontré pour la première fois, chez l'Homme et chez la Souris, la faculté qu'ont des cellules souches de demeurer dans un état de dormance quand leur environnement devient hostile, y compris plusieurs jours après la mort de l'individu. Cette capacité à considérablement réduire leur activité métabolique leur permet de préserver leur potentiel de division cellulaire pour favoriser la réparation et la croissance d'un organe ou d'un tissu quand les conditions du milieu redeviennent favorables. Cette découverte laisse envisager des perspectives thérapeutiques pour de nombreuses maladies. Cette publication est parue dans la revue Nature communications.
Des cellules souches pour réparer l'os
En 2012, l'Inserm a mis au point une technique qui est actuellement testée sur des patients souffrant de fractures non consolidées. De la moelle osseuse est prélevée, puis les cellules souches qu'elle contient sont mises en culture. Elles sont ensuite déposées sur une prothèse en céramique, greffée au niveau de la fracture. Résultats de l'essai dans un à deux ans. Une autre technique prometteuse : voir ci-dessous.
Le projet Reborne : cellules souches pour réparer les fractures osseuses (2 septembre 2014)
En injectant au niveau de la fracture un mélange de granulés de phosphate de calcium et des cellules souches adultes provenant du patient lui-même, Pierre Layrolle directeur de recherche au Laboratoire de physiopathologie de la résorption osseuse (université de Nante/Inserm), a réussi à consolider l'os réfractaire à une simple greffe de tissu osseux. C'est l'objet du projet Reborne.
Les cellules souches choisies sont des cellules souches mésenchymateuses présentes dans la moelle osseuse. Leur concentration étant trop faible à l'état naturel (environ 100 000 cellules souches dans une ponction de 10 à 30 ml de moelle osseuse), elles sont cultivées en laboratoire. Au bout de vingt et un jours, elles sont alors 400 millions, prêtes à être injectées au cœur de la fracture.
Les granulés de phosphate de calcium constitue un biomatériau qui va former une matrice, un échafaudage qui facilite la colonisation cellulaire. Il comble le vide puis, au fur et à mesure que les cellules souches s'installent, il se résorbe pour laisser place à un os tout à fait naturel.
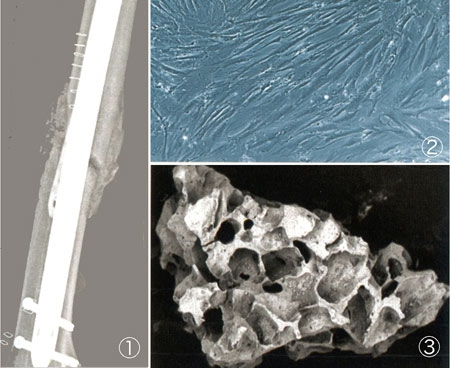
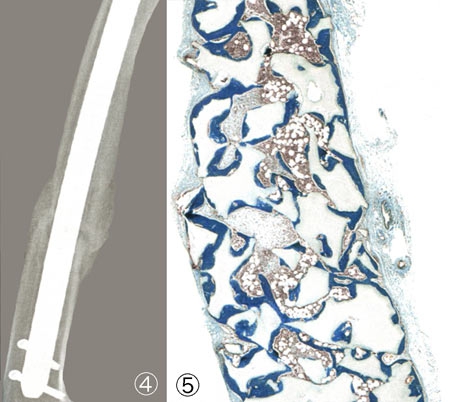
Consolidation d'une fracture par cellules souches
Fracture non consolidée (1) traitée par un mélange de cellules souches (2) et d'un biomatériau à base de granulés de phosphate de calcium (3). Six mois après, l'os est réparé (4) : il s'est régénéré (5) : os coloré en bleu-vert, moelle osseuse colorée en rose.
Dans le cadre du projet Reborne, les chercheurs testent également cette association cellules souches-biomatériau en chirurgie maxillo-faciale. "Chaque année en France, entre 200 000 et 400 000 patients reçoivent un implant dentaire. Or, dans 30 % des cas, le capital osseux n'est pas suffisant pour supporter cet implant. Cela nécessite alors une greffe osseuse qui n'est pas toujours possible, notamment chez les patients âgés ", indique Pierre Layrolle.
Un autre essai clinique teste l'injection de cellules souches, cette fois sans le biomatériau, dans le traitement de la nécrose de la tête fémorale. Un problème qui touche 50 000 Français par an. Déjà, pour soigner ces patients, la moelle osseuse est appelée en renfort. "Mais il s'agit simplement de la prélever, puis d'en injecter directement les cellules souches dans la tête de fémur du patient ", détaille le biologiste.
Évidemment, cette procédure ne permet d'obtenir qu'un nombre limité de cellules. Avec sa technique de mise en culture et de multiplication cellulaire en laboratoire, Pierre Layrolle espère donc offrir aux patients de meilleures chances de guérison.
Avant de commencer leurs essais, les chercheurs ont franchi un premier obstacle de taille. "Dès lors que la moelle osseuse sort du bloc opératoire pour rejoindre le laboratoire où elle est amplifiée, les cellules souches deviennent un médicament. Elles sont alors soumises à un ensemble de réglementations très strictes auxquelles le projet Reborne a dû se conformer ", explique Pierre Layrolle.
Cette conformité aux règles européennes est aujourd'hui l'une des forces du projet. En effet, d'autres essais associant cellules souches et biomatériaux ont déjà eu lieu dans le monde - le premier dans les années 1990 en ex-URSS. Mais chaque fois, les grands espoirs nés des expériences en laboratoire se sont fracassés sur la réalité du bloc opératoire... et des exigences de sécurité et de reproductibilité. Même si certaines équipes ont publié des résultats positifs, leurs procédures n'ont jamais pu être reproduites. Depuis, elles ont d'ailleurs jeté l'éponge.
Reste la question du coût. Guy Dacuisi, spécialiste des biomatériaux et des substituts osseux à l'université de Nantes, le reconnaît, la technique coûte cher. "Environ 20 000 euros par patient", précise-t-il. Un coût qui pourrait toutefois diminuer, selon Pierre Layrolle, si l'on utilisait non plus les cellules du patient, mais celles d'un donneur. "A l'avenir, on pourrait disposer de banques de cellules dans lesquelles on puiserait à l'envi pour soigner les patients", imagine-t-il.
Cela complique la procédure, et plus encore les dispositions réglementaires à prendre. Mais demain, appeler sa banque de cellules pour un déficit osseux sera peut-être la règle.
Quant aux cellules souches mésenchymateuses du projet Reborne, elles ont déjà servi à traiter, avec succès, une dizaine de patients victimes de graves brûlures cutanées induites par des rayonnements ionisants. Des accidents rares, mais qui conduisent souvent à l'amputation.
Source :
Hancok Coralie (2014).- Cellules souches : elles réparent même les fractures., Science & Vie n° 1164, septembre 2014, pp. 102-105.
À consulter : le site du projet Reborne (financé par la Commission européenne)
Des cellules souches créées à partir d'urine (Sciences et Avenir n° 792, février 2013, p. 38.)
Fabriquer des cellules souches à partir d'échantillons d'urine, c'est possible ! Des biologistes chinois de l'Institute of Biomedicine and Health de Canton avaient publié le concept en 2011 ; aujourd'hui, ils dévoilent le détail de leur méthode dans Nature. L'équipe a prélevé dans les urines de trois donneurs des cellules epithéliales d'urètre et de rein. Puis, après les avoir mises eu culture deux semaines durant, elle les a infectées avec des rétrovirus chargés de les reprogrammer, s'inspirant des travaux du Japonais Shinya Yamanaka, prix Nobel 2012 de physiologie.
Les cellules se sont alors « dédifférenciées » pour devenir des cellules souches pluripotentes induites (Induced Pluripotent Stem cells ou iPS, capables de donner de nouveau tous les types cellulaires. L'équipe chinoise a ensuite démontré que ces iPSc pouvaient se transformer en cellules du système nerveux, du foie ou du cœur. « L'intérêt de cette méthode est de ne pas êtreinvasive, commente Mathilde Girard, chargée de recherche à l'Institut des cellules souches (Evry). Elle est plus simple à mettre en œuvre que les méthodes actuelles (prélèvement de peau, sang ou cheveux...).»
Reste à vérifier que ces cellules, pour leur utilisation médicale, ne présentent pas d'anomalies. « Celles-ci peuventêtre chromosomiques, épigénétiques ou ou ponctuelles. Il semble que les méthodes de reprogrammation anciennes - par rétrovirus - engendrent davantage d'anomalies que les techniques plus récentes. » Les chercheurs devront apporter la preuve de l'innocuité de la reprogrammation.
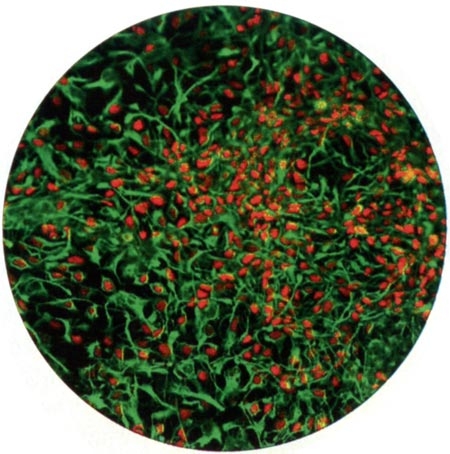
Cellules neuronales en culture dérivées de cellules prélevées dans l'urine humaine
Cellules souches et greffe de trachée (ajout du 5 mai 2013)
La première personne à avoir reçu une trachée artificielle recouverte de cellules souches, dans un hôpital suédois en juin 2011, se porte bien et d'autres greffes du même type ont été réalisées avec succès.
Le receveur, un Erythréen de 36 ans, "se porte très bien depuis quatre mois et a pu reprendre une vie normale", a expliqué le professeur Tomas Gudbjartsson, un des coauteurs de l'étude dans la revue britannique. A l'issue d'une opération de douze heures et après deux mois de séjour à l'hôpital puis dans un centre de réhabilitation, cet homme marié et père de deux enfants a pu reprendre ses études en géophysique à l'université de Reykjavik en Islande.
Une autre greffe de même type vient d'être réalisée par le Pr Paolo Macchiarini et son équipe de l'hôpital universitaire Karolinska de Huddinge, près de Stockholm, sur un Américain de 30 ans qui souffrait, comme dans le premier cas, d'un cancer des voies respiratoires. La deuxième greffe utilise une structure composée de nanofibres et par conséquent "représente une avancée supplémentaire" par rapport à la première intervention, a déclaré le Pr Macchiarini, cité par The Lancet. La trachée artificielle est fabriquée sur mesure avec des fibres de plastique recouvertes de cellules souches extraites de la moelle osseuse du patient. La même technique peut être adaptée pour concevoir des bronches artificielles.
Une troisième greffe avec la même technique a permis de traiter en avril 2013 un bébé sud-coréen âgé de treize mois seulement. "Nous allons continuer à améliorer la technique en médecine régénérative pour les greffes de trachées et allons l'étendre aux poumons, au cœur et à l'œsophage", commente le Pr Macchiarini.
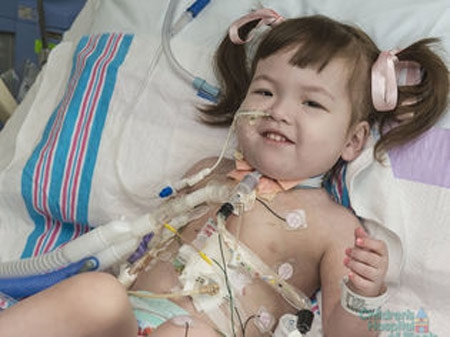
La petite coréenne Hannah Waren après son opération
© 2013 OSF Saint Francis Medical Center, Peoria, Illinois. Jim Carlson, Photographer.
Ce procédé repose sur une structure synthétique faite sur mesure dans laquelle sont "insérées" des cellules souches du patient. Il a l'avantage de ne pas dépendre d'un don d'organe et, grâce aux cellules souches du malade, permet d'éviter le phénomène de rejet. Cette technique est radicalement différente de celle également innovante, dévoilée fin 2010 par une équipe de chirurgiens français, qui utilise des morceaux de peau et fragments de côtes des malades pour reconstruire la trachée.
Cellules souches et cartilage
Le premier implant destiné à régénérer à la fois le cartilage et l'os, réparant ainsi l'ensemble de l'articulation, est en passé d'être testé en France par l'Inserm juillet 2016). II est composé d'une membrane dotée de nanoréservoirs remplis de facteurs de croissance et d'une couche d'hydrogène renfermant des cellules souches destinées à se différencier en cellules du cartilage.
Cellules souches et rein
Le rein artificiel n'existe pas encore, mais, en 2015, des chercheurs de l'université Jikey, à Tokyo (Japon), ont réussi à réaliser des reins à partir de cellules souches humaines capables de filtrer le sang et d'excréter de l'urine. Ils ont été testés chez la souris et le cochon. Le passage à l'homme prendra encore des années.
Métastases : des cellules souches impliquées (Sciences et Avenir n° 787, septembre 2012)
Des cellules souches cancéreuses ont récemment été identifiées dans plusieurs tumeurs solides (cancer du cerveau, du sein, du colon, de l’intestin…) et dans les leucémies. Elles sont à l’origine de la transformation de cellules saines en cellules tumorales et elles semblent aussi être à l’origine des métastases et de la récidive de certains cancers.
En effet, des travaux récents ont montré que seul un petit groupe de cellules était responsable de la croissance d'une tumeur (elles représentent moins de 0.1% de la population totale des cellules qui composent une tumeur). Ces cellules souches cancéreuses sont capables comme les cellules souches saines, de s’auto-renouveler, mais elles sont aussi capables de générer des cellules tumorales. Elles pourraient donc jouer un rôle direct dans le développement des cancers.
Certaines tumeurs, si ce n’est toutes, seraient donc composées à la fois de cellules tumorales qui se divisent de manière anarchique et de cellules souches cancéreuses. Ces dernières sont présentes en de très faibles proportions dans les tissus ce qui rend difficile leur étude et sont le plus souvent au repos. Elles échappent donc aux traitements anticancéreux qui ciblent les cellules qui se divisent rapidement, ce qui expliquerait la récidive de certains types de cancers à arrêt du traitement.
Les thérapies actuelles traitent toutes les cellules cancéreuses de la même façon. Le défi des prochaines années, sera de mettre au point des traitements capables d’éliminer les cellules souches cancéreuses sans toucher aux cellules souches normales de l’organisme.
Comprendre comment fonctionnent ces cellules souches cancéreuses est essentiel, et permettra de mettre au point des traitements plus efficaces.
Une étape très importante dans la compréhension de la formation des cancers vient d'être franchie : trois études indépendantes, publiées dans les revues Nature et Science, accusent de concert un même responsable dans la genèse de la croissance tumorale : les cellules souches cancéreuses (CSC). Celles-ci seraient non seulement à l'origine de la croissance d'une tumeur, mais permettraient aussi d'expliquer l'apparition de métastases. Autrement dit, la survie passée inaperçue de quelques cellules malignes pourrait à elle seule entraîner la résurgence d'un cancer.
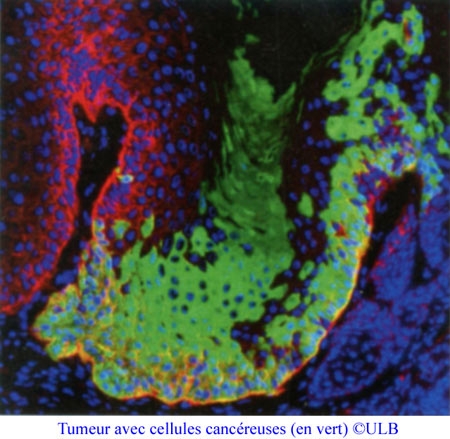
Les trois études, menées chez la souris, ont permis d'identifier des cellules souches cancéreuses dans des tissus tumoraux de l'intestin, du cerveau et de la peau. Trois preuves qui valident l'existence des CSC. Les chercheurs supposent que de telles cellules seront découvertes dans tous les types de tumeurs.
Les perspectives sont immenses : si l'on parvenait à bloquer la prolifération de ces cellules, on bloquerait de facto le développement des tumeurs. Surtout l'enjeu ultime sera de prévenir métastases et récidives en s'assurant, quelle que soit la stratégie thérapeutique retenue (chirurgie, rayonnements, chimiothérapie), que l'on débarrasse le patient de ces cellules cancéreuses particulières.
Avant cela, les chercheurs doivent mettre au point des techniques pour cibler facilement les CSC. Car en les identifiant, ils se sont aussi aperçus qu'elles présentent un défaut de taille : elles ressemblent beaucoup aux cellules souches saines qui permettent aux tissus humains de se régénérer. Un traitement insuffisamment ciblé risquerait donc d'éliminer simultanément les deux lignées.
Le premier foie cultivé fonctionne (Science & Vie, n° 1152, septembre 2013, p. 40.)
Des cellules souches obtenues à partir d'un échantillon de peau humaine cultivées en présence de cellules prélevées sur un cordon ombilical sur un milieu de culture approprié ont abouti à la formation au bout de quelques jours d'un mini-foie capable d'assurer quelques quelques-unes des fonctions majeures de cet organe complexe ! Plus qu'une simple recette, c'est un véritable exploit qu'a réalisé le département de médecine régénérative de l'Université de Yokohama (Japon).
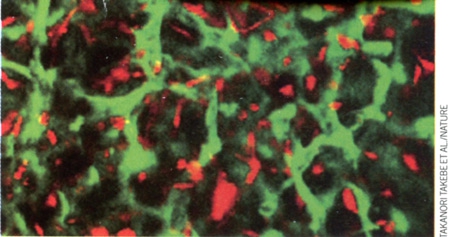
Génération de bourgeons de foie humain à partir de
différents types de cellules souches (en vert et en rouge)
C'est la première fois qu'un tissu hépatique vascularisé, fonctionnel et organisé en trois dimensions est fabriqué en laboratoire. Cette association de plusieurs types de cellules a recréé l'environnement propice à la genèse des organes chez l'embryon. Transplantés chez la souris, ces bourgeons de foie humain d'environ 5 millimètres se connectent au système vasculaire en moins de quarante-huit heures, puis continuent de croître et de se transformer pendant au moins deux mois. Comme l'organe naturel, ils sont capables de synthétiser des protéines et de pallier une insuffisance hépatique induite. Ces résultats obtenus chez la Souris sont très prometteurs. Mais il faudra encore une dizaine d'années avant de pouvoir passer aux études sur l'Homme. Un espoir lointain, mais réel, pour les patients.
Réparer l'oreille interne (Science & Vie, n°1152, septembre 2013 p. 44)
Une fois endommagés par un traumatisme sonore ou par certains médicaments, les composants de l'oreille interne ne se régénèrent pas spontanément, provoquant ainsi des troubles irréversibles de l'équilibre ou de l'audition. Jusqu'à présent, les tentatives de recréer ces cellules avaient toutes échoué. Mais les neuroscientifiques s'en approchent grâce aux cellules souches. À l'école de médecine de l'université d'Indiana, Etats-Unis), une équipe de chercheurs a réussi à recréer en laboratoire une oreille interne de souris ouvrant ainsi la voie à de potentiels futurs traitements sur l'Homme.
Pour cela, ils ont transformé des cellules souches embryonnaires de l'animal en cellules ciliées de l'oreille interne, responsables de la détection des sons et du sens de l'équilibre. "Nous avons observé les mécanismes qui forment les cellules ciliées chez l'animal, et exposé nos cellules souches aux mêmes contraintes chimiques, explique la chercheuse Eri Hashino, qui a dirigé les recherches. Les résultats ont été bien au-delà de nos espérances, puisque les cellules ciliées créées ont d'elles-mêmes évolué pour former différents types de cellules de l'oreille interne." Enfin une piste pour une toute première thérapie.
[1] L'équipe du Pr Philippe Menasché fait partie du consortium REVIVE
Pour en savoir plus :
Un livre :
Nicole le Douarin (2007). - Les cellules souches porteuses d'immortalité, Odile Jacob Sciences Ed.
Un article récent :
Jean François Haït (2013). - Cellules souches : le corps réparé ? Sciences et Avenir hors série octobre-novembre 2013 pp 26-29.
10:00 Publié dans Biologie, Nature et santé, Sexualité-embryologie | Tags : cellules souches, cellules souches adultes induites, cellules souches embryonnaires, ectoderme, endoderme, mésoderme, œuf, cellules germinales, gonocytes, cellule totipotente, cellule souche embryonnaire, cellule souche adulte, cellule souche multipotente, pluripotent stem cells, pst, cellules souches pluripotentes induites, ipsc, hesc | Lien permanent | Commentaires (1) | ![]() Facebook | | |
Facebook | | |
10/10/2013
Les cellules souches pluripotentes induites (iPS)
 Les cellules souches pluripotentes induites (iPS)
Les cellules souches pluripotentes induites (iPS)
par Hervé Ratel
journaliste scientifique
(Sciences et Avenir n° 794, avril 2013, pp. 66-68)
(dernière mise à jour : 28 février 2014)
Le sigle iPS désigne les cellules souches pluripotentes induites, c'est-à-dire des cellules adultes rajeunies au stade embryonnaire. Un stade où elles sont capables de donner n'importe quel type de cellule de l'organisme (pluripotence). Les iPS ouvrent des perspectives majeures dans le traitement de nombreuses maladies incurables. Les premiers essais vont commencer au Japon.
Rajeunir les cellules, c'est la prouesse annoncée par ce simple sigle : iPS. Ce terme désigne les cellules souches pluripotentes induites, soit des cellules adultes reprogrammées jusqu'au stade primitif de cellules embryonnaires. Pour nombre de scientifiques, la révolution annoncée est comparable à celle des vaccins ou des antibiotiques en leur temps. Mise sous les projecteurs en octobre 2012 avec le prix Nobel décerné à leur découvreur, le Japonais Shinya Yamanaka (voir Sciences et Avenir n° 789, novembre 2012), ces cellules iPS sont en effet susceptibles de rendre d'immenses services dans le domaine des greffes de tissus, de faciliter la mise au point de médicaments pour des maladies génétiques et d'élucider certains mécanismes du cancer. Un comité d'éthique japonais a d'ailleurs donné son feu vert pour de premiers essais cliniques qui devraient débuter dès le mois d'avril 2013.
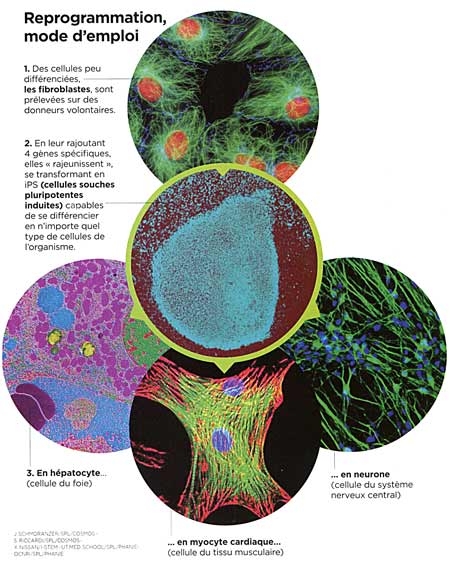
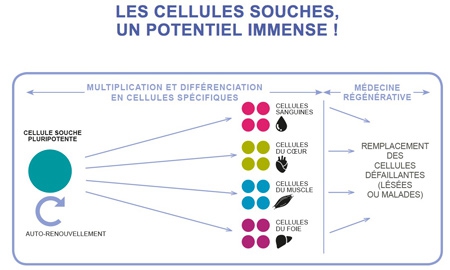
Diagramme © Institut Pasteur
Dans la course mondiale qui démarre, la France est bien placée. "Elle pourrait prendre la tête d'un consortium chargé de piloter un projet de banque européenne de cellules iPS. Celui-ci sera finalisé d'ici à la fm de cette année", pronostique Annelise Bennaceur-Griscelli (Inserm), qui coordonne la plate-forme nationale de cellules souches Ingestem, rassemblant plusieurs laboratoires de l'Hexagone.
Pourtant, les chercheurs français reviennent de loin ! En cause : la loi de bioéthique de 1994 - révisée en 2004 - qui interdit toute recherche sur les cellules souches embryonnaires humaines (CSEh). Ces dernières - qui ne sont pas des iPS - nécessitent en effet d'avoir directement recours à des embryons surnuméraires issus de fécondations in vitro. « Pour obtenir une dérogation les autorisant à travailler sur les CSEh, les chercheurs devaient remplir des documents faisant plusieurs dizaines de pages, raconte Frank Yates, enseignant-chercheur à l'école Sup'Biotech de Paris. Il fallait par exemple décrire à l'avance - exercice impossible et absurde les progrès médicaux attendus des expériences envisagées... Certains baissaient les bras ou s'exilaient à l'étranger devant ce cauchemar bureaucratique.» D'autres pays comme le Royaume-Uni, ont une réglementation moins restrictive, plus en phase avec la recherche fondamentale.

Les scientifiques abasourdis par ces résultats
La découverte des iPS en 2006 est donc venue bouleverser la donne puisque ces cellules ne nécessitent comme matériel de départ que des cellules adultes déjà différenciées, prélevées sur des donneurs consentants. Lors de leur découverte annoncée en 2006 dans la revue Cell c'est pourtant le scepticisme qui avait dominé parmi la communauté scientifique. « J'ai eu la chance d'assister à la première conférence du PrYamanaka sur le sujet, se remémore Frank Yates. Quand il a présente ses résultats, tout le monde était abasourdi. Parvenir à reprogrammer une cellule paraissait totalement improbable. » Improbable parce que cette découverte réduisait à néant l'un des dogmes majeurs de la biologie : une cellule différenciée, comme une cellule musculaire, ne pouvait pas se transformer en une cellule d'un autre type, une cellule hépatique par exemple. Pourtant, il n'a pas fallu longtemps pour que les résultats du chercheur japonais soient reproduits et confirmés par d'autres équipes de biologistes cellulaires à travers le monde. Les cellules iPS étaient bel et bien une réalité.
Pour comprendre, il faut revenir à l'intuition de génie de Shinya Yamanaka : le chercheur a voulu savoir ce qui se passerait si on transférait des gènes actifs uniquement au stade embryonnaire, dans une cellule différenciée adulte. Pour mener l'expérience, il a, avec son équipe, identifié dans un premier temps 24 gènes de ce type, avant de restreindre la sélection à 4 d'entre eux (Oct4, Sox2, Klf4 et c-Myc). Et ça a marché ! Les cellules adultes ont "remonté le temps" jusqu'à redevenir des cellules indifférenciées. Mais cette recette est évidemment bien plus délicate à mettre en œuvre. Et elle ne fonctionne pas à tous les coups : « Dans le meilleur des cas, le taux de conversion de cellules adultes en iPSn'excède pas 5 % », précise Jean-Marc Lemaitre (Inserm, Montpellier). De très nombreux obstacles restent donc à franchir avant de trouver des applications directes aux iPS.
Un travail de culture astreignant fait à la main
La première difficulté consiste à obtenir ces fameuses iPS en quantités suffisantes. Car développer une lignée, c'est un peu comme réussir un soufflé : les ingrédients sont peu nombreux, mais rien n'est possible sans un bon tour de main, du doigté et de la patience. Une fois une iPS obtenue au bout de quelques jours, il faut en effet absolument éviter qu'elle ne se différencie à nouveau et ne redevienne une cellule adulte. Comment ? En veillant en permanence à séparer les iPS nouvellement créées du reste de leurs consœurs encore à l'état différencié dans la boîte de Pétri, ces récipients où l'on cultive les cellules en laboratoire. Un travail astreignant qui, aujourd'hui, se fait encore manuellement. Trois semaines de culture sont nécessaires pour obtenir une colonie et il faut plusieurs mois avant que cette colonie compte quelques milliers de spécimens. « De plus, les cellules iPS sont très sensibles et capricieuses. Il faut les surveiller 24 h/24 », explique Lina El Kassar. Tous les trois mois, cette biologiste de l'I-Stem au Génopole d'Evry, dans l'Essonne, accueille ainsi des chercheurs dans son atelier pour leur transmettre son savoir-faire. À l'issue du stage, chacun repart avec ses propres lignées d'iPS sur lesquelles il peut poursuivre ses travaux de recherche. Une initiative fructueuse qui a permis de former rapidement à la culture des iPS quantité de biologistes français, contribuant au bon positionnement de la France.
Autre difficulté : les iPS souffrent de défauts épigénétiques. En effet, la cure de jouvence qu'elles subissent ne parvient pas à remettre parfaitement tous les compteurs biologiques à zéro. Ainsi, les iPS - à l'inverse des CSEh, les cellules souches embryonnaires humaines - conservent de petites « étiquettes » à la surface de leurs gènes indiquant toujours leur signature de cellules adultes. Autrement dit, vues sous l'angle épigénétique, les iPS n'ont que l'apparence de cellules embryonnaires. En profondeur, elles demeurent de "vieilles" cellules. « Que ce soit pour unefuturemédecine régénératrice ou comme modèle in vitro d'une pathologie, ces désordres épigénétiques doivent êtrepris en compte, explique Marc Peschanski, directeur scientifique de l'I-Stem. Il faudra vérifier au préalable qu'ils ne constituent pas une nuisance.» Car le risque que des iPS souffrant de tels défauts deviennent cancéreuses n'est pas à écarter.
Obtenir des cellules souches pluripotentes par balnéation acide ? (janvier 2014) (Sciences et Avenir n° 805, mars 2014, p. 23)
Plonger des cellules dans un bain légèrement acide est-il de nature à les stresser suffisamment pour les transformer en cellules souches comme le proclame l'équipe de Haruku Obokata, du centre Riken, à Kobe ?
Depuis la publication fin janvier dans les colonnes de Nature du travail des Japonais, des critiques n'ont pas tardé à apparaître sur Internet, et plusieurs équipes dans le monde ont tenté de reproduire ces résultats, pour l'instant, la moisson n'est pas fameuse.
Selon le décompte du site Ipscell, sur dix tentatives, une seule s'est révélée fructueuse, et encore avec une production très modeste. « J'aurais tendance à classer ce résultat des Japonais dans les artefacts de culture, avoue Frank Yates, enseignant-chercheur à Sup'Biotech. Intuitivement, nous sommes beaucoup à penser que s'il était aussi simple d'obtenir des cellules souches, nous y serions arrivés bien avant par accident... »
Irrégularités méthodologiques, fraude délibérée, erreurs de manipulation ou travail scientifique révolutionnaire de nature à changer la face des biotechnologies ? La réponse définitive viendra sous peu, à la fin des investigations scientifiques de rigueur.
Des champs d'application très larges
Étudier une maladie.
En prélevant des cellules sur un malade, les iPS permettent de suivre le développement d'une cellule affectée d'une mutation. Ce qui était impossible avec les CSEh, car il faut disposer d'embryons porteurs de la pathologie.
Mieux comprendre le cancer.
En suivant le devenir d'une cellule à partir de son stade embryonnaire, les chercheurs espèrent élucider les mécanismes conduisant aux processus tumoraux et notamment les métastases.
Concevoir de nouveaux médicaments.
Les iPS doivent permettre à terme détester facilement l'effet de molécules potentiellement intéressantes pour bon nombre de maladies. Cette recherche est actuellement au point mort.
Élaborer une médecine régénératrice.
C'est l'objectif ultime : pouvoir remplacer des neurones, des cellules musculaires, un épiderme, etc. à partir de cellules suffisamment proches du système immunitaire du malade. Voir également sur ce même blog les articles : cellules souches et rajeunissement, des cellules souches dans la rétine, régénération de la rétine humaine, élaboration d'une rétine humaine en culture à partir de cellules souches, obtenir des neurones à l'aide de fibroblastes, créer des dents biologiques grâce à des cellules souches,
L'industrie pharmaceutique n'est pas prête à investir
Les espoirs se tournent plutôt vers la constitution de banques de cellules iPS qui seraient immunologiquement compatibles avec la majeure partie d'une population donnée : Européens, Asiatiques, etc. Soit des banques ethniques qui risquent de faire grincer bien des dents... D'autant que les firmes pharmaceutiques ne semblent pas décidées à participer à la constitution de telles banques. « Culturellement, les industriels de la pharmacie sont des chimistes, pas des biologistes, justifie Marc Peschanski. Ils ont encore du mal à travailler avec du matériel vivant. » Un avis partagé par Laurence Daheron, responsable de la plate-forme iPS/CSEh à l'université Harvard (Cambridge. États-Unis) : « L'industrie pharmaceutique commence tout juste à entrevoir le potentiel des iPS. Elle est loin d'être prête à s'investir dans la thérapie cellulaire. Il n'y a aucun changement radical à attendre de sa part pour les années à venir. Elle se contentera d'utiliser les iPS pour rester des médicaments classiques, rien de plus. »
Pourtant, tout porte à croire que le jour où la recherche publique aura prouvé le potentiel thérapeutique des iPS, la demande de millions de patients en attente d'un traitement sera suffisamment pressante pour forcer la main des industriels. Il reste juste à espérer que ces derniers auront alors la capacité de prendre le train en marche...
S'affranchir des manipulations fastidieuses in vitro en produisant in vivo des cellules souches pluripotentes induites (iPS)
Dans un article de Nature paru le 11 septembre 2013, des chercheurs espagnols sont parvenus à reprogrammer « in vivo » des cellules adultes de souris. Cette technique permet donc de s'affranchir des fastidieuses et coûteuses mises en culture des cellules adultes !
Le premier défi pour les chercheurs du Centre national de recherche sur le cancer (CNIO, Madrid) était de reproduire l'expérience de Yamanaka chez un être vivant. Ils ont choisi la souris comme organisme modèle. En utilisant des techniques de manipulation génétique, les chercheurs ont créé des souris dans lesquelles quatre gènes de Yamanaka pouvaient être activés à volonté. Lorsque ces gènes sont activés, les chercheurs ont observé que les cellules adultes étaient capables de régresser dans leur développement évolutif pour devenir des cellules souches embryonnaires dans plusieurs tissus et organes
En outre, l'équipe de Manuel Serrano a ainsi obtenu des cellules souches de meilleure qualité que celles produites in vitro. C'est un résultat spectaculaire : faire en sorte que des souris fabriquent des cellules souches pluripotentes induites, capables de fournir quasiment n'importe quelle cellule spécialisée de l'organisme. Autrement dit, qu'au sein d'un animal vivant des cellules adultes redeviennent des cellules souches embryonnaires ! Reprogrammer in vivo des cellules est désormais possible. La démonstration chez l'animal de la faisabilité d'un tel concept pourrait bouleverser la pratique de la future médecine régénératrice.
Les chercheurs espagnols ont ainsi franchi une nouvelle étape, en obtenant les mêmes résultats que Yamanaka, mais cette fois au sein du même organisme, chez la souris, sans avoir besoin de passer à travers dans des boîtes de culture in vitro. La génération de ces cellules dans un organisme apporte cette technologie encore plus proche de la médecine régénérative.
L'étape du laboratoire sera ainsi supprimée. Jusqu'à présent, on imaginait que pour greffer ces cellules iPS à un malade souffrant de diabète insuline-dépendant, d'insuffisance cardiaque ou de la maladie de Parkinson, il fallait au préalable les produire en passant par des manipulations sophistiquées et coûteuses en laboratoire. Le travail réalisé par l'équipe de Manuel Serrano bouleverse ce protocole : il sera possible d'induire la production de ces précieuses cellules souches au sein même du tissu ou de l'organe à réparer sans passer par l'étape du laboratoire. Une fois ces iPS produites par le patient, elles seraient amenées à se différencier en un type cellulaire particulier, en cellule du pancréas, du cœur, en neurone, par exemple.
Comme indiqué au début de cet article, pour reprogrammer des cellules adultes (de peau notamment) en cellules souches, il faut y introduire quatre gènes clés (Oct4, Sox2, Kfl4 et c-Myc). Ceux-ci produisent quatre facteurs de croissance jouant un rôle dans les premiers temps du développement embryonnaire. Les cellules adultes ainsi reprogrammées, dénommées iPS, sont capables de « remonter le temps » jusqu'au stade embryonnaire.
Cette technique de production, mise au point en 2006, a d'ailleurs valu le prix Nobel de médecine en 2012 au Japonais Shinya Yamanaka. Les chercheurs espagnols sont allés plus loin : l'organisme de leurs souris transgéniques fabrique lui-même ces quatre facteurs de croissance. Pour activer les quatre gènes, ils ont fait boire aux rongeurs de l'eau contenant de faibles doses d'un antibiotique : la doxycycline. Résultat : au bout de deux semaines et demie, les rongeurs ont développé des tumeurs (tératomes,) issues de cellules souches pluripotentes et contenant plusieurs types cellulaires adultes. Preuve manifeste pour les chercheurs que des cellules adultes de ces rongeurs avaient bien été reprogrammées en iPS avant qu'elles ne se transforment, à leur tour, et en divers endroits, en plusieurs types cellulaires. Par ailleurs, l'analyse de tissus de l'estomac, de l'intestin, du pancréas et des reins des rongeurs a montré la présence disséminée d'une reprogrammation cellulaire in vivo. De même, les chercheurs ont détecté la présence d'iPS dans le sang des souris qui avaient été reprogrammées pour en fabriquer.
Ces cellules iPS sont d'une qualité supérieure
Une autre surprise attendait les chercheurs : les cellules iPS produites chez ces souris et obtenues directement à partir de l'intérieur de l'organisme, ont une plus grande capacité de différenciation que ceux obtenus par culture in vitro. Plus précisément,ces ceklules ont les caractéristiques des cellules totipotentes, un état primitif jamais obtenu dans un laboratoire.
En effet, outre leur capacité à se transformer en n'importe quel type de cellule d'un embryon, elles ont pu se différencier en placenta. Ce résultat étonnant fait dire aux chercheurs que ces iPS obtenues in vivo sont à un stade encore plus précoce que les iPS produites en laboratoire. Il est évidemment hors de question d'utiliser une procédure semblable chez l'Homme, dans la mesure où les cellules reprogrammées risqueraient de former des tumeurs. En revanche, une stratégie de régénération in vivo pourrait, dans l'avenir, consister à administrer au malade, localement et pendant un temps limité, des gènes synthétiques codant les quatre facteurs de croissance identifiés par le prix Nobel Shinya Yamanaka.
D'autres pistes sont à l'étude comme administrer, au sein d'un organe ou d'un tissu malade, un cocktail de petites molécules capables d'activer le programme génétique de production de cellules iPS ou utiliser des virus rendus inoffensifs pour délivrer les quatre fameux gènes clés.
María Abad, le principal auteur de l'article et chercheur dans le groupe de Serrano, a déclaré: "Ce changement de direction dans le développement n'a jamais été observé dans la nature, nous avons démontré que nous pouvons également obtenir des cellules souches embryonnaires dans les organismes adultes et pas seulement en. le laboratoire ".
"Nous pouvons maintenant commencer à penser à des méthodes pour induire la régénération localement et de manière transitoire pour un tissu endommagé particulier.", précise Manuel Serrano.
Les cellules souches obtenues chez la souris montrent également des caractéristiques totipotentes jamais produites dans un laboratoire, équivalentes à celles présentes dans les embryons humains au stade de 72 heures de développement, quand ils sont composés de seulement 16 cellules.
En comparaison avec les cellules obtenues avec la technique développée par Yamanaka, les cellules souches obtenues par le CNIO représentent donc un état encore embryonnaire plus précoce, avec une plus grande capacité de différenciation.
Les auteurs ont même été capables d'induire la formation de structures pseudo-embryonnaires dans les cavités thoracique et abdominale des souris. Ces pseudo-embryons affichaient les trois couches typiques des embryons (ectoderme, mésoderme et endoderme), et des structures extra-embryonnaires tels que la membrane vitelline et même l'ébauche de cellules sanguines.
"Ces données nous disent que nos cellules souches sont beaucoup plus polyvalentes que les cellules iPS obtenues in vitro par Yamanaka, qui génèrent les différentes couches de l'embryon mais jamais les annexes embryonnaires, comme le placenta", a déclaré Manuel Serrano.
Les auteurs soulignent que les applications thérapeutiques possibles de leurs travaux restent lointaines, mais ils admettent que, sans doute, cela pourrait signifier une réorientation de la recherche sur les cellules souches, la médecine régénérative et l'ingénierie tissulaire.
"Nos cellules souches survivent aussi en culture, permettant ainsi de les manipuler dans un laboratoire. L'étape suivante est d'étudier si ces nouvelles cellules souches sont capables de produire efficacement différents tissus tels que ceux du pancréas, du foie ou du rein. ", a déclaré Abad.
Sources :
- María Abad, Lluc Mosteiro, Cristina Pantoja,Marta Cañamero, Teresa Rayon,Inmaculada Ors, Osvaldo Graña, Diego Megías, Orlando Domínguez,Dolores Martínez, Miguel Manzanares,Sagrario Ortega & Manuel Serrano. (2013). Reprogramming in vivo produces teratomas and iPS cells with totipotency features Nature : 10.1038/nature12586.
- Marc Gozian (2013) Des souris vivantes ont produit des cellules souches (Sciences et Avenir, n° 800, octobre 2013, pp. 78-79).
Voir également dans ce blog, l'article : Les-potentialités infinies des cellules souches.
16:50 Publié dans Biologie, Médecine | Tags : cellules souches, cellules souches adultes induites, ips, cseh, rétine, cancer | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |