05/10/2009
La Couleuvre verte et jaune
 La Couleuvre verte et jaune
La Couleuvre verte et jaune
Hierophis viridiflavus
(Reptile squamate Ophidien Colubridé)
par André Guyard
(Dernière mise à jour le 23 août 2016)

La Couleuvre verte et jaune (Hierophis viridiflavus) est une espèce de serpent de la famille des Colubridés qui se rencontre principalement au nord de la Méditerranée (France, Italie, sud de la Suisse, Espagne, pays de l’ancienne Yougoslavie, Grèce, ainsi que quelques îles comme Malte ou Chypre).
Morphologie
Il s’agit d’une grande couleuvre mesurant entre 1,10 m et 1,30 m. Certains spécimens atteignent même 1,80 m. Adulte, la face dorsale présente une vingtaine de lignes longitudinales discontinues jaune verdâtre. La face ventrale est blanc jaunâtre.

La longueur du corps peut atteindre 1,80 m
photo DR

Contrairement à la pupille en fente verticale des Vipéridés

Tête de Couleuvre verte et jaune © Michel Cottet

La face dorsale de la tête de la Couleuvre verte et jaune
La Couleuvre verte et jaune fréquente les terrains rocheux, secs et bien ensoleillés, exceptionnellement les milieux un peu plus humides comme les prairies et les bords de rivières. Serpent solitaire sauf pendant les accouplements, et pendant la période hivernale.

Le serpent n’hésite pas à grimper

© Nicole Lartigau
Alimentation
Le régime évolue avec leur croissance. Les jeunes se contentent d’insectes, de petits lézards, tandis que les adultes chassent activement souris, rats, lézards, oiseaux et parfois d’autres serpents. Elle peut s’approcher des habitations pour y attraper des souris.

Contrairement aux vipères aux écailles carénées,
En mars-avril, la Couleuvre verte et jaune sort de sa léthargie hivernale et s’accouple. L'accouplement donne lieu à une danse spectaculaire décrite par la vidéo suivante due à Pascal Thormeyer 19 mai 2012.
Photographies prises par André Guyard en mai 2009 au Creux sous Roche dans le Marais de Saône, lors d’une sortie "Nature et Découvertes" animée par Michel Cottet.
21:51 Publié dans Herpétologie, Limnologie-hydrobiologie | Tags : couleuvre verte et jaune, hierophis viridiflavus, serpents non venimeux, ophidiens | Lien permanent | Commentaires (3) | ![]() Facebook | | |
Facebook | | |
Les pistes de dinosaures de Coisia (Jura)
 Les pistes de dinosaures
Les pistes de dinosaures
Suite à l’élargissement de la départementale qui conduit au village de Coisia, une dalle au pendage prononcée est apparue en bordure de route. En 2004, un géologue amateur éclairé appartenant à la Société Des Naturalistes d'Oyonnax (SDNO) eut son attention attirée par des empreintes de pas gigantesques.

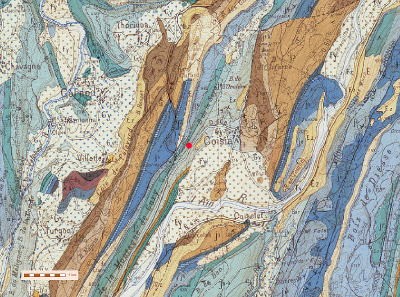



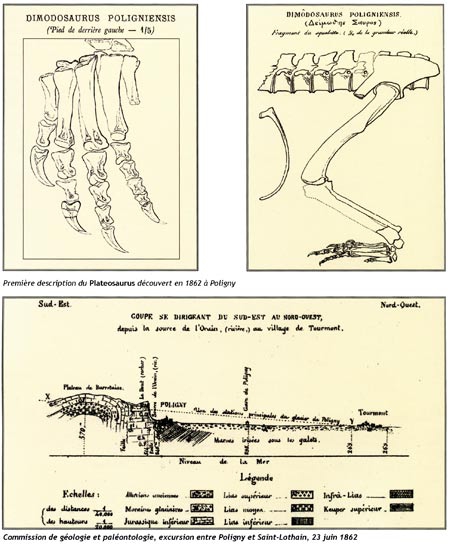
Document tiré de Jura… Jurassique, Hantzpergue et al. 2010
21:43 Publié dans Paléontologie - archéologie | Tags : dinosaures, sauropodes, fossiles, pistes, jurassique | Lien permanent | Commentaires (2) | ![]() Facebook | | |
Facebook | | |
Les Cnidaires d’eau douce
 Hydres et autres Cnidaires
Hydres et autres Cnidaires
en eau douce
par André Guyard
(Texte mis à jour le 05/01/2013)
Les Cnidaires sont des Métazoaires (animaux pluricellulaires) diploblastiques (à deux feuillets), à symétrie radiaire parfois accompagnée d’une symétrie bilatérale. Ils comprennent environ dix mille espèces toutes aquatiques, la plupart marines et carnivores. Le corps possède une cavité unique, le coelentéron ou cavité gastrique. Des cellules urticantes ou cnidoblastes sont localisées dans des zones stratégiques de l’ectoderme et jouent un rôle dans la capture des proies. Les Cnidaires étaient autrefois regroupés avec les Cténaires (formes exclusivement marines) dans l’embranchement devenu caduque des Coelentérés.
ORGANISATION GÉNÉRALE
La plupart des Cnidaires ont deux stades dans leur cycle de vie sans parler de la phase larvaire : un stade fixé donc benthique - le polype - et un stade libre planctonique - la méduse.
Le corps du polype a la forme d’un sac fixé à une extrémité sur le substrat par une sole pédieuse. A l’autre extrémité, au sommet d’un petit renflement dessinant une zone hypostomiale, s’ouvre l’unique orifice du corps, la bouche entourée par des tentacules ; elle est dirigée vers le haut et met en communication avec l’extérieur la cavité gastrique dont les ramifications se terminent dans les tentacules. Le corps se divise ainsi en trois régions : corps du polype, tentacules et sole pédieuse. Le polype est capable de reproduction asexuée.
La méduse qui représente la forme libre a au contraire, l’orifice buccal dirigé vers le bas et offre l’image d’une cloche transparente dont le battant correspond à la région gastrique (manubrium).
La cloche ou ombrelle, est formée de fines digitations, les tentacules, implantés sur le pourtour d’un cercle rétréci (chez les Hydroméduses) par un voile ou velum, délimitant une cavité sous-ombrellaire dans laquelle pend le manubrium.
La bouche s’ouvre à l’extrémité de ce manubrium ; elle donne accès à un court oesophage qui aboutit dans un estomac situé au sommet de la cloche. Il en part des canaux radiaires au nombre de 4 ou d’un multiple de 4, qui rejoignent un canal circulaire ou marginal bordant l’ouverture de l’ombrelle. Ce canal envoie un diverticule dans chaque tentacule et est flanqué de deux cordons nerveux qui se prolongent également dans les tentacules.
Les gonades se développent sur les canaux ou sur le manubrium. La méduse possède des organes des sens : ocelles ou yeux rudimentaires disposés à la base des tentacules, et statocystes, ou organes d’équilibration situés entre les tentacules.
Parmi les formes d’eau douce de nos régions, on ne trouve que des représentants de la classe des Hydrozoaires. Cette classe groupe en principe des individus dont le cycle de vie est métagénétique avec alternance de générations de polypes asexués et de méduses sexuées. Cependant il existe des exceptions et c’est le cas des hydres d’eau douce (ordre des Hydrides) qui ne présentent que la forme polype et des Limnoméduses où le stade méduse devient nettement prépondérant.
LES HYDRES D’EAU DOUCE
Elles comportent plusieurs espèces commune à la belle saison. On les trouve fixées aux végétaux immergés dans les mares et les étangs.
MORPHOLOGIE EXTERNE
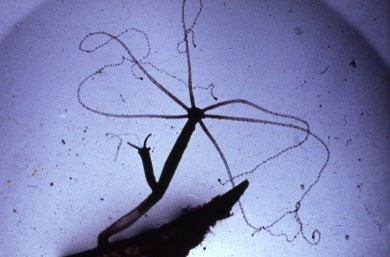
A l’état d’extension, l’hydre est un sac allongé, terminé par une couronne de six tentacules (ou 8) très longs et très contractiles qui entourent la bouche. Dans la région opposée, l’hydre est fixée par la sole pédieuse.
On distingue dans nos régions trois espèces : Pelmatohydra oligactis (fig. 1) a une colonne gastrique d’un brun noirâtre qui surmonte un pédoncule long mince et translucide, et porte des tentacules très étirés.
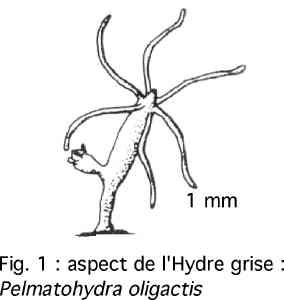
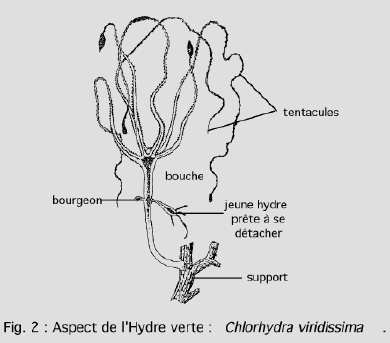
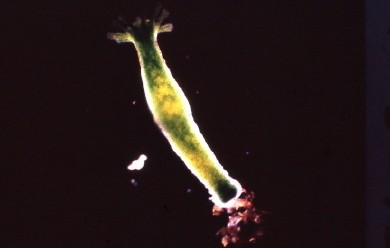
Elle doit sa couleur à la présence de
Hydra attenuata, gris brun, très pâle au niveau du pédoncule qui se prolonge par une colonne de même diamètre.
En période de reproduction, l’hydre présente à sa surface des renflements qui correspondent aux ovaires ou aux testicules. Elle peut également bourgeonner.
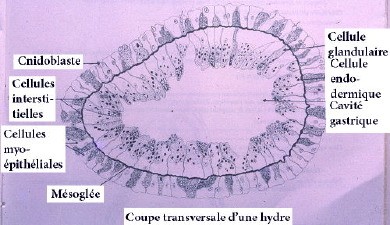
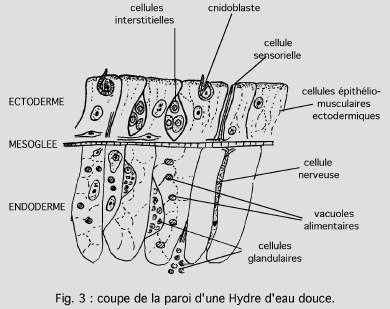
STRUCTURE
La paroi du corps (fig. 3) comporte un ectoderme unistratifié de cellules myo-épithéliales, avec des cellules nerveuses multipolaires, des massifs de cellules interstitielles, à caractères embryonnaires, pouvant redonner par multiplication et différenciation tout élément cellulaire ; des cnidoblastes ou cellules urticantes, munies d’un harpon creux injectant aux proies un poison l’actinocongestine.
L’endoderme tapisse la cavité digestive. Il est formé d’une unique couche de cellules très vacuolisées dont la base s’étendant sur la mésoglée, montre des myofibrilles transversales et leur bord libre du côté de la cavité présente des flagelles. Elles sont douées de phagocytose. On trouve également des cellules glandulaires et des cellules neuroépithéliales comme dans l’ectoderme.
La mésoglée est une substance colloïdale peu épaisse constituée par les lames basales des deux épithéliums.
BIOLOGIE
1. Locomotion et mouvements.
- Suivant le degré d’excitation, l’hydre peut se rétracter en une boule à peine visible à l’œil nu. Le réseau nerveux assure une certaine coordination aux mouvements des tentacules étalés normalement en position de chasse.
- Les déplacements se font par glissement sur la sole pédieuse ou par arpentage avec culbute (fig. 4). L’hydre présente un phototropisme variable suivant l’espèce.
- L’hydre peut quitter son support et nager par ses tentacules.

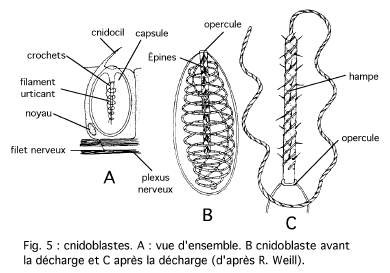
Les tentacules capturent les proies, les paralysent par les cnidoblastes et les amènent à la bouche. La digestion est extra-cellulaire dans la cavité gastrique avec un broyage dû aux mouvements du corps, puis intra-cellulaire après phagocytose dans les cellules endodermiques.
L’hydre s’accroît constamment par sa région orale par mitose de cellules interstitielles, si les conditions de vie sont favorables. Cette croissance est compensée par l’usure des cellules au niveau de la sole pédieuse. Une Hydre est ainsi totalement rénovée en un à deux mois.
4. Multiplication asexuée
- Bourgeonnement
- Scissiparité longitudinale par dédoublement de la zone de croissance.
- Régénération très facile.
À l'inverse, lorsque les biologistes allemands ont inactivé spécifiquement ce gène, les cellules souches de l'animal se sont différenciées en cellules adultes.
Bien que présent dans l'ensemble du monde animal, et donc chez l'Homme, le gène FoxO voit son expression diminuer au fil du processus normal de vieillissement... sauf chez l'hydre qui, de fait, ne vieillit pas et ne meurt jamais. En conclusion, un seul gène assure la régénération sans fin de tous les tissus du corps de l'hydre. Une propriété à exploiter pour lutter contre le vieillissement chez l'Homme ?
5. Reproduction sexuée
Elle apparaît quand les conditions de température deviennent défavorables : 10-12°C pour P. oligactis, 16-20°C pour C. viridissima et H. attenuata. P. oligactis et H. attenuata sont gonochoriques (sexes séparés). C. viridissima est hermaphrodite protandre (les spermatozoïdes sont mûrs avant les ovules).
Les gonades constituent des renflements apparaissant sur la colonne. Les testicules apparaissent dans le quart antérieur de la colonne, les ovaires à la moitié de la colonne.
Après fécondation, l’œuf commence sa segmentation totale et égale.
RÔLE BIOLOGIQUE DES HYDRES D’EAU DOUCE
Elles jouent un rôle qui passe inaperçu dans les biocénoses dulçaquicoles.
Utilisation dans les méthodes biologiques
Elles ne sont citées que dans la méthode des saprobies dans les zones :
β-mésosaprobe : Hydra vulgaris, Hydra oligactis = H. fusca et Hydra polypus existent déjà en zone α-mésosaprobe dans le périphyton des étangs des fossés et des eaux calmes.
oligosaprobe : Chlorohydra viridissima. Cordylophora lacustris : existe déjà dans la zone β-mésosaprobe.

Dans ce déversoir ferrugineux du lac Pavin (Auvergne),
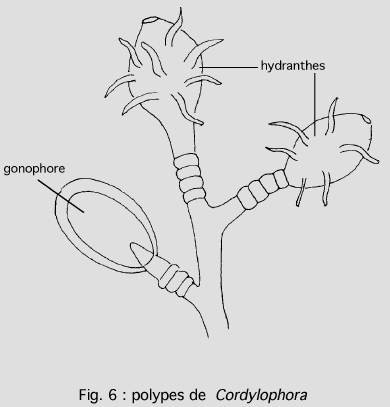
Dans les eaux saumâtres, on rencontre une espèce d’Hydraire gymnoblastique de la famille des Claviidae : Cordylophora caspia ( = lacustris). Cette espèce répandue sous toutes les latitudes, se présente sous la forme d’une colonie de polypes pouvant atteindre plusieurs cm (fig. 6). La colonie est fixée au substrat par un réseau de stolons, sur lesquels s’élèvent les hydrocaules portant les polypes (hydranthes) et les gonophores (polypes spécialisés dans la production de gamètes). Il n’y a pas de stade méduse.
Dans cet ordre, le stade méduse devient prépondérant et le polype, très régressé, de quelques millimètres de longueur, est souvent solitaire ou forme des colonies de 4 à 5 individus seulement. Les représentants vivent en eau douce ou saumâtre.
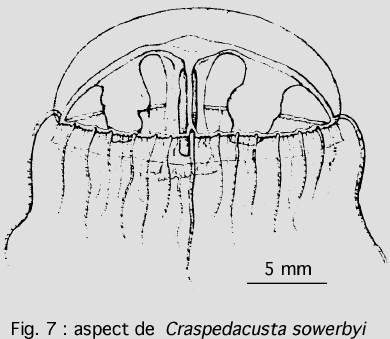

L’apparition de cette méduse en Europe vers 1880 pose des problèmes encore non résolus, par exemple celui de sa reproduction. Généralement, les méduses trouvées dans une même région sont de même sexe. Ce fait est dû probablement à l’existence d’une génération de polypes asexués décrits sous le terme de Microhydra ryderi. Mais il s’agit de la même espèce.
On ignore comment elle est arrivée là : cette méduse existe dans le bassin de l’Institut des Sciences Naturelles, place Leclerc à Besançon. Dans les années mille neuf cent soixante, elle s’est signalée par une prolifération étonnante, envahissant de ses ombrelles la totalité du volume du bassin. De nouveau dans les années quatre-vingt, autre prolifération. La forme polype, difficile à observer, persiste certainement sur les parois du bassin. Et la forme méduse, forme sexuée se manifeste lorsque les conditions de vie du polype deviennent difficiles.
Autre limnoméduse, dans les lagunes saumâtres du Sud de la France, Picard (1951) a observé la limnoméduse Odessia maeotica f. gallica qui présente annuellement deux périodes d’activité sexuelle et fait partie de la famille des Moerisiidae.
On ne connaît comme autre méduse d’eau douce que le genre africain Limnocnida.
16:23 Publié dans Cnidaires, Invertébrés, Limnologie-hydrobiologie | Lien permanent | Commentaires (5) | ![]() Facebook | | |
Facebook | | |
Le Chocard à bec jaune
 Le Chocard à bec jaune
Le Chocard à bec jaune
Pyrrhocorax graculus
(Famille des Corvidés)
par André Guyard

Le Chocard fréquente les alpages

Les deux sexes sont semblables
Les chocards sont grégaires. Ils volent en bandes pouvant compter plus d’une centaine d’individus. Ils excellent dans l’art d’utiliser les courants, planant et profitant des ascendances thermiques.

À l’affût d’un morceau de pain
Le Chocard se nourrit principalement d’invertébrés, en particulier d’insectes et de petits escargots. Mais il repère très vite les randonneurs et s’invite sans tarder au pique-nique.
Photos et vidéo dues à André Guyard et réalisées dans le Chablais.
16:11 Publié dans Ornithologie | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
Le Chamois des Alpes
 Le Chamois des Alpes
Le Chamois des Alpes
Rupicapra rupicapra
(Famille des Bovidés, sous-famille des Caprinés)
par André Guyard
Le Chamois appartient à la famille des Bovidés et à la sous-famille des Caprinés (chèvres). Trois sous-espèces de Chamois habitent notre pays : le Chamois des Alpes (Rupicapra rupicapra rupicapra), le Chamois de Chartreuse (Rupicapra rupicapra cartusiana) et le Chamois des Pyrénées ou Isard (Rupicapra pyrenaica pyrenaica).
Le Chamois des Alpes mesure de 0,75 m à 0,80 m au garrot et de 1, 25 m à 1, 35 m de longueur. Le poids d’un mâle adulte varie de 35 à 50 kg, celui d’une femelle de 25 à 38 kg.

Crinière hérissée, le bouc surveille les intrus surgissant sur son territoire

Dans le parc du Mercantour, les chamois ne
Chez le Chamois, comme pour tous les bovidés, les cornes sont conservées tout au long de la vie. Elles poussent dès la naissance, mais ne sont visibles que vers 2 mois. À 6-7 mois, elles mesurent de 3 à 5 cm et amorcent une légère courbure vers l’arrière.
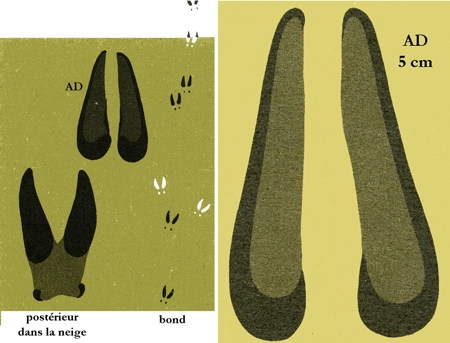
Empreintes et voie de chamois dans la neige
L'empreinte du Chamois est très caractéristique 6 cm de long sur 3,5 cm de large). Les marques des deux sabots sont très nettes et et à peu près aussi larges en avant qu'en arrière et il y a toujours un intervalle aussi important entre les deux pinces. Les doigts postérieurs en position élevée sur la jambe ne laissent des traces qu'en neige profonde.
Le Chamois des Alpes peuple naturellement tous les départements des Alpes et du Jura. Il a été introduit dans les Vosges et dans le Cantal. Le Chamois de Chartreuse se rencontre uniquement dans le massif de la Chartreuse entre Grenoble et Chambéry.
L’estimation des effectifs de chamois donne un minimum de 70 000 dans les Alpes, 3 000 dans le Jura, 2 600 dans les Vosges et 600 dans le Massif central.
La reproduction
Dès le mois d’octobre, en général au-dessus de la forêt, on observe de grands rassemblements d’animaux où se joignent les mâles d’habitude solitaires. Le rut commence dès novembre pour se terminer vers la mi-décembre. Dans la première moitié du rut, ce sont les mâles âgés qui empêchent les plus jeunes de courtiser les femelles et qui assurent les saillies.
C’est à peu près 23 semaines plus tard, entre printemps et été, que la femelle donne naissance à un jeune. Il n’est pas rare qu’une femelle âgée de 15 ans et plus soit encore féconde. Le chevreau mesure 0,50 m de long et 0,35 m de haut et pèse de 2 à 2, 7 kg. Il lui suffit de quelques heures pour se tenir debout et quelques jours pour suivre sa mère. À l’âge de 2 mois, il pèse entre 9 et 10 kg.
L’habitat
Malgré une idée largement répandue, le Chamois n’est pas l’animal de la haute montagne. Il préfère la zone forestière et la partie inférieure de la montagne pastorale. Le critère prépondérant à l’habitat du Chamois, c’est le relief accidenté. Il n’existe pas de population vivant en terrain plat et dépourvu de pentes rocheuses.
L’utilisation du milieu est très variable, la répartition dans l’espace des animaux n’est jamais figée. Elle varie aussi dans le temps. Enfin les regroupements sont liés au sexe et à l’âge des animaux. Le Chamois est particulièrement bien adapté à la vie en montagne. En hiver le sous-pelage est constitué d’un duvet laineux de 2 à 3 cm d’épaisseur qui couvre tout le corps. Les os longs des membres antérieurs et postérieurs forment des angles très fermés qui leur procurent une souplesse et une détente étonnantes. Le bord des sabots permet une adhérence élevée sur les rochers et la palmure interdigitale assure une bonne portance sur la neige. Enfin le cœur des chamois et isard est un muscle très puissant. Abondamment oxygéné par le sang très riche en globules rouges, il permet aux animaux de soutenir des efforts intenses et violents.
L’alimentation
Les végétaux constituent la nourriture exclusive des chamois. Ils consacrent une grande partie de leur temps à cette activité.
Au printemps : chamois et isards gagnent les fonds de vallées attirés par les pousses nouvelles de graminées ou de fleurs. Grisés par cette nourriture, leur observation peut être alors d’une grande facilité ;
En été et en automne : la ressource alimentaire est vaste, légumineuses et graminées sont préférées ;
En hiver : l’accessibilité à la nourriture est liée à la couverture neigeuse. Les animaux parcourent alors les rares secteurs où la neige ne tient pas. Ils s’alimentent aussi en forêt, utilisant les rameaux, écorces et lichens. Toutefois cette situation est très fluctuante dans l’espace et dans le temps et l’on considère que les chamois ne commettent pas de dégâts importants.
Les chamois sont friands de sel, qui est un élément nutritif nécessaire. Ils le trouvent sous forme de salines naturelles et de pierres à sel déposées par les bergers pour les moutons. Les besoins en eau sont assurés par la consommation des végétaux et par la rosée matinale, il est rare d’observer un chamois qui se désaltère.
Les relations avec les autres espèces
L’augmentation des effectifs des différentes espèces d’ongulés sauvages en montagne et particulièrement du Cerf et du Chevreuil fait que la fréquence des contacts est élevée. Ces relations sont dépendantes des différents facteurs du milieu tels que la densité des espèces, la ressource alimentaire, les conditions hivernales. En hiver en montagne, Chamois et Chevreuil cohabitent, si des conditions difficiles persistent cela peut conduire à des concentrations élevées. On suppose que la tolérance entre espèces est mutuelle. Les choix alimentaires des espèces sont le plus souvent complémentaires.
La fréquentation d’un même territoire par les chamois et des troupeaux d’animaux domestiques est rarement simultanée. En été, chamois et moutons ne fréquentent qu’exceptionnellement les mêmes versants et les mêmes altitudes.
Sur des territoires où cohabitent le Loup ou le Lynx et le Chamois, ce dernier représente une part non négligeable de l’alimentation de ces grands prédateurs.
Le petit film qui illustre cet article a été réalisé par André Guyard dans le Parc du Mercantour ainsi que les photos qui sont extraites du film.
De nombreux sites sont consacrés au Chamois, en particulier :
http://fr.wikipedia.org/wiki/Chamois
http://www.capserveur.com/ancgg/especes_chamois.asp
15:58 Publié dans Mammifères | Lien permanent | Commentaires (2) | ![]() Facebook | | |
Facebook | | |
Le Bouquetin des Alpes
 Le Bouquetin des Alpes
Le Bouquetin des Alpes

Voici le barrage de Cingino en Italie,
mais regardez de plus près…
(photo DR)

La paroi du barrage est constellée de bouquetins !
(photo DR)

Les bouquetins aiment broûter les mousses
et lichens et lécher les concrétions salines
qui se forment sur la paroi du barrage
(photo DR)
Le mâle

Un vieux solitaire en pleine rumination
Dès l’âge de trois mois, la tête du mâle s’orne de cornes persistantes, recourbées vers l’arrière et plus ou moins divergentes selon les individus et les populations. Ces cornes grandissent toute la vie en se parant de nodosités, aussi appelées bourrelets de parure. Lors de la mort de l’animal, elles peuvent atteindre un mètre de longueur et peser près de 5 kg la paire.
La femelle

Femelles et jeunes restent en hardes,
Reconnaissance des sexes
À partir de l’âge de deux ans, le dimorphisme sexuel est suffisamment marqué pour que la détermination des sexes en nature soit possible. Avant cet âge, la détermination du sexe est plus délicate et repose essentiellement sur un examen attentif des cornes : celles des éterlous (jeunes mâles) sont plus épaisses à la base (du fait de l’apparition des premières nodosités), tandis que celles des éterles (jeunes femelles) sont plus minces et dépourvues de bourrelets.
Reproduction
Le Bouquetin est une espèce polygame. Les hardes mixtes commencent à se former dès le début du mois novembre, mais le rut à proprement parler ne débute réellement qu’au début du mois de décembre. Au sein de ces troupeaux, il se crée une hiérarchie.
Des conditions météorologiques difficiles en début d’hiver, empêchant les mâles de rejoindre les femelles, peuvent entraîner des accouplements plus tardifs, jusqu’en février. Bien sûr, ils provoquent des mise bas retardées, courant juillet (au lieu de début juin). À la fin du rut qui se termine généralement début janvier, les animaux se montrent particulièrement fatigués car ils mangent très peu durant cette période.
La mise bas s’effectue tous les ans pour chaque femelle après 165 à 170 jours de gestation. Les naissances interviennent généralement au début du mois de juin, mais peuvent s’échelonner entre la fin du mois de mai et la mi-juillet.
L’étagne met bas un seul cabri généralement, mais des jumeaux peuvent être observés dans certaines colonies, notamment dans les plus jeunes. L’allaitement dure deux à trois mois, mais peut se prolonger durant l’hiver (jusqu’en janvier parfois). La longévité potentielle extrême est estimée à 25 ans chez le Bouquetin des Alpes. La femelle, par son mode de vie, aurait une espérance de vie légèrement supérieure à celle du mâle.
Habitat
Le Bouquetin des Alpes est un animal de rocher. Il s’épanouit sur les adrets (versants tournés au sud), dans de grandes parois rocheuses abruptes, riches en surplombs, couloirs, vires... Dans les massifs élevés, il se tient généralement entre 2400 et 3300 mètres, mais, sur ces mêmes massifs, on peut le voir évoluer 1000 mètres plus bas. Le Bouquetin n’aime pas la neige et ne franchit jamais de grands névés ou de glaciers.
Nourriture
En haute montagne, les plantes herbacées constituent la base principale de l’alimentation du Bouquetin des Alpes : poacées, fabacées, astéracées et cypéracées. Mais il ne dédaigne pas pour autant les feuilles et les jeunes pousses d’arbustes de l’année. Les hardes de bouquetins n’hésitent pas à se mêler aux troupeaux de chèvres domestiques comme au Refuge de Trébentaz sur le GR5 au-dessus de Châtel (Haute-Savoie). Le Bouquetin absorbe souvent de l’eau sous forme de neige ou de rosée, mais boit (dans un ruisseau ou une flaque) très rarement.
* CRAVE et Parc national des Écrins, 1995. - Faune Sauvage des Alpes du Haut Dauphiné - Atlas des vertébrés - Tome 1. 303 p.
* DRAGESCO Éric, 1995. - La vie sauvage dans les Alpes. - Éditions Delachaux et Niestlé. 239 p.
* KRAMMER Mathieu, 2003. – Le Bouquetin des Alpes, Capra ibex ibex. www.bouquetin-des-alpes.org.
* ONCFS, 1997. - Le Bouquetin des Alpes. - Brochure technique de l’ONCFS n°24. 32 p.
* Publications de l’École moderne française et des parcs nationaux de France, BT Nature, 1991. - Le Bouquetin. 39 p.
* SCHILLING D., SINGER D. & DILLER H. 1986. – Guide des Mammifères d’Europe. Éditions Delachaux et Niestlé. 280 p.
* WEBER Éric, 1994. - Sur les traces des Bouquetins d’Europe. - Éditions Delachaux et Niestlé. 176 p.
* http://fr.wikipedia.org/wiki/Bouquetin
Vidéo et photos prises dans le Parc National du Mercantour par André Guyard. On trouvera sur internet de nombreux sites, souvent élaborés par des naturalistes passionnés et beaucoup plus complets que ce simple aperçu.
15:35 Publié dans Mammifères | Lien permanent | Commentaires (4) | ![]() Facebook | | |
Facebook | | |
Le Crapaud sonneur à ventre jaune (Bombina variegata)
 Le Sonneur à ventre jaune
Le Sonneur à ventre jaune
Bombina variegata
(Amphibien anoure discoglossidé)
par André Guyard
(Dernière mise à jour : 19 septembre 2014)

Appelé aussi Crapaud sonneur à ventre jaune, c'est un petit crapaud (50 mm de long) que l'on trouve dans toute l'Europe centrale et méridionale (sauf la Péninsule Ibérique), dans des mares, ornières ou flaques d'eau en forêt. Il cohabite volontiers avec ses congénères et des tritons mais évite d'autres anoures. Il mène une vie aquatique mais chasse à terre insectes, vers, petits crustacés et mollusques.

Le sonneur à ventre jaune présente une face dorsale pustuleuse, gris marron et homochrome au milieu.

Il dévoile sa face ventrale d'un jaune vif taché de noir lorsqu'il est menacé par un prédateur.

Bombina variegata face ventrale
Les couleurs vives de sa livrée ventrale préviennent
l’éventuel prédateur de la présence du venin. (Vue en aquarium)
Selon l'attaque, il prend différentes postures, et libère un liquide visqueux, poison irritant pour les yeux, à l'odeur repoussante. La pupille de l'œil est en forme de cœur.

Tête de Bombina variegata.
La peau verruqueuse montre des pustules venimeuses
Le sonneur à ventre jaune se reproduit en mai, juste après l'hibernation qui a lieu d'octobre à avril. Le mâle chante pour attirer une femelle. L'accouplement se produit lorsque la température de l'eau est supérieur à 11° C. Le mâle enserre la femelle et féconde les œufs éjectés. La femelle accroche aux plantes aquatiques immergées une petite grappe de quelques œufs (1 à 10 maxi). Ceux-ci éclosent après 10 jours.
Le chant du mâle, que l’on pourra écouter dans la vidéo ci-dessous, est destiné à attirer les femelles dans le point d’eau choisi pour la reproduction.
Photos de André Guyard prises dans le Bois d’Aglans lors d’une excursion "Natures et Découvertes" animée par Michel Cottet (mai 2009).
Vidéo : André Guyard.
Le Sonneur à ventre jaune est une espèce vulnzérable protégée. Voir à ce sujet la fiche réalisée par l'Onéma.
Menaces sur les Amphibiens : une vidéo Xenius d'Arte.
15:11 Publié dans Herpétologie, Limnologie-hydrobiologie | Tags : amphibiens | Lien permanent | Commentaires (1) | ![]() Facebook | | |
Facebook | | |
La Bécassine des marais
 La Bécassine des marais
La Bécassine des marais
Gallinago gallinago
(Famille des Scolopacidés)
par André Guyard
La Bécassine des marais se caractérise par un long bec flexible, des ailes pointues et une coloration roux orangé sur la queue. Elle vit et se reproduit dans les zones herbeuses humides, au bord des marais d’eau douce et des étangs ainsi que dans les prairies inondées. Plus petite que la Bécasse, elle est plus grande que la Bécassine sourde.

S’abattant dans la prairie, elle sonde le sol
à la recherche de vers
Elle se nourrit d’invertébrés : vers, mais aussi insectes, crustacés, mollusques, et parfois de graines et de baies, picorant la nourriture sur ou dans le sol. L’extrémité flexible de son bec lui permet de "sentir" la proie tout en sondant la boue. Elle explore également les rives des lacs et étangs, dans la zone des hélophytes.

Perchée sur un piquet, la bécassine va plonger
La femelle pond 3 à 4 œufs qu’elle couve durant 18 à 20 jours. Les poussins sont nourris par les parents pendant la première semaine. Au bout de dix jours, ils sont capables de trouver seuls leur nourriture en parcourant la végétation environnante, mais retournent au nid pour dormir. Ils prennent leur envol à l’âge de 15 à 20 jours.
La vidéo ci-dessous montre une bécassine perchée sur un piquet bordant une prairie humide d’Islande où elle va s’abattre pour sonder le sol à la recherche de vers de terre.
15:01 Publié dans Limnologie-hydrobiologie, Ornithologie | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
Pensées socialistes et conception de la nature
 Pensées socialistes
Pensées socialistes
et conception de la nature
par André Guyard
À Besançon, patrie des socialistes Fourier et Proudhon, en particulier, s'est déroulé du 15 au 17 avril 2009 un colloque consacré à la pensée sociale du XIXe siècle. Il s'agissait d'établir comment s'est constitué puis modifié le partage traditionnel entre la nature d'un côté et la société de l'autre.

Le laboratoire de Recherches philosophiques sur les logiques de l'agir de l'université de Franche-Comté étudie les rapports nature/culture de l'Antiquité à nos jours. Et c'est plus particulièrement à la pensée sociale du XIXe siècle que ce colloque s'est attaché.
Comment les socialismes se sont-ils rapportés au partage nature/société ? Plus généralement, dans quelle mesure la pensée socialiste des XIXe et XXe siècles a-t-elle eu besoin, pour assurer ses bases théoriques, de développer une certaine vision de la nature, des êtres et des lois qui la définissent, ainsi qu'une certaine conception des rapports entre la nature et les activités humaines ?
Bref, y a-t-il eu une (ou des) « philosophie(s) de la nature » créée(s) ou transformée(s) pour leurs besoins par les penseurs qui se réclamaient du projet socialiste au sens large ? Quels furent, le cas échéant, les grands thèmes de cette (ou ces) conception(s) ? En particulier, a-t-elle comporté des aspects «environnementalistes», voire «écologistes» méritant d'être explorés et même réactivés à la lumière des questions contemporaines ?

Laboratoire de Recherches philosophiques sur les logiques de l'agir, Université de Franche-Comté. Tél. 03 81 66 54 42, - arnaud.mace@univ-fcomte.fr
14:54 Publié dans Nature & philosophie | Tags : philosophie, socialisme | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |


