28/07/2012
Des cellules souches dans la rétine
 Des cellules souches dans la rétine
Des cellules souches dans la rétine
(Dernière mise à jour : 2/11/2014)
Dans ce même blog, nous avons évoqué l'emploi de cellules souches embryonnaires pour régénérer la rétine. Ces cellules embryonnaires sont pluripotentes car elles sont à l'origine de toutes les cellules de l'organisme (voir dans ce même blog les articles : Cellules souches et rajeunissement et Élaboration d'une rétine à partir de cellules souches embryonnaires).
Une autre technique est utilisée dans le même but de régénération de la rétine par une autre équipe américaine : des cellules souches découvertes dans la rétine d'individus adultes décédés ouvrent une nouvelle piste de traitement de l’une des premières causes de cécité, la dégénérescence maculaire liée à l’âge, ou DMLA.
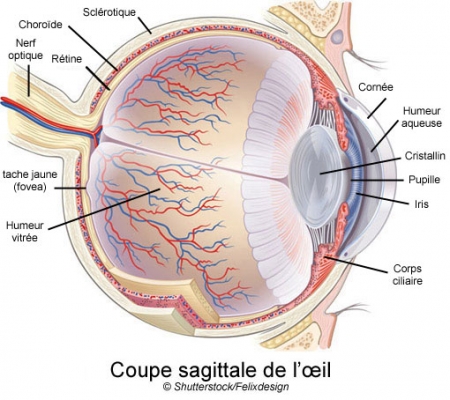
La dégénérescence maculaire liée à l'âge (DMLA) détruit les cellules de l'épithélium pigmentaire de la rétine. Cette couche de cellules qui tapisse le fond de la rétine assure le bon fonctionnement des cellules photoréceptrices de l'œil. Une maladie qui n'est pas négligeable et qui s'aggrave avec l'âge des patients. D'après le journal d'ophtalmologie, 2007, le taux de DMLA dans le monde, s'établit selon l'âge : de 55 à 64 ans à 12,2%, 65 à 74 ans à 18,3%, plus de 74 ans à 29,7% (600 000 patients en France).
Les travaux de l’équipe de Sally Temple, de l’Institut des cellules souches neuronales de Rensselaer, aux États-Unis ouvrent un espoir de remédier à la DMLA. En cultivant sous diverses conditions de telles cellules prélevées sur des donneurs décédés, les biologistes ont mis en évidence, parmi elles, l’existence d’une sous-population de cellules souches multipotentes, c’est-à-dire capables de se différencier en plusieurs types cellulaires – dont les cellules de l’épithélium pigmentaire de la rétine.

La DMLA (dégénérescence maculaire liée à l'âge) entraîne l'apparition d'une ou plusieurs taches noires qui occultent la vision centrale
Cet épithélium est une couche de cellules qui tapisse le fond de la rétine et assure le bon fonctionnement des cellules photoréceptrices de l’œil, les bâtonnets et les cônes. La DMLA, principale cause de malvoyance et de cécité dans les pays industrialisés – elle y touche sept pour cent des personnes de plus de 75 ans –, est due à la disparition progressive de ces cellules. Il n’existe encore aucun traitement pour la forme la plus fréquente, dite DMLA « sèche » ou atrophique.
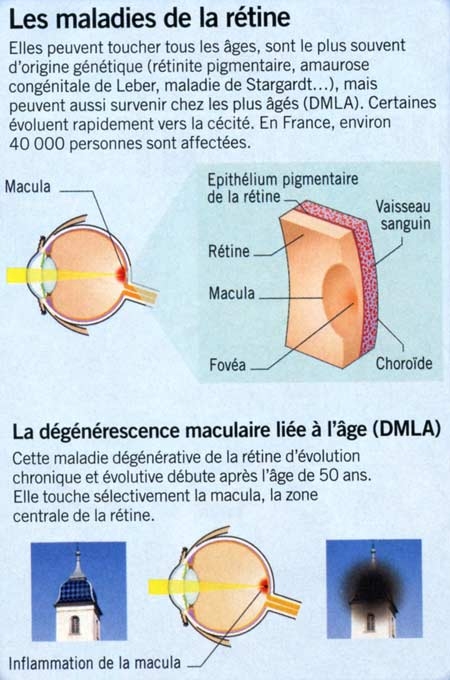
Infographie : Betty Lafon pour Sciences et Avenir
Une piste explorée par plusieurs équipes consiste à greffer dans la rétine des cellules de l’épithélium pigmentaire de la rétine produites en laboratoire à partir de cellules souches embryonnaires (cellules ES) ou de cellules induites à la pluripotence (cellules iPS), c’est-à-dire capables de se différencier en cellules de n'importe lequel des trois feuillets embryonnaires (lors de l’embryogenèse, ces feuillets produisent les organes du futur individu).
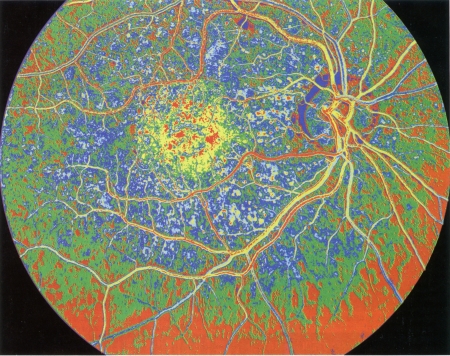
La DMLA (dégénérescence maculaire liée à l'âge) se caractérise par une atteinte de la zone centrale de la rétine, la macula (le cercle jaune vu en rétino-angiographie)
© KOKEL/BSIP
En découvrant des cellules souches dans l’épithélium pigmentaire de la rétine humaine adulte, les biologistes américains ouvrent la voie à une nouvelle piste : en culture, sous certaines conditions, ces cellules souches multipotentes se différencient en cellules de l’épithélium pigmentaire. Existerait-il des conditions similaires qui activeraient leur différenciation dans la rétine des personnes atteintes de la maladie, et ainsi la régénération in situ de l’épithélium défectueux ? Certains animaux à sang froid, comme les amphibiens, ont déjà cette capacité de régénérer leur épithélium pigmentaire et d’autres tissus oculaires lorsque ceux-ci sont abîmés. Prochaine étape : décortiquer le mécanisme qui active la différenciation de ces nouvelles cellules souches – une donnée indispensable pour mettre au point les conditions favorables à la régénération de l’épithélium in situ.
« C’est la première fois que l’on met en évidence des cellules souches dans ce tissu chez l’adulte, commente Olivier Goureau, de l’Institut de la vision, à Paris. Cette piste de réparation endogène semble prometteuse. » Celle de la greffe de cellules de l’épithélium pigmentaire dérivées de cellules pluripotentes n’est pas abandonnée pour autant. Son équipe, qui travaille sur la production de différentes cellules rétiniennes à partir de cellules souches pluripotentes humaines, s’apprête, en collaboration avec le laboratoire ISTEM du génopole d’Evry, à effectuer chez la souris des tests de greffe d’un tel épithélium.
Pour en savoir plus
E. Salero et al., Adult human RPE can be activated into a multipotent stem cell that produces mesenchymal derivatives, Cell Stem Cell, vol. 10, pp. 88-95, 2012.
C. Delcourt, Les troubles de la vision liés à l'âge, Pour la Science, n° 292, pp. 38-45, 2002.
Les cellules souches embryonnaires humaines tiennent leurs promesses (ajout de janvier 2013)
Des patients ont reçu une greffe de cellules souches embryonnaires humaines. Une première mondiale qui offre un espoir de traitement pour cette maladie incurable.
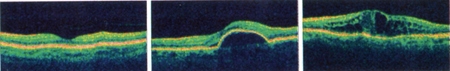
De gauche à droite, tomographie par cohérence optique de la rétine d'une macula normale, d'une rétine atteinte de DMLA et enfin d'un œdème maculaire, une complication rencontrée souvent chez les diabétiques
(CMCR MAISON ROUGE STRASBOURG)
Pour la première fois, une équipe du prestigieux Jules Stein Eye Institute de Los Angeles (États-Unis) a réalisé avec succès, en mars 2012, une greffe de cellules souches embryonnaires humaines (CSEh) chez deux patientes atteintes de dégénérescence maculaire liée à l'âge (DMLA). L'une des patientes souffrait de la forme dite sèche. L'autre d'une affection proche appelée maladie de Stargardt. Ces CSEh, prélevées sur l'embryon aux premiers stades de développement, ont la particularité de se répliquer indéfiniment avant de se différencier pour former plus de 200 types de tissus humains. 50 000 d'entre elles ont été injectées sous la rétine de patientes très malvoyantes pour reconstituer de la rétine. Six mois après, l'une pouvait à nouveau se déplacer seule, l'autre était capable d'utiliser partiellement un ordinateur. Un succès. Mais ces résultats doivent, bien sûr, être confirmés sur la durée. C'est pourquoi l'étude va se poursuivre pendant encore deux ans et inclure vingt-quatre autres patients.
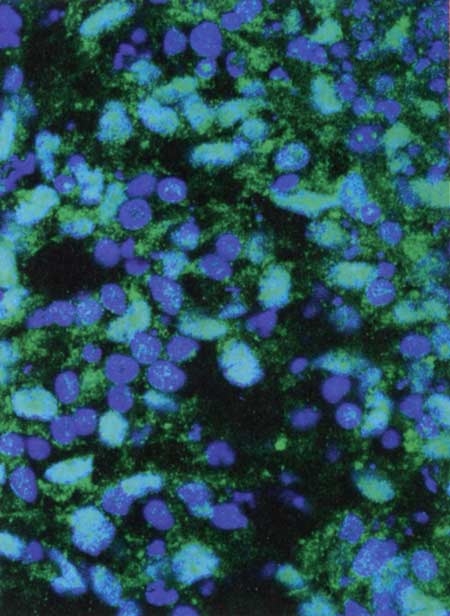
Les greffes de cellules souches embryonnaires humaines (ci-dessus, vues au microscope) sont peut-être la thérapie de l'avenir. Au dernier stade de leur développement, elles donneront un véritable tissu rétinien, aidant à restaurer la vision du patient
© UC IRVINE
S'ils sont avérés, ces résultats constitueront un immense espoir de traitement pour les deux formes de cette maladie dont les symptômes sont une déformation des lignes droites avec l'apparition progressive d'une ou plusieurs taches noires centrales, les scotomes, traduction de la perte de la vision centrale. Moins fréquente (20 % des cas), la forme dite humide est la plus grave. Elle se caractérise par la formation de néovaisseaux sous la rétine, une prolifération due à une production anormale de facteurs de croissance (VEGF : Vascular Endothelial growth factor). En revanche, il n'existe à ce jour aucun traitement pour la forme sèche sans néovascularisation (dite aussi atrophique, plus lente et plus répandue (80 %), les antiVEGF étant inopérants. L'objectif thérapeutique est dans ce cas de stabiliser la destruction progressive des cellules photoréceptrices de la rétine et de bloquer l'inflammation locale. « Plusieurs molécules sont à l'étude et des essais cliniques vont démarrer dans les mois qui viennent », prévoit le Pr Eric Souied, président de l'Association DMLA*.
Face à une affection dont le nombre de cas pourrait doubler d'ici à 2030 en raison du vieillissement de la population, les chercheurs s'intéressent aussi au dépistage. On sait ainsi de longue date que le risque de développer une DMLA est plus important en cas de tabagisme et de surpoids. Plus récemment, des travaux ont été consacrés à la prédisposition génétique et plusieurs marqueurs ont été identifiés (ARMS2, CFH...). Un test de dépistage à partir d'un simple prélèvement salivaire, Macula Risk, est même déjà fabriqué et commercialisé au Canada et sur Internet par la firme Artic DX. Toutefois, son usage reste controversé et surtout prématuré comme l'a précisé un communiqué spécial émis par l'American Academy of Ophtalmology (AAO) en novembre 2012. « À l'avenir, ces tests pourront probablement aider à mieux traiter les patients à haut risque en permettant des traitements adaptés, a ainsi précisé le Dr Edwin Stone, responsable du groupe de travail de l'AAO sur la prédisposition génétique. « Mais les preuves d'un réel bénéfice pour le patient manquent encore. » Pour l'heure, en France, ce test est depuis peu en cours d'évaluation au centre hospitalier intercommunal de Créteil (Val-de-Marne) selon un protocole rigoureux, et uniquement, auprès de patients présentant des antécédents familiaux. L'équipe de Créteil poursuit par ailleurs un projet de génétique appliquée. « Nous avons identifié des marqueurs génétiques prédictifs de sévérité, détaille le Pr Souied. D'ici à cinq ans, nous espérons pouvoir adapter notre prise en charge au profil de chacun. » Un premier pas de soin personnalisé de la DMLA.
*N° vert 0.800.880.66.
Source :
Sylvie Riou-Millot (2013) . - Bien voir - Sciences et Avenir n° 792, février 2013, pp. 46-57.
Les cellules souches induites adultes (iPS) entrent dans la danse (ajout de mars 2013)
Dans le traitement de la DMLA, les premiers essais cliniques impliquant des cellules iPS devraient démarrer au Japon en 2013 au centre hospitalier de Kobe. Cette opération, qui se pratique déjà avec les CSEh (voir plus haut et également le dossier « Vision », Sciences et Avenir n° 792, février 2013) consistera à injecter des iPS différenciées directement dans l'œil du patient afin de reconstituer les cellules abîmées.
Peut-on envisager de déployer cette technique pour des interventions nécessitant de plus importantes réparations dans des tissus nécrosés ? Dans le cas de la rétine, le nombre de cellules iPS à injecter est relativement faible. Mais s'il est possible d'envisager de greffer en surface de l'œil quelques milliers de cellules rétiniennes au millimètre carré, sera-t-il possible de réparer en profondeur un trouble cardiaque comme l'ischémie qui détruit plusieurs dizaines de milliards de cellules ? Sera t-il possible de produire autant de cellules, et à quel coût ? Autant de questions qui restent sans réponse. Pour toutes ces raisons, il semble illusoire - du moins pour l'heure - d'envisager que les iPS puissent ouvrir la voie à une médecine totalement personnalisée où l'on pourra soigner chaque patient à partir de ses propres cellules expurgées de leurs défauts.
Une greffe relance l'espoir dans la DMLA (ajout du 2 novembre 2014)
Une première mondiale : l'équipe menée par Yasuo Kurimoto, du Kobe City Médical Center Général Hospital au Japon a réalisé un implant de tissu rétinien à partir de cellules souches pluripotentes induites (iPS).
Le 12 septembre 2014, une Japonaise de 70 ans atteinte de DMLA a reçu une greffe d'un tissu rétinien conçu à partir de cellules souches pluripotentes induites (IPS). Une première mondiale.
Même s'il est trop tôt pour évaluer le résultat, la patiente a déclaré, le lendemain, que sa vue était plus "brillante". Les iPS en question étaient des cellules souches obtenues à partir de cellules adultes différenciées — ici de peau de la patiente — puis reprogrammées en cellules de rétine. L'équipe japonaise a implanté un feuillet de 1,3 sur 3 mm d'épithélium rétinien dans l'œil de la patiente.
« Cette excellente équipe a réalisé ce que nous appelons "une preuve de concept" », commente Marc Peschanski, directeur scientifique d'I-Stem au génopôle d'Évry (Essonne). Nous attendons les résultats dans les deux ans. » Un éventuel succès pourrait cependant être difficile à étendre au plus grand nombre. « Le procédé n'étant pas du tout industrialisé, nous allons nous retrouver devant un problème éthique : nous aurons le traitement mais pas les moyens de l'appliquer. »
Source : Article de Sciences et Avenir, n° 813, novembre 2014 p. 28.
Une piste autre que les cellules souches : Un collyre anti-cholestérol pour ralentir la DMLA
Une possibilité de ralentir la maladie vient d'être explorée par une équipe de chercheurs américains dirigée par Rajendra Apte, du département d'ophtalmologie de l'École de médecine de l'université Washington à Saint-Louis (Missouri).
Principale cause de malvoyance chez les personnes âgées, la DMLA pourrait être prévenue par des gouttes oculaires évacuant le cholestérol de l'œil. Un essai prometteur chez le rat.
Les injections dans l'œil utilisées pour traiter localement la DMLA pourraient céder la place à un simple collyre. C'est en effet la piste ouverte par des chercheurs américains qui publient une étude dans Cell Metabolism. Selon ce travail, il serait possible de ralentir la prolifération anormale des vaisseaux qui caractérise cette affection en régulant le métabolisme du cholestérol à l'intérieur de l'œil. L'approche qui n'a encore été testée que chez la souris — consisterait à cibler avec un collyre les cellules chargées d'évacuer le cholestérol. Celui-ci retournerait ainsi dans la circulation sanguine et ne s'accumulerait plus dans l'œil, empêchant la maladie de progresser. Cette idée inédite vient compléter l'arsenal des techniques en développement pour préserver ou restaurer la vision (lire Sciences et Avenir, n° 793, février 2013).
Rappelons que le cholestérol est un lipide impliqué dans de nombreux processus biochimiques. Mais quel rapport peut-il exister entre le cholestérol et le développement de vaisseaux sanguins de la rétine ? Il n'y a pas de lien entre DMLA et taux sanguin de cholestérol. La clef s'appelle en fait macrophages. Cette catégorie de cellules immunitaires joue en effet un rôle primordial dans l'élimination du cholestérol de l'œil. Or, les macrophages deviennent moins performants avec l'âge. Il en résulte des dépôts lipidiques qui entretiennent un foyer inflammatoire. Celui-ci favorise le développement de vaisseaux anormaux sous la rétine, responsables d'altérations sévères de la vision centrale. Pour l'heure, on ignore les mécanismes précis qui conduisent ces « vieux » macrophages à induire cette prolifération vasculaire. En revanche, de récents travaux ont montré qu'ils comptaient moins d'ABCAl, une protéine « transporteuse » permettant d'évacuer le cholestérol. Pour preuve, de « jeunes » macrophages dépourvus de ce même transporteur se comportent effectivement comme de « vieux » macrophages, favorisant une vascularisation anormale. D'où l'idée des chercheurs de « booster » l'expression d'ABCAl dans ces cellules afin qu'elles puissent se débarrasser de leur cholestérol et trouver la capacité à réguler la croissance vasculaire.
Pour ce faire, l'équipe de Rajendra Apte, du département d'ophtalmologie de l'École de médecine de l'université Washington à Saint-Louis (Missouri), a utilisé des gouttes ophtalmiques contenant un agoniste du LXR (Liver X Receptor). Cet agent stimule l'action d'un récepteur initialement découvert dans le foie et impliqué dans le métabolisme des lipides. Des études préalables ont en effet montré qu'il augmente la production du transporteur ABCA1 par les macrophages. Et les résultats des essais ont été encourageants : ainsi « dopées », les « vieilles » cellules se sont remises à fabriquer cet indispensable transporteur dans les mêmes proportions que les « jeunes ».
Restait à évaluer cette stratégie sur des souris chez lesquelles on a induit, sous l'effet d'un laser, une croissance anormale des vaisseaux sous-rétiniens, reproduisant ainsi ce que l'on observe chez les patients souffrant de DMLA. Là encore, les résultats ont été positifs. Administré en collyre, l'agoniste du LXR a permis de réduire significativement la prolifération vasculaire chez les souris traitées, les macrophages défaillants parvenant à nouveau à évacuer efficacement le cholestérol.
Il pourrait s'agir d'un progrès thérapeutique majeur
II faut désormais poursuivre ces recherches pour confirmer ces bons résultats, et surtout les appliquer à l'homme, ce qui prendra encore de longues années. S'ils se révélaient concluants, il s'agirait d'un progrès thérapeutique majeur dans la mesure où la fréquence de la DMLA augmente avec l'âge, représentant la principale cause de malvoyance chez les personnes de plus de 50 ans. Selon les chercheurs, « intervenir avant que la maladie ne soit à un stade avance avec des agents efficaces capables de stimuler la sortie du cholestérol de l'œil pourrait empêcher la progression de la maladie. Cette stratégie pourrait être déployée préventivement ».
Source : Marc Gozian Sciences et Avenir, n° 795, mai 2013, pp. 78-79.
12:29 Publié dans Biologie, Médecine | Tags : cellules souches, cellules souches embryonnaires, médecine régénératrice, rétine, thérapie | Lien permanent | Commentaires (3) | ![]() Facebook | | |
Facebook | | |
Élaboration d'une rétine en culture à partir de cellules souches embryonnaires
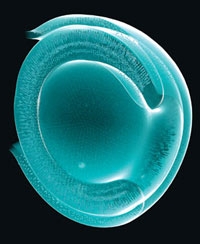 Élaboration d'une rétine en culture
Élaboration d'une rétine en culture
à partir de cellules souches embryonnaires
par Yoshiki Sasai[1]
Lors du développement embryonnaire, dans l'utérus, un petit amas de cellules identiques donne naissance aux divers types de cellules du corps humain. Elles s'arrangent en structures variées et finissent par former les organes. Un "programme" interne dirige cette progression depuis des éléments simples jusqu'à des tissus de forme et de taille appropriées.
Les biologistes aimeraient reproduire le développement embryonnaire en laboratoire, à la fois pour mieux comprendre ses mécanismes et pour élaborer des moyens le réparer et remplacer des tissus endommagés. Le succès est peut-être proche : de récents progrès laissent envisager la "culture d'organes" de remplacement à l'extérieur du corps ; ils pourraient être disponibles pour les opérations chirurgicales d'ici dix ans.
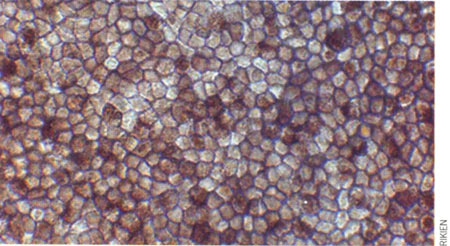
Cellules épithéliales pigmentées de la rétine
Mon optimisme se fonde sur des études sur les cellules souches – des divers types de cellules. Nous avons montré que des cultures de cellules souches peuvent donner naissance à une rétine ; cette structure clef de l'œil traduit la lumière en signaux électriques et chimiques, qui sont ensuite transmis au cerveau. Dans d'autres travaux, nous avons fait pousser du tissu cérébral (cortex) et une partie de l'hypophyse (une petite glande située à la base du cerveau). Pour ce faire, nous avons placé une mince couche de cellules dans une boîte de Pétri, où nous avons ajouté un cocktail de molécules présentes dans l'organisme. Ces cellules se sont développées en une structure tridimensionnelle. Nous espérons que du tissu rétinien produit de la sorte permettra de traiter plusieurs maladies de l'œil, telle la dégénérescence maculaire (la macula est la partie centrale de la rétine.
La formation de la rétine est un phénomène auto-organisé, fondé sur un programme interne des cellules.
À l'origine, nous cherchions à mieux comprendre la formation de la rétine. Nous savions qu'elle provient d'une partie du cerveau embryonnaire nommée diencéphale. Durant les premiers stades du développement embryonnaire, un segment du diencéphale s'étend pour former la vésicule optique, une structure en forme de ballon. Celle-ci s'invagine, formant la "cupule optique", qui deviendra la rétine (voir figure ci-dessous).
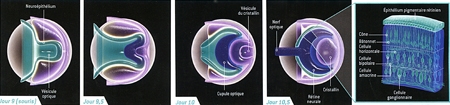
Naissance de la rétine chez l'embryon
L'œil se forme à partir d'un petit amas de cellules embryonnaires. Au début, une couche de tissu, le neuroépithélium, se replie vers l'extérieur, donnant naissance à la vésicule optique (jour 9). La paroi de ce bourgeon s'incurve ensuite vers l'intérieur (jour 9,5), et la vésicule du cristallin se développe (jour 10). Une partie de la vésicule optique engendre la cupule optique, à l'origine de la rétine et du nerf optique (jour 10,5). La rétine contient trois couches distinctes de cellules (à l'extrême droite), l'une d'elles étant constituée des photorécepteurs (les bâtonnets et les cônes). La rétine représentée ici, d'une taille de 250 micromètres est celle d'une souris. La rétine humaine est similaire, mais plus grosse, et sa formation est plus longue.
Depuis plus d'un siècle, les biologistes débattent sur le mécanisme de formation de la cupule optique. Une question importante concerne le rôle des structures voisines, telles que le cristallin et la cornée. Certains chercheurs pensent que le cristallin façonne la cupule optique en exerçant une pression sur la vésicule, tandis que d'autres affirment que la cupule peut se former sans lui et sans les autres tissus voisins.
Il est difficile d'observer les mécanismes physiologiques sous-tendant le développement sur des animaux vivants. Il y a environ dix ans, nous avons donc décidé de reproduire le développement de l'œil dans une boîte de Pétri. Pour ce faire, nous avons utilisé des cellules souches embryonnaires, que nous avons exposées à diverses substances chimiques connues pour être impliquées dans la formation de l'œil. Les cellules souches embryonnaires constituent le type le plus immature de cellules souches. Elles sont capables de se différencier en tous les types cellulaires du corps, des neurones jusqu'aux cellules musculaires.
Aucune technique existante ne permettait d'engendrer des organes à partir de cultures de cellules souches. Des essais avaient été réalisés en plaçant les cellules sur une sorte d'échafaudage artificiel, qui imitait la forme de l'organe ciblé (en l'occurrence une vessie ou un œsophage), mais ils n'avaient remporté qu'un succès mitigé. Nous avons donc tenté une approche différente.
En 2000, nous avons élaboré une méthode pour transformer des cellules souches embryonnaires de souris en différents types de neurones. Nous avons ensuite placé une monocouche de ces cellules souches dans une boîte de Pétri, avec des cellules dites nourricières : ces dernières transmettaient des signaux chimiques déclenchant la différenciation des cellules souches embryonnaires. Cette couche mince ne reproduisait pas les organes tridimensionnels réels, mais nous désirions déjà savoir si les molécules sélectionnées suffisaient à obtenir les types particuliers de neurones apparaissant précocement lors du développement de l'œil.
Après des débuts difficiles, nous avons développé une nouvelle méthode en 2005, qui nous a permis de dépasser le stade bidimensionnel : nous avons créé une suspension de cellules souches dans un milieu liquide, qualifiée de culture flottante. L'intérêt d'une telle culture tridimensionnelle est double. Tout d'abord, un agrégat de cellules est mieux à même de prendre la forme des tissus s'il est tridimensionnel que s'il est plat. Ensuite, la formation de structures complexes requiert de multiples communications entre cellules, et ces dernières interagissent plus facilement dans une culture tridimensionnelle.
Nous avons placé des cellules en suspension dans de petits réservoirs - comptant chacun en moyenne 3 000 cellules - au sein d'une boîte de Pétri. Initialement séparées les unes des autres, les cellules se sont liées avec leurs voisines. Nous avons ensuite déclenché la différenciation de ces petits agrégats de cellules en des progéniteurs neuronaux (des cellules neuronales immatures) présents à l'avant du cerveau. Les cellules ont alors commencé à échanger des signaux.
Trois à quatre jours plus tard, elles se sont organisées spontanément en une sphère creuse formée d'une couche cellulaire ; on parle de neuroépithélium. Nous avons nommé SFEBq cette méthode de culture (pour Serum free floating culture of embryoid body-like aggregate with quick reaggregation, littéralement culture sans sérum flottante d'agrégats embryonnaires se réagrégeant rapidement).
Dans l'embryon, les cellules neuroépithéliales forment des structures cérébrales spécifiques, après avoir reçu des signaux chimiques externes. L'un de ces signaux déclenche le développement du diencéphale, qui engendrera la rétine et l'hypothalamus (une aire cérébrale contrôlant l'appétit et de nombreuses fonctions physiologiques fondamentales). Après avoir fait s'agréger les cellules en sphères, nous avons provoqué leur différenciation en progéniteurs rétiniens - les précurseurs des cellules rétiniennes matures. Pour ce faire, nous avons ajouté à notre culture un mélange de protéines, incluant celles qui assurent ce rôle chez l'embryon.
Quelques jours plus tard, des structures semblables à la vésicule optique ont spontanément bourgeonné sur les sphères, avant de changer de forme : la structure finale ressemblait à la cupule optique de l'œil embryonnaire (voir figure ci-dessous). Comme la cupule optique des animaux vivants, cette structure issue de cellules souches embryonnaires se composait de deux parois (deux épithéliums), l'une extérieure et l'autre intérieure ; c'est cette dernière qui est à l'origine de la rétine.
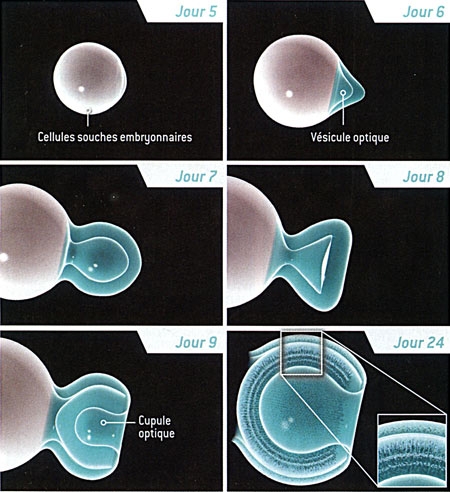
Formation de la rétine à partir d'une cellule souche
La formation d'une rétine à partir d'une culture de cellules souches embryonnaires ressemble à ce qui se produit dans l'utérus. Les cellules s'agrègent et commencent à former la vésicule optique "primitive" environ cinq jours après avoir été mélangées avec des substances nommées facteurs de croissance. Cette vésicule gonfle, puis forme la cupule optique. Le 24e jour, toutes les couches de la rétine sont visibles.
Ainsi, une structure ordonnée est née de la seule agrégation de cellules souches dans un récipient. Contrairement à ce qui se passe chez l'embryon, il ne se formait pas de cristallin ou de lentille au voisinage de la cupule optique. Nos travaux montrent donc qu'aucune force exercée par des tissus voisins (tel le cristallin) n'est nécessaire à la formation de la protorétine. Au moins in vitro, c'est un phénomène auto-organisé, fondé sur un programme interne des cellules. Ce programme est encodé dans leur ADN, et nous travaillons à préciser ses mécanismes d'action.
L'apparition spontanée d'une structure stratifiée
Le développement normal de la rétine, tel qu'on l'observe chez les embryons, s'est poursuivi dans nos cultures. En deux semaines supplémentaires, la cupule optique a grandi jusqu'à environ deux millimètres de diamètre, et l'épithélium monocouche interne est devenu une structure stratifiée, contenant les six catégories de cellules d'une rétine naturelle après la naissance. L'une des couches extérieures de cette structure était constituée de photorécepteurs et l'autre de cellules dites ganglionnaires, qui, dans le corps, relient la rétine au cerveau. Entre les deux se trouvaient plusieurs couches de cellules de liaison, nommées interneurones.
De nombreuses questions demeurent, notamment sur la façon dont une boule de cellules entre dans un programme de différenciation, qui aboutit à des tissus distincts. Tout au long du développement embryonnaire, des formes complexes apparaissent spontanément à partir d'amas de matière homogène - on parle de brisure de symétrie. En l'absence de ce phénomène, les divisions cellulaires de l'œuf fécondé n'engendreraient qu'une masse indifférenciée de cellules. Nos cultures de cellules souches embryonnaires qui s'auto-organisent devraient aider à mieux comprendre les mécanismes en jeu dans les brisures de symétrie.
On cherche également à mieux comprendre comment s'effectue le modelage de la cupule optique à partir d'une simple couche de cellules (l'épithélium rétinien). La force qui s'applique sur les cellules et la rigidité varient dans l'épithélium. En mesurant in vitro la direction de la force et la rigidité du tissu en différents endroits, nous avons découvert que la cupule optique se forme en plusieurs étapes. Tout d'abord, la rigidité de la protorétine diminue, ce qui accroît sa flexibilité. Dans le même temps, les cellules qui se trouvent à la jonction de l'épithélium (la boule dont a bourgeonné la rétine) et de la protorétine adoptent une forme en coin. Finalement, la protorétine commence à se replier vers l'intérieur en raison de sa rapide extension. Nous avons appliqué les conditions mécaniques correspondantes à une simulation sur ordinateur, et la forme de la cupule optique est apparue !
Pour y voir plus clair...
Nos travaux aideront-ils à lutter contre les troubles oculaires humains ? Nous avons progressé dans cette voie. En particulier, mon équipe a récemment recréé une cupule optique et un tissu neuronal à couches multiples à partir de cellules souches embryonnaires humaines. La même méthode de culture devrait être applicable à des cellules souches humaines dites pluripotentes induites - des cellules matures et différenciées dont on a « inversé » le développement pour qu'elles se comportent comme des cellules souches embryonnaires. Nous avons également inventé une méthode fiable de cryoconservation, qui permet de stocker du tissu rétinien issu de cellules embryonnaires humaines dans de l'azote liquide.
Ces travaux promettent des applications médicales. Par exemple, nous pourrions créer des rétines artificielles, qui aideront à étudier les maladies de l'œil et, peut-être, à développer des médicaments et des thérapies géniques pour inverser la dégénérescence rétinienne.
Trois catégories de dégénérescence rétinienne pourraient bénéficier de nos recherches : la dégénérescence maculaire, la rétinopathie pigmentaire et le glaucome. Ces maladies touchent des millions d'individus à travers le monde et altèrent des couches différentes de la rétine.
Dans la dégénérescence maculaire, un tissu nommé épithélium pigmentaire rétinien est endommagé : ce tissu tapisse le fond de la rétine et supporte les photorécepteurs, qui se détériorent également, en particulier dans la région centrale de la rétine.
Dans la rétinopathie pigmentaire, les bâtonnets (un type de photorécepteurs) disparaissent progressivement pendant plusieurs années. La maladie se manifeste d'abord par une cécité nocturne, ou héméralopie, puis le champ visuel se réduit jusqu'à se limiter à une petite zone au centre, avant que le patient ne devienne totalement aveugle.
Enfin, le glaucome endommage les cellules ganglionnaires, qui relient la rétine au cerveau via le nerf optique.
De ces trois maladies, la dégénérescence maculaire semble la plus susceptible d'être traitée par une thérapie cellulaire. Pour obtenir les cellules nécessaires au remplacement de l'épithélium pigmentaire rétinien endommagé, on transforme des cellules souches embryonnaires humaines ou des cellules souches pluripotentes induites, au sein de cultures conventionnelles ou flottantes. Des essais cliniques à petite échelle ont débuté aux États-Unis et sont prévus dans d'autres pays : les cellules d'épithélium pigmentaire issues de cellules souches sont injectées sous la rétine avec une fine aiguille, afin de remplacer au moins une partie du tissu endommagé.
Pour la rétinopathie pigmentaire, la thérapie cellulaire est une perspective plus lointaine. À l'inverse d'une culture classique, notre méthode peut engendrer une couche dense de bâtonnets facilement transplantable. En revanche, ces photorécepteurs doivent s'intégrer dans le circuit neuronal de l'œil - ce qui n'était pas nécessaire pour l'épithélium, simple tissu de soutien. Ainsi, ils doivent se connecter à un autre type de cellules sensorielles, les cellules bipolaires, et nous ne savons pas encore comment réaliser cette connexion.
Le glaucome pourrait être la plus difficile des trois maladies à traiter par thérapie cellulaire. Des cultures de cellules souches embryonnaires peuvent produire les cellules ganglionnaires nécessaires, mais dans l'œil postnatal, le nerf optique ne se reforme pas spontanément. Autrement dit, une fois les cellules ganglionnaires transplantées, on ne sait pas connecter leurs axones (les prolongements des neurones qui forment le nerf optique) aux cellules cérébrales.
Notre méthode a décuplé les possibilités des tissus formés à partir de cellules souches embryonnaires. Reste à découvrir ce qu'elle peut nous apprendre sur les mécanismes qui conduisent d'une cellule unique à un organe aussi complexe que l'œil...
BIBLIOGRAPHIE
Y. Sasai (2013). – Une rétine en culture. Pour la Science, n° 426 avril 1993, pp. 58-63.
T. Nakano et al. (2012). - Self-formation of optic cups and storable stratified neural retina from human ESCs, Cells Stem Cell, vol. 10, pp. 771-785.
D Schwartz et al. (2012). - Embryonic stem cell trials for macular degeneration : a preliminary report, Lancet, vol. 379, pp. 713-720, 2012.
M. Eiraku et al. (2011). - Self-organizing optic-cup morphogenesis in three-dimensional culture, Nature, vol. 472, pp. 51-56.
Les alternatives thérapeutiques aux cellules souches
par Serge Picaud et José Sahel, Institut de la vision, Paris
Si les cellules souches ouvrent de nouvelles perspectives thérapeutiques pour les patients aveugles, une autre technique en est déjà au stade commercial : celle des prothèses rétiniennes. Ces dispositifs visent à stimuler artificiellement une rétine ayant perdu ses photorécepteurs. Les images, filmées par une caméra fixée sur une paire de lunettes, sont d'abord transformées en matrices d'impulsions électriques. Celles-ci sont ensuite transmises à des électrodes implantées sur la rétine résiduelle (voir la figure ci-dessous).
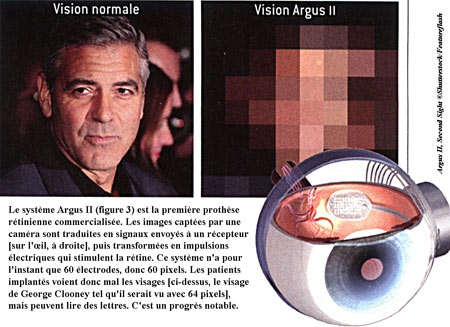
Commercialisée depuis deux ans en Europe, la première prothèse rétinienne opérationnelle a reçu l'autorisation de mise sur le marché aux États-Unis en février 2013. En France, quatre patients aveugles ont participé aux essais cliniques. Cependant, les images perçues ne sont constituées que de 60 points ou pixels, puisque l'implant n'a que 60 électrodes : c'est insuffisant pour bien voir une image complexe, tel un visage, mais suffisant pour une image simple, de sorte que certains patients sont capables de lire des lettres d'environ 10 centimètres de hauteur.
De nombreux chercheurs tentent d'augmenter le nombre de pixels, chaque électrode devant activer une zone disjointe de sa voisine. Ainsi, à l'Institut de la vision, on poursuit plusieurs objectifs : le développement de nouvelles formes tridimensionnelles pour les implants, avec l'ESIEE (École supérieure d'ingénieurs en électrotechnique et électronique) et le CEA; l'utilisation de matériaux semi-conducteurs différents, tels le graphène et le diamant (projet européen NEUROCARE) ; l'amélioration du codage des informations visuelles.
Une piste alternative, la thérapie optogénétique, est inspirée d'algues unicellulaires et de bactéries dotées de protéines photosensibles. Ces protéines sont des canaux ioniques dont l'ouverture est contrôlée par la lumière. L'idée est d'insérer le gène qui les code dans les neurones non photosensibles de la rétine, qui pourraient alors être activés par la lumière.Ainsi, chaque cellule produisant les protéines jouerait le rôle d'un pixel. Ces protéines étant moins performantes que nos pigments visuels, les aveugles devront porter des lunettes rehaussant la luminance.
Ainsi, dans le cadre du projet européen RETICIRC, nous avons rendu la vue à des souris aveugles grâce à une protéine bactérienne. Nous avons ensuite montré que cette protéine permet l'activation de cellules rétiniennes humaines par la lumière, grâce à des cultures de cellules prélevées post mortem. Avant de passer à une application clinique, nous devrons vérifier que la thérapie génique visant à faire exprimer la protéine bactérienne n'entraîne pas d'inflammation ou de rejet chez le primate.
[1] Yoshiki SASAI est directeur du groupe d'organogenèse et de neurogenèse au Centre de biologie du développement du RIKEN, à Kobe, au Japon. Plus d'information sur Y. Sasai et ses recherches.
12:05 Publié dans Biologie, Médecine | Tags : cellules souches embryonnaires, rétine, culture organotypique, macula, dmla, rétinopathie pigmentaire, glaucome, prothèse rétinienne | Lien permanent | Commentaires (2) | ![]() Facebook | | |
Facebook | | |
27/07/2012
Controverse acide sur les cellules souches
 Controverse acide sur les cellules souches
Controverse acide sur les cellules souches
Un article paru dans la revue "Sciences & Vie" de mai 2014 fait état de l'obtention de cellules souches par choc acide à la suite de travaux d'une équipe japonaise, résultats publiés dans "Nature" de janvier 2014. (Nature 01/2014; 505(7485):641-7.)
Dans "Pour la Science" en ligne (avril 2014), un article de Yvan Pandelé[1] fait le point sur cette publication. Ci-dessous la publication in extenso de cet article.
La récente découverte d’une méthode pour fabriquer des cellules souches par choc acide a suscité l’enthousiasme de la communauté scientifique. Avant d’être gravement mise en doute...
La nouvelle avait fait grand bruit. En janvier dernier, des chercheurs japonais et américains annonçaient avoir réussi à transformer des cellules de souris adultes en cellules souches par une nouvelle méthode : la soumission à un choc acide. Nommées STAP (Stimulus-triggered acquisition of pluripotency), les cellules souches obtenues seraient pluripotentes, c'est-à-dire capables de se différencier en de nombreux types cellulaires une fois réinjectées chez l’embryon.
Assez vite cependant, les publications concernées – un article et une lettre parues dans la revue Nature le 30 janvier dernier – ont suscité des doutes. Des chercheurs ont pointé des détails problématiques : incohérence méthodologique, images modifiées ou reprises de la thèse de doctorat du premier auteur… Des observations qui, mises bout à bout, commençaient à faire désordre.
Plus grave, aucune équipe de recherche n’est jusqu’à présent parvenue à répliquer les résultats. On s’est également aperçu que les cellules STAP produites ne provenaient pas de la souche de souris mentionnée dans l’article, mais de deux autres souches. Sur son blog de recherche, Paul Knoepfler, spécialiste des cellules pluripotentes à l’Université de Californie à Davis, a publié une série de sondages informels qui semblent indiquer un scepticisme croissant au sujet de l’existence des cellules STAP.
Une découverte prometteuse
La méthode découverte par Haruko Obokata et ses collègues semblait pourtant très prometteuse, combinant une technique simple – modifier l’acidité du milieu de culture – et des résultats encourageants. En effet, les cellules STAP présenteraient un potentiel de différenciation encore supérieur aux cellules pluripotentes induites (IPS) obtenues par reprogrammation génétique, récompensées par un prix Nobel de médecine en 2012. Les enjeux sont forts : la thérapie cellulaire à base de cellules souches permettra peut-être de traiter de nombreuses maladies, en remplaçant les tissus ou les organes lésés.
Certains des auteurs impliqués dans la découverte des cellules STAP se sont exprimés publiquement. Teruhiko Wakayama, chercheur à l’Université de Yamanashi, s’est prononcé en faveur d’un retrait des articles : le 10 mars dernier, il déclarait avoir perdu confiance dans le travail effectué et préférer approfondir les recherches en vue d’une éventuelle republication. Charles Vacanti, auteur sénior et chercheur à la Faculté de médecine de Harvard, continue pour sa part de défendre la validité de l’étude. Le 20 mars dernier, il mettait à la disposition de la communauté une version détaillée du protocole employé, afin de faciliter d’éventuelles réplications.
Des accusations de fraude
Mais les critiques se focalisent surtout sur le premier auteur, Haruko Obokata, une jeune biologiste (30 ans) responsable d’équipe au Riken, un prestigieux institut de recherche japonais. À la suite des suspicions émises, le Riken a rapidement lancé une enquête interne. Les conclusions, parues à la fin du mois de mars, sont sévères vis-à-vis de Haruko Obokata, qui se voit accusée d’avoir manipulé volontairement certaines données annexes, se rendant coupable de fraude scientifique (scientific misconduct). Dans une conclusion au vitriol, les rapporteurs estiment le protocole expérimental difficile à suivre – donc à reproduire – et vont jusqu’à déplorer « le manque total d’intégrité et d’humilité » de la chercheuse.
Violemment mise en cause par son propre institut et au centre d’un ouragan médiatique, Haruko Obokata a répliqué mercredi 9 avril dans une conférence de presse. Visiblement très éprouvée, elle s’est excusée pour les erreurs commises, mais plaide la bonne foi et maintient la validité des résultats de son équipe. « Le phénomène des cellules STAP est une réalité que j'ai vérifiée à plus de 200 reprises », affirme-t-elle, ajoutant que le protocole a été répliqué par une tierce personne. Le Riken a confirmé cette dernière information tout en minimisant les résultats obtenus, affirmant qu’ils ne constituaient pas une réplication complète. Le chercheur en question, également membre de l'institut japonais, semble vouloir conserver l’anonymat. Jusqu’à ce que ses résultats soient confirmés ?
Un retrait des articles ?
La question de l’existence des cellules STAP reste donc ouverte. Pour l’heure, la revue Nature n’a pas annoncé de retrait des publications mises en cause, et continue de couvrir l’affaire sur son blog d’actualité. Quant aux réactions des institutions de recherche, elles sont contrastées. Si le Riken a joué la transparence et a mis beaucoup d’ardeur à se désolidariser de H. Obokata, l’Université Harvard est pour sa part restée silencieuse. Toujours est-il qu’en l’absence de demande de retrait de la part des institutions scientifiques ou des principaux auteurs, les publications restent, jusqu’à nouvel ordre, valides.
Ces dernières années, on observe une augmentation du nombre de rétractations d’articles scientifiques. Une revue conduite en 2012 sur la base PubMed, qui référence un très grand nombre d’articles dans le champ biomédical, a montré que les deux tiers des rétractations étaient dues à des cas de fraude scientifique, c'est-à-dire du plagiat (ou auto-plagiat) ou de la manipulation volontaire de données. Cette hausse pourrait toutefois révéler, plutôt qu’une intensification des mauvaises pratiques, une plus grande sensibilité du système de détection.
En cas de fraude avérée, le scandale est généralement à la mesure des espoirs suscités. En 2005, dans un article publié dans Science, une équipe de recherche coréenne avait affirmé avoir créé des cellules souches embryonnaires à partir de clones humains… Las, la découverte s’était révélée factice et l’article avait été retiré dans un scandale retentissant. Espérons que l’affaire des cellules STAP ne connaîtra pas la même issue.
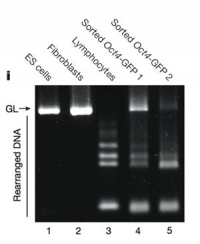
© Haruko Obokata
Cette figure, qui présente le résultat d'une électrophorèse sur gel, a été falsifiée (le couloir 3 correspond à un gel différent des autres couloirs). Il s'agit d'un des deux cas de fraude scientifique identifiés par l'institut de recherche où travaille Haruko Obokata.
Pour en savoir plus
M.-N. Cordonnier, Des cellules souches produites par choc acide, Pour la Science, en ligne le 8 février 2014.
H. Obokata et al., Stimulus-triggered fate conversion of somatic cells into pluripotency, Nature, vol. 505, pp. 641-647, 30 janvier 2014.
H. Obokata et al., Bidirectional developmental potential in reprogrammed cells with acquired pluripotency, Nature, vol. 505, pp. 676-680, 30 janvier 2014.
F. C. Fang et al., Misconduct accounts for the majority of retracted scientific publications, PNAS, 109(42), 2012.
D. Fanelli, Why growing retractions are (mostly) a good sign, PLOS Medicine, 10(12), 2013.
[1] Yvan Pandelé est journaliste à Pour la Science.
09:15 Publié dans Actualité des Sciences, Médecine | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
24/07/2012
L'agroterrorisme dans nos assiettes
Alerte à tous les futurs cancéreux
que nous sommes !

« J'ai autrefois craché le sang à la suite de traitements chimiques avec lesquels j'empoisonnais moi-même les autres… Tout le monde sait que les produits chimiques sont cancérigènes. » 30 juillet 1972, 20 h, première chaîne de télévision, le présentateur Philippe Gildas relate le congrès international de la défense de la Nature, tenu à Fleurance (Gers), dont le maire était alors l'illustre Maurice Mességué.
Chaque jour, chaque fois que vous ingérez un aliment, une boisson, vous risquez de contracter un cancer. L'agriculture et son complice capitaliste l'agro-alimentaire nous tuent à petit feu. C'est probablement le plus grand scandale du troisième millénaire.
Ne serait-il pas judicieux d'étendre le délit de risque causé à autrui (articles 223-1 & 2 du code pénal) aux atteintes sanitaires des consommateurs, victimes involontaires, et non seulement des exploitants volontaires ?
http://www.wat.tv/video/son-cancer-aux-pesticides-50ch5_2...
Morts de kamikazes, et nous ? Car ce n'est pas QUE la dose qui fait le poison, mais aussi la durée de l'empoisonnement :
http://videos.tf1.fr/infos/2010/agriculteurs-victimes-du-...
http://www.dailymotion.com/video/xqdpak_la-mort-est-dans-...
Alors qu'il est déjà trop tard parce que tous les sols et bien des corps sont irréversiblement contaminés, ici et là, le combat ne fait que commencer
Comme en Inde :
http://www.youtube.com/watch?v=Tq4EjQDiPIw
Ou en Argentine :
http://www.lapresse.ca/international/amerique-latine/2012...
Et en Europe : ?

Contre toutes censures, un livre aborde pour la première fois l'agriculture et sa logique de mort, il s'annonce comme un best-seller :
L’AGROTERRORISME DANS NOS ASSIETTES
Michel Tarrier, 256 pages, Éditions LME
http://www.amazon.fr/Agroterrorisme-dans-assiettes-Michel...
Consultez aussi :
http://www.notre-planete.info/actualites/com.php?id=2122
Et pour en parler, vous pouvez rejoindre ce réseau :
http://www.facebook.com/groups/paysansvoyous/
19:14 Publié dans Environnement-Écologie, Pollution | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |
23/07/2012
Kokopelli : Biodiversité sacrifiée sur l'autel de la productivité
La Biodiversité sacrifiée
sur l'autel de la productivité
La Cour de Justice de l'Union Européenne désavoue Kokopelli et son propre avocat général
Suite au jugement scandaleux de la Cour Européenne de Justice — qui prouve une fois de plus que ces institutions Européennes sont complètement corrompues et à la botte des banskters, du Cartel de la Chimie, des multinationales biocidaires et autres marionnettes politiques — certains amis de Kokopelli ont pensé qu'il était adéquat de relancer des énièmes pétitions pour la défense des semences libres.
(Pour plus de détails, voir l'article correspondant sur le site de Kokopelli.)
10:09 Publié dans Actualité des Sciences, Pollution | Tags : kokopelli, semences, cour européenne de justice | Lien permanent | Commentaires (0) | ![]() Facebook | | |
Facebook | | |